تشخیص و انهدام سلولهای سرطانی با حسگر پروتئینی
محققان برای ساخت این سیستم جدید، باید قابلیت اتصال به دیانای انگشتان زینک را با یک پیامد – فعال کردن یک پروتئین فلورسنت برای نمایش حضور دیانای مئورد نظر یا ایجاد فعالیت دیگری در داخل سلول- مرتبط میکردند. آنها توانستند با استفاده از پروتئینی موسوم به «intein» توانستند این امر را محقق کنند. این پروتئین کوتاه میتواند درون یک پروتئین بزرگتر قرار گرفته و به دو قطعه تقسیم شود.
محققان MIT همچنین این سیستم را با مرتبط کردن شناسایی دیانای با تولید آنزیمی موسوم به NTR، برای کشتن سلولها مورد استفاده قرار دادند. آنها اکنون این سیستم را برای شناسایی ویروس نهفته اچآیوی که حتی بعد از درمان نیز در برخی سلولهای آلوده، نهفته میمانند، سازگار کردهاند. یادگیری بیشتر در مورد چنین ویروسهایی میتواند به دانشمندان در شناسایی روشهایی برای حذف کامل آنها کمک کند. یافتههای این تحقیق در مجله Nature Methods منتشر شده است.
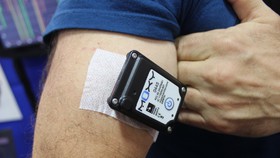 مهندسان در امریکا نوعی مانیتور چسبی به نام Moxy ارائه دادهاند که به ورزشکاران دریچه جدیدی برای نظارت بر عملکرد بدنشان حین تمرینات ورزشی ارائه میدهد. این سیستم سطوح اکسیژن موجود در عضلات ورزشکاران را به صورت فوری رهگیری کرده و اطلاعات دریافتی را به همراه دادههای سلامتی در برنامه نرمافزاری و تلفن همراه آنها نمایش میدهد.
مهندسان در امریکا نوعی مانیتور چسبی به نام Moxy ارائه دادهاند که به ورزشکاران دریچه جدیدی برای نظارت بر عملکرد بدنشان حین تمرینات ورزشی ارائه میدهد. این سیستم سطوح اکسیژن موجود در عضلات ورزشکاران را به صورت فوری رهگیری کرده و اطلاعات دریافتی را به همراه دادههای سلامتی در برنامه نرمافزاری و تلفن همراه آنها نمایش میدهد. 
 محققان انگلیسی حسگر جدیدی را توسعه دادهاند که با قرار گرفتن در پایههای تختخواب، وضعیت چرخه خواب شبانگاهی فرد را مورد بررسی قرار میدهد. دستگاه Bed Scales مجموعهیی از حسگرهاست که در پایههای تختخواب قرار داده شده و علاوه بر بررسی چرخه خواب شبانگاهی، تغییرات وزن در هنگام خواب را اندازه گیری میکند. این دستگاه همچنین از قابلیت بیدار کردن فرد در دوره خواب سبک برای پیشگیری از بیخوابی در نیمه شب برخوردار است. بر خلاف دستگاههای پوشیدنی مانند Fibit، FuelBand یا حسگرهایی که زیر بالش یا تشک قرار داده میشوند، کاربر در هنگام خواب از هیچ وسیله خاصی استفاده نکرده و حسگرها در قسمت پایه تخت براحتی وضعیت چرخه خواب شبانگاهی را بررسی میکنند. محققان شرکت Genetrainer بدنبال جذب سرمایه برای تجاریسازی طرح حسگر خواب هستند.
محققان انگلیسی حسگر جدیدی را توسعه دادهاند که با قرار گرفتن در پایههای تختخواب، وضعیت چرخه خواب شبانگاهی فرد را مورد بررسی قرار میدهد. دستگاه Bed Scales مجموعهیی از حسگرهاست که در پایههای تختخواب قرار داده شده و علاوه بر بررسی چرخه خواب شبانگاهی، تغییرات وزن در هنگام خواب را اندازه گیری میکند. این دستگاه همچنین از قابلیت بیدار کردن فرد در دوره خواب سبک برای پیشگیری از بیخوابی در نیمه شب برخوردار است. بر خلاف دستگاههای پوشیدنی مانند Fibit، FuelBand یا حسگرهایی که زیر بالش یا تشک قرار داده میشوند، کاربر در هنگام خواب از هیچ وسیله خاصی استفاده نکرده و حسگرها در قسمت پایه تخت براحتی وضعیت چرخه خواب شبانگاهی را بررسی میکنند. محققان شرکت Genetrainer بدنبال جذب سرمایه برای تجاریسازی طرح حسگر خواب هستند.  یک حسگر جاسازی شده در دندان، در آینده میتواند پزشکان را از زمانهایی که بیماران توصیههای آنها در مورد ترک سیگار یا کم خوردن را نادیده گرفتهاند، آگاه سازد. این حسگر که در یک صفحه مدار بسیار کوچک با قابلیت نصب در حفره دندان ساخته شده، شامل یک شتابسنج برای ارسال داده در مورد حرکت دهان به یک گوشی هوشمند است. نرمافزار یادگیری ماشین برای شناسایی هر الگوی حرکت فک آموزش دیده و سپس میزان زمان جویدن، نوشیدن، صحبت کردن، سرفه یا سیگار کشیدن بیمار را ثبت میکند. مخترعان این حسگر از دانشگاه ملی تایوان در تایپه قصد دارند از دهان به عنوان دریچهای برای انواع مسائل مربوط به سلامت استفاده کنند. این دستگاه میتواند در دندان مصنوعی یا مهاربند دندانها نصب شود و مخترعان قصد دارند دستگاهها را به اندازهای کوچک کنند که در حفره یا تاج دندان جای بگیرد.
یک حسگر جاسازی شده در دندان، در آینده میتواند پزشکان را از زمانهایی که بیماران توصیههای آنها در مورد ترک سیگار یا کم خوردن را نادیده گرفتهاند، آگاه سازد. این حسگر که در یک صفحه مدار بسیار کوچک با قابلیت نصب در حفره دندان ساخته شده، شامل یک شتابسنج برای ارسال داده در مورد حرکت دهان به یک گوشی هوشمند است. نرمافزار یادگیری ماشین برای شناسایی هر الگوی حرکت فک آموزش دیده و سپس میزان زمان جویدن، نوشیدن، صحبت کردن، سرفه یا سیگار کشیدن بیمار را ثبت میکند. مخترعان این حسگر از دانشگاه ملی تایوان در تایپه قصد دارند از دهان به عنوان دریچهای برای انواع مسائل مربوط به سلامت استفاده کنند. این دستگاه میتواند در دندان مصنوعی یا مهاربند دندانها نصب شود و مخترعان قصد دارند دستگاهها را به اندازهای کوچک کنند که در حفره یا تاج دندان جای بگیرد.  محققان سوئیسی موفق به ارائه روش تشخیصی جدیدی برای شناسایی آر.ان.ای سلول سرطانی پوست شدند. تومور سیاه پوست یکی از خطرناکترین سرطانهای پوست محسوب میشود. در 50 درصد موارد، یک ژن جهش یافته مسؤول بروز این بیماری است. از آنجاییکه شانس و مدت زنده ماندن بیمارانی که دچار این جهش ژنی شدند، میتواند با استعمال یک داروی جدید به شدت افزایش یابد، به همین دلیل یافتن راهی برای شناسایی زودهنگام این جهش بسیار مهم است. برای حل این مشکل یک تیم تحقیقاتی از دانشگاه بازل با همکاری محققانی از موسسه تحقیقات سرطان لودوینگ روش جدیدی ارائه کردهاند.
محققان سوئیسی موفق به ارائه روش تشخیصی جدیدی برای شناسایی آر.ان.ای سلول سرطانی پوست شدند. تومور سیاه پوست یکی از خطرناکترین سرطانهای پوست محسوب میشود. در 50 درصد موارد، یک ژن جهش یافته مسؤول بروز این بیماری است. از آنجاییکه شانس و مدت زنده ماندن بیمارانی که دچار این جهش ژنی شدند، میتواند با استعمال یک داروی جدید به شدت افزایش یابد، به همین دلیل یافتن راهی برای شناسایی زودهنگام این جهش بسیار مهم است. برای حل این مشکل یک تیم تحقیقاتی از دانشگاه بازل با همکاری محققانی از موسسه تحقیقات سرطان لودوینگ روش جدیدی ارائه کردهاند. محققان دانشگاه واشنگتن یک حسگر زیستپزشکی را با استفاده از نانومیلههای طلا، برای تشخیص افزایش لیپوکالین وابسته به ژلاتیناز نوتروفیل بعنوان یک زیستنشانگر آسیبهای حاد کلیه ساختهاند. یافتههای «اِوان کراش» و همکارانش در دانشکده پزشکی دانشگاه واشنگتن تشخیص آسیبهای جدی کلیه را به سادگی از طریق فرو بردن یک کاغذ آزمایش در ادرار میسر کرده است. زیستنشانگرها عموما مولکولها یا پروتئینهای کوچکی در بدن هستند که با تغییر غلظت در بدن به بیماری و یا درمان پاسخ میدهند. «کراش» معتقد است که این فناوری مبتکرانه بررسی عملکرد کلیه را بصورت بالینی و با هزینه کمتر فراهم میآورد.
محققان دانشگاه واشنگتن یک حسگر زیستپزشکی را با استفاده از نانومیلههای طلا، برای تشخیص افزایش لیپوکالین وابسته به ژلاتیناز نوتروفیل بعنوان یک زیستنشانگر آسیبهای حاد کلیه ساختهاند. یافتههای «اِوان کراش» و همکارانش در دانشکده پزشکی دانشگاه واشنگتن تشخیص آسیبهای جدی کلیه را به سادگی از طریق فرو بردن یک کاغذ آزمایش در ادرار میسر کرده است. زیستنشانگرها عموما مولکولها یا پروتئینهای کوچکی در بدن هستند که با تغییر غلظت در بدن به بیماری و یا درمان پاسخ میدهند. «کراش» معتقد است که این فناوری مبتکرانه بررسی عملکرد کلیه را بصورت بالینی و با هزینه کمتر فراهم میآورد.  محققان دانشگاه صنعتی مونیخ حسگر جدیدی مبتنی بر حفرههای نانومقیاس از جنس نیمههادی تولید کردهاند.
محققان دانشگاه صنعتی مونیخ حسگر جدیدی مبتنی بر حفرههای نانومقیاس از جنس نیمههادی تولید کردهاند.  پژوهشگران
پژوهشگران مهندسان آمریکایی نسل جدید حسگر کنترل علائم حیاتی بدن را در ابعاد و ضخامت یک تمبر طراحی کردهاند که با وزن بسیار سبک و اندازه کوچک، براحتی به پانسمان بدن بیمار متصل میشود. گروهی از مهندسان برق دانشگاه ایالتی اورگان نسل جدید حسگر «سیستم بر روی تراشه» را طراحی کردهاند که در حجم بالا قابل تولید است. این حسگر الکترونیکی یک بار مصرف و ارزان قیمت، از عملکرد بسیار دقیقی برای کنترل علائم حیاتی بیمار برخوردار است. پروفسور «پاتریک چیانگ» از محققان دانشگاه اورگان تأکید میکند: فناوریهای کنونی امکان اندازهگیری سیگنالهای بدن را با استفاده از ابزار و دستگاههای بزرگ، سنگین و پر هزینه فراهم کردهاند، اما حسگر جدید یک وسیله سبک و کوچک است که با هزینهای بسیار کم تولید میشود.
مهندسان آمریکایی نسل جدید حسگر کنترل علائم حیاتی بدن را در ابعاد و ضخامت یک تمبر طراحی کردهاند که با وزن بسیار سبک و اندازه کوچک، براحتی به پانسمان بدن بیمار متصل میشود. گروهی از مهندسان برق دانشگاه ایالتی اورگان نسل جدید حسگر «سیستم بر روی تراشه» را طراحی کردهاند که در حجم بالا قابل تولید است. این حسگر الکترونیکی یک بار مصرف و ارزان قیمت، از عملکرد بسیار دقیقی برای کنترل علائم حیاتی بیمار برخوردار است. پروفسور «پاتریک چیانگ» از محققان دانشگاه اورگان تأکید میکند: فناوریهای کنونی امکان اندازهگیری سیگنالهای بدن را با استفاده از ابزار و دستگاههای بزرگ، سنگین و پر هزینه فراهم کردهاند، اما حسگر جدید یک وسیله سبک و کوچک است که با هزینهای بسیار کم تولید میشود. محققان مؤسسه مهندسی زیستپزشکی فرانهوفر آلمان، حسگر ضد رطوبت جدیدی را برای ارزیابی فشار مغزی ابداع کردهاند که میتواند به تشخیص زودهنگام زوال عقل و جنون منجر شود. این حسگر که مشابه حسگرهای فشار مورد استفاده در صنعت خودروسازی بوده، نشانگر یک تحول از کاشتهای پیشین است که به رطوبت اجازه ورود و تخریب دستگاه را میدادند. این دستگاه از ارتفاع و عرض یک در دو سانتیمتر برخوردار بوده و انتظار میرود تا در نسخههای آینده کوچکتر شود. محققان آلمانی قاب خارجی آن را که پیش از این از مواد مصنوعی ساخته میشد با فلز درجه بالای قابل انعطاف تعویض کردند. تغییرات فشار درون مغز باعث خم شدن این قاب شده و این اطلاعات سپس به حسگر فشار درون آن منتقل میشود. مقادیر اندازهگیری شده در نهایت از طریق پالسهای رادیویی به یک دستگاه خوانش در خارج از بدن بیمار انتقال یافته که نیروی مورد نیاز حسگر را تامین میکند و از این رو دیگر نیازی به پیل بر روی این دستگاه نیست.
محققان مؤسسه مهندسی زیستپزشکی فرانهوفر آلمان، حسگر ضد رطوبت جدیدی را برای ارزیابی فشار مغزی ابداع کردهاند که میتواند به تشخیص زودهنگام زوال عقل و جنون منجر شود. این حسگر که مشابه حسگرهای فشار مورد استفاده در صنعت خودروسازی بوده، نشانگر یک تحول از کاشتهای پیشین است که به رطوبت اجازه ورود و تخریب دستگاه را میدادند. این دستگاه از ارتفاع و عرض یک در دو سانتیمتر برخوردار بوده و انتظار میرود تا در نسخههای آینده کوچکتر شود. محققان آلمانی قاب خارجی آن را که پیش از این از مواد مصنوعی ساخته میشد با فلز درجه بالای قابل انعطاف تعویض کردند. تغییرات فشار درون مغز باعث خم شدن این قاب شده و این اطلاعات سپس به حسگر فشار درون آن منتقل میشود. مقادیر اندازهگیری شده در نهایت از طریق پالسهای رادیویی به یک دستگاه خوانش در خارج از بدن بیمار انتقال یافته که نیروی مورد نیاز حسگر را تامین میکند و از این رو دیگر نیازی به پیل بر روی این دستگاه نیست. دانشمندان چینی توانستهاند که با استفاده از یک زیستحسگر نانوسیمی دو نوع مختلف آنفلوآنزا را در عرض چند دقیقه تشخیص دهند. این دانشمندان امیدوارند که افزاره آنها انقلابی در تشخیص آنفلوآنزا ایجاد کند و شیوع بیماری را در یک رخداد فراگیر به کنترل درآورد. اپیدمیهای سالیانه آنفلوآنزا توسط دو نوع اصلی رخ میدهند و منجر به پنج میلیون مورد وخیم در سال با بیش از 500 هزار مرگ میشوند. آنفلوآنزای A انسانی یا از نوع H3N2 است یا H1N1 که به آنفلوانزای خوکی نیز معروف است. سهولت انتقال این بیماری، یک تست تشخیصی ساده و معتبر برای پزشکان مهیا میکند.
دانشمندان چینی توانستهاند که با استفاده از یک زیستحسگر نانوسیمی دو نوع مختلف آنفلوآنزا را در عرض چند دقیقه تشخیص دهند. این دانشمندان امیدوارند که افزاره آنها انقلابی در تشخیص آنفلوآنزا ایجاد کند و شیوع بیماری را در یک رخداد فراگیر به کنترل درآورد. اپیدمیهای سالیانه آنفلوآنزا توسط دو نوع اصلی رخ میدهند و منجر به پنج میلیون مورد وخیم در سال با بیش از 500 هزار مرگ میشوند. آنفلوآنزای A انسانی یا از نوع H3N2 است یا H1N1 که به آنفلوانزای خوکی نیز معروف است. سهولت انتقال این بیماری، یک تست تشخیصی ساده و معتبر برای پزشکان مهیا میکند.  طراحان امیدوارند با افزودن حسگرهای مادون قرمز به تلفن همراه هوشمند، این دستگاه را به یک دماسنج بسیار حساس تبدیل کنند. نسل جدید تلفنهای همراه هوشمند به دوربینهای حساس، صفحات نمایشی لمسی و نرم افزارهای کاربردی مجهز شده اند و محققان امیدوارند که کاربرد تلفن همراه با افزودن حسگرهای مادون قرمز چند برابر شود. اندازه گیری درجه حرارت بدن نوزادان و کودکان یکی از دغدغه های والدین محسوب می شود؛ «جاکوب فرادن» در طرح ابتکاری خود قصد دارد از حسگرهای مادون قرمز بر روی تلفن همراه هوشمند بعنوان دماسنج استفاده کند. لنزهای مادون قرمز بدون برآمدگی در کنار دوربین تلفن همراه تعبیه می شوند و کاربر با نگه داشتن دستگاه مقابل پیشانی کودک می تواند در مدت یک ثانیه درجه حرارت بدن را با دقت بسیار بالا اندازه گیری کند.
طراحان امیدوارند با افزودن حسگرهای مادون قرمز به تلفن همراه هوشمند، این دستگاه را به یک دماسنج بسیار حساس تبدیل کنند. نسل جدید تلفنهای همراه هوشمند به دوربینهای حساس، صفحات نمایشی لمسی و نرم افزارهای کاربردی مجهز شده اند و محققان امیدوارند که کاربرد تلفن همراه با افزودن حسگرهای مادون قرمز چند برابر شود. اندازه گیری درجه حرارت بدن نوزادان و کودکان یکی از دغدغه های والدین محسوب می شود؛ «جاکوب فرادن» در طرح ابتکاری خود قصد دارد از حسگرهای مادون قرمز بر روی تلفن همراه هوشمند بعنوان دماسنج استفاده کند. لنزهای مادون قرمز بدون برآمدگی در کنار دوربین تلفن همراه تعبیه می شوند و کاربر با نگه داشتن دستگاه مقابل پیشانی کودک می تواند در مدت یک ثانیه درجه حرارت بدن را با دقت بسیار بالا اندازه گیری کند.  دانشمندان مؤسسه علمی وایزمن در تلاش برای کمک به نابینایان در مسیریابی ایمنتر و موثرتر از یک منبع غیرمنتظره یعنی سبیلهای موش الهام گرفتهاند. این محققان از داوطلبان خواسته بودند تا چشمبند بسته و از یک سبیل پلاستیکی منعطف 30 سانتیمتری بر روی انگشت اشاره که در پایه آن حسگرهای نیرو و موقعیت قرار گرفته بود، برای مسیریابی استفاده کنند. در دنیای موشها، حرکت سبیلها شامل عقب و جلو بردن آنها در حدود هشت بار در یک ثانیه برای موقعیت یابی اجسام در محیط اطرافشان است. این نتایج که در مجله Neuroscience منتشر شده، میتواند به درک بهتر از فرآیند حس و ساخت دستگاههای کوچک قابل پوشش بر روی دست منجر شود که ورودیهای ویدیویی را به تحریک مکانیکی تبدیل کرده و به نابینایان یک کمک حسی شهودی ارائه میکنند.
دانشمندان مؤسسه علمی وایزمن در تلاش برای کمک به نابینایان در مسیریابی ایمنتر و موثرتر از یک منبع غیرمنتظره یعنی سبیلهای موش الهام گرفتهاند. این محققان از داوطلبان خواسته بودند تا چشمبند بسته و از یک سبیل پلاستیکی منعطف 30 سانتیمتری بر روی انگشت اشاره که در پایه آن حسگرهای نیرو و موقعیت قرار گرفته بود، برای مسیریابی استفاده کنند. در دنیای موشها، حرکت سبیلها شامل عقب و جلو بردن آنها در حدود هشت بار در یک ثانیه برای موقعیت یابی اجسام در محیط اطرافشان است. این نتایج که در مجله Neuroscience منتشر شده، میتواند به درک بهتر از فرآیند حس و ساخت دستگاههای کوچک قابل پوشش بر روی دست منجر شود که ورودیهای ویدیویی را به تحریک مکانیکی تبدیل کرده و به نابینایان یک کمک حسی شهودی ارائه میکنند.  محققان دانشگاه ميسوري- كلمبيا موفق به تبديل گلبولهاي قرمز به حسگرهاي شيميايي شدند كه ميتواند ضمن بازگشت به سيستم گردش خون، براي بررسي وضعيت لحظهاي خون در بدن بيمار مورد استفاده قرار گيرد. بسياري از بيماران مانند افراد مبتلا به ديابت بايد بصورت مستمر و در يك روش تهاجمي، سطح گلوگز را از طريق دستگاه اندازه گيري سطح قند خون مورد بررسي قرار دهند. همزمان با برگزاري نشست انجمن شيمي آمريكا در شهر فيلادلفيا، دستاورد جديد محققان شيمي دانشگاه ميسوري در توليد حسگرهاي شيميايي از سلول هاي خون معرفي شد كه مي تواند در آينده در يك روش غير تهاجمي و طولاني براي بررسي خون مورد استفاده قرار بگيرد. به گفته «شيائول شائو» سرپرست تيم تحقيقاتي، نور نزديك به مادون قرمز ميتواند از طريق پوست وارد بدن شود و بر مولكول هاي فلورسنت در حال گردش در خون تأثير بگذارد.
محققان دانشگاه ميسوري- كلمبيا موفق به تبديل گلبولهاي قرمز به حسگرهاي شيميايي شدند كه ميتواند ضمن بازگشت به سيستم گردش خون، براي بررسي وضعيت لحظهاي خون در بدن بيمار مورد استفاده قرار گيرد. بسياري از بيماران مانند افراد مبتلا به ديابت بايد بصورت مستمر و در يك روش تهاجمي، سطح گلوگز را از طريق دستگاه اندازه گيري سطح قند خون مورد بررسي قرار دهند. همزمان با برگزاري نشست انجمن شيمي آمريكا در شهر فيلادلفيا، دستاورد جديد محققان شيمي دانشگاه ميسوري در توليد حسگرهاي شيميايي از سلول هاي خون معرفي شد كه مي تواند در آينده در يك روش غير تهاجمي و طولاني براي بررسي خون مورد استفاده قرار بگيرد. به گفته «شيائول شائو» سرپرست تيم تحقيقاتي، نور نزديك به مادون قرمز ميتواند از طريق پوست وارد بدن شود و بر مولكول هاي فلورسنت در حال گردش در خون تأثير بگذارد.  سالهاست که قرار دادن مدارهای الکترونیکی درون بافتهای بدن یک نوع داستان علمی تخیلی محسوب میشده است، اما اخیرا پژوهشگران آمریکایی راهی برای رشد بافتهای زنده یافتهاند که درون آنها حسگرهای الکترونیکی قرار دارد. نتایج این پژوهش میتواند منجر به ساخت اندامهای سنتز شده و جایگزینی آنها در بدن شود.
سالهاست که قرار دادن مدارهای الکترونیکی درون بافتهای بدن یک نوع داستان علمی تخیلی محسوب میشده است، اما اخیرا پژوهشگران آمریکایی راهی برای رشد بافتهای زنده یافتهاند که درون آنها حسگرهای الکترونیکی قرار دارد. نتایج این پژوهش میتواند منجر به ساخت اندامهای سنتز شده و جایگزینی آنها در بدن شود.  محققان دانشگاه ايلينويز در حال طراحي بخيه الكترونيكي هوشمندي هستند كه مي تواند در آينده براي تشخيص عفونت در محل زخم و كمك به بهبود سريعتر مورد استفاده قرار گيرد. نمونه اوليه بخيه الكترونيكي هوشمند توسط پروفسور «جان راجرز» طراحي شده كه از حسگرهاي سيليكوني فوق باريك متصل به نوارهاي پليمري يا ابريشمي استفاده ميكند. اين حسگرها در زمان تماس با پوست مي توانند نشانه هاي بروز عفونت را شناسايي كنند و حتي قادر هستند با افزايش دما به از بين رفتن عفونت در محل زخم نيز كمك كنند؛ ديويد سيليكون و نانو غشاي پلاتين به عنوان حسگرهاي گرمايي استفاده ميشوند. براي ساخت حسگرهاي نازك، محققان با استفاده از مواد شيميايي، قطعه كوچكي از سيليكون را از يك ويفر سيليكون برش دادند و سپس از يك مهر لاستيكي براي انتقال غشاي نانو به نوار پليمري يا ابريشمي استفاده كردند؛ با افزودن الكترودهاي فلزي و سيمها در بالاي نوار، دستگاه در لايهاي از اپوكسي پوشش داده شد. نتايج اين دستاورد در مجله Small منتشر شده است.
محققان دانشگاه ايلينويز در حال طراحي بخيه الكترونيكي هوشمندي هستند كه مي تواند در آينده براي تشخيص عفونت در محل زخم و كمك به بهبود سريعتر مورد استفاده قرار گيرد. نمونه اوليه بخيه الكترونيكي هوشمند توسط پروفسور «جان راجرز» طراحي شده كه از حسگرهاي سيليكوني فوق باريك متصل به نوارهاي پليمري يا ابريشمي استفاده ميكند. اين حسگرها در زمان تماس با پوست مي توانند نشانه هاي بروز عفونت را شناسايي كنند و حتي قادر هستند با افزايش دما به از بين رفتن عفونت در محل زخم نيز كمك كنند؛ ديويد سيليكون و نانو غشاي پلاتين به عنوان حسگرهاي گرمايي استفاده ميشوند. براي ساخت حسگرهاي نازك، محققان با استفاده از مواد شيميايي، قطعه كوچكي از سيليكون را از يك ويفر سيليكون برش دادند و سپس از يك مهر لاستيكي براي انتقال غشاي نانو به نوار پليمري يا ابريشمي استفاده كردند؛ با افزودن الكترودهاي فلزي و سيمها در بالاي نوار، دستگاه در لايهاي از اپوكسي پوشش داده شد. نتايج اين دستاورد در مجله Small منتشر شده است. محققان امريکايي با استفاده از نانولولههاي کربني موفق به توليد حسگر زيستي جديدي شدهاند. اين حسگر ميتواند سرعت انجام تستهاي پزشکي را افزايش دهد. پژوهشگران دانشگاه ايالتي «اورگون» از ويژگيهاي نانولولههاي کربني براي ساخت حسگرهاي زيستي استفاده کردند. با چنين حسگري ميتوان در زماني بسيار کوتاه و هزينه اندک، تشخيص و درمان بيماري را انجام داد. نتايج تحقيقات اخير منجر به توليد يک نوع حسگر زيستي جديد شده است که نه تنها ميتواند در پزشکي مورد استفاده قرار گيرد، بلکه در حوزههاي سم شناسي، ساخت داروهاي جديد و مسائل زيست محيطي ميتوان از آن استفاده کرد. نتايج اين تحقيق در نشريه «Lab on a Chip» به چاپ رسيده است.
محققان امريکايي با استفاده از نانولولههاي کربني موفق به توليد حسگر زيستي جديدي شدهاند. اين حسگر ميتواند سرعت انجام تستهاي پزشکي را افزايش دهد. پژوهشگران دانشگاه ايالتي «اورگون» از ويژگيهاي نانولولههاي کربني براي ساخت حسگرهاي زيستي استفاده کردند. با چنين حسگري ميتوان در زماني بسيار کوتاه و هزينه اندک، تشخيص و درمان بيماري را انجام داد. نتايج تحقيقات اخير منجر به توليد يک نوع حسگر زيستي جديد شده است که نه تنها ميتواند در پزشکي مورد استفاده قرار گيرد، بلکه در حوزههاي سم شناسي، ساخت داروهاي جديد و مسائل زيست محيطي ميتوان از آن استفاده کرد. نتايج اين تحقيق در نشريه «Lab on a Chip» به چاپ رسيده است.  دانشمندان دانشگاه پرینستون موفق به ساخت حسگر دهاني به نازکی کاغذ شدهاند که قابل خالکوبی بر روی دندان بوده و به عنوان یک سیستم هشدار اولیه فوق حساس برای تشخيص بیماریها از راه تنفس فرد عمل میکند. این حسگر از گرافن ساخته شده و قادر به شناسایی باکتری و انتقال اطلاعات به کادر پزشکی است. در آزمایشات انجام شده، یک داوطلب روی این حسگر که بر دندانهای یک گاو کاشته شده بود، به تنفس پرداخته و این حسگر توانست مولکولهای باکتری موجود در نفس وی را شناسایی کند. این حسگر بیسیم، قابل نصب بر روی دندان بوده و قادر به تشخیص عفونت و انتقال اطلاعات به متخصصان پزشکی است. محققان بر این باورند که میتوان از این حسگرها برای کارکنان ارتش حاضر در میدان جنگ جهت تشخیص امکان عفونی شدن جراحات آنها یا در بیمارستانها بر روی بیمارانی که به دلیل سیستم ایمنی ضعیف در برابر باکتریها آسیب پذیر هستند، استفاده کرد. محققان در حال حاضر مشغول برنامهریزی برای کسب مجوز و تجاری کردن این دستگاه هستند.
دانشمندان دانشگاه پرینستون موفق به ساخت حسگر دهاني به نازکی کاغذ شدهاند که قابل خالکوبی بر روی دندان بوده و به عنوان یک سیستم هشدار اولیه فوق حساس برای تشخيص بیماریها از راه تنفس فرد عمل میکند. این حسگر از گرافن ساخته شده و قادر به شناسایی باکتری و انتقال اطلاعات به کادر پزشکی است. در آزمایشات انجام شده، یک داوطلب روی این حسگر که بر دندانهای یک گاو کاشته شده بود، به تنفس پرداخته و این حسگر توانست مولکولهای باکتری موجود در نفس وی را شناسایی کند. این حسگر بیسیم، قابل نصب بر روی دندان بوده و قادر به تشخیص عفونت و انتقال اطلاعات به متخصصان پزشکی است. محققان بر این باورند که میتوان از این حسگرها برای کارکنان ارتش حاضر در میدان جنگ جهت تشخیص امکان عفونی شدن جراحات آنها یا در بیمارستانها بر روی بیمارانی که به دلیل سیستم ایمنی ضعیف در برابر باکتریها آسیب پذیر هستند، استفاده کرد. محققان در حال حاضر مشغول برنامهریزی برای کسب مجوز و تجاری کردن این دستگاه هستند.