تایید یک داروی جدید برای مقابله با سرطان پستان در بریتانیا
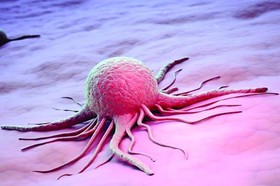
مقامات بریتانیایی اعلام کردهاند که داروی جدیدی که به کاهش سرعت گسترش یک نوع لاعلاج از سرطان پستان کمک میکند، برای استفاده از سوی سازمان بهداشت ملی بریتانیا تایید شده است. داروی جدیدی که به کاهش سرعت گسترش یک نوع غیر قابل درمان از سرطان پستان کمک میکند، برای استفاده در بریتانیا تایید شد. دانشمندان تایید این دارو موسوم به کاپیواسرتیب(capivasertib) از سوی مؤسسه ملی بهداشت و مراقبت عالی بریتانیا(NICE) را به عنوان یک «اتفاق برجسته» توصیف میکنند. سازمان بهداشت ملی بریتانیا(NICE) گفت: بیش از ۱۰۰۰ زن مبتلا به نوع «HER2-منفی» این بیماری «HR مثبت» میتوانند از مصرف دو بار در روز این قرص در هر سال سود ببرند.
این دارو که به نام تجاری تروکاپ(Truqap) نیز شناخته میشود، توسط غول داروسازی بریتانیایی یعنی شرکت آسترازنکا(AstraZeneca) ساخته شده است و به کند کردن یا توقف پیشرفت سرطان کمک میکند، به این معنی که میتواند به برخی از بیماران کمک کند عمر طولانیتری داشته باشند. هلن نایت(Helen Knight)، مدیر ارزیابی دارویی NICE گفت: درمانهایی مانند «کاپیواسرتیب» برای افراد مبتلا به سرطان پیشرفته پستان ارزشمند است، چرا که نیاز به شیمیدرمانی و عوارض جانبی مرتبط با آن را به تاخیر میاندازد.
نوع پیشرفته سرطان پستان دارای جهشهای ژنتیکی خاصی است و در بافت پستان یا سایر قسمتهای بدن گسترش مییابد. قرص «کاپیواسرتیب» با مسدود کردن عملکرد پروتئینی غیرطبیعی که به سلولهای سرطانی میگوید تکثیر شوند، عمل میکند. نتایج یک کارآزمایی بالینی نشان داد که «کاپیواسرتیب» به همراه هورموندرمانی، مدت زمان قبل از بدتر شدن سرطان را در مقایسه با دارونما حدود ۴ ماه افزایش داد.
مؤسسه تحقیقات سرطان(ICR) در لندن از این اقدام که به دنبال دههها تحقیق توسط دانشمندان آن انجام شده است، استقبال کرد. کریستین هلین(Kristian Helin)، مدیر اجرایی ICR گفت: این دارو، درمان این بیماران مبتلا به شایعترین نوع سرطان پیشرفته پستان را بهبود میبخشد. حدود نیمی از بیماران مبتلا به این نوع سرطان پستان دارای جهش در یک یا چند ژن هستند و «کاپیواسرتیب» برای این بیماران میتواند پیشرفت بیماری را متوقف کند. سازمان بهداشت ملی بریتانیا(NICE) میگوید ۴۰ هزار و ۱۹۲ نفر در سال ۲۰۲۰ در این کشور مبتلا به سرطان پستان تشخیص داده شدند که تقریباً ۱۵ درصد از آنها در هنگام تشخیص، به مراحل پیشرفته این بیماری مبتلا بودهاند.
 تیمی از دانشمندان فرانسوی به تازگی یه کاشت فراصوت را برای 15 نفر آزمایش کردهاند که به ارسال بهتر داروهای شیمیدرمانی به تومورهای مغزی کمک میکند. یکی از بزرگترین مشکلات در درمان سرطان مغز این است که تنها مقدار محدودی از داروهای شیمیدرمانی به داخل مغز راه مییابند زیرا رگهای خونی مغز شدیدا به سلولها پیوند خوردهاند تا از ورود مواد سمی و پاتوژنها جلوگیری کنند. اما این سد خونی همچنین از انتقال داروها به تومورها نیز جلوگیری میکند.
تیمی از دانشمندان فرانسوی به تازگی یه کاشت فراصوت را برای 15 نفر آزمایش کردهاند که به ارسال بهتر داروهای شیمیدرمانی به تومورهای مغزی کمک میکند. یکی از بزرگترین مشکلات در درمان سرطان مغز این است که تنها مقدار محدودی از داروهای شیمیدرمانی به داخل مغز راه مییابند زیرا رگهای خونی مغز شدیدا به سلولها پیوند خوردهاند تا از ورود مواد سمی و پاتوژنها جلوگیری کنند. اما این سد خونی همچنین از انتقال داروها به تومورها نیز جلوگیری میکند.  دانشمندان آزمایشگاه جت پیشرانش ناسا در یک تحقیق جدید برای نخستین بار به بررسی میکروبهایی پرداختهاند که ممکن است با سرطان پستان مرتبط باشند. محققان با استفاده از تکنیکهای حفاظت سیارهای که از آلوده نشدن جهانهای دیگر توسط فضاپیماهای ناسا اطمینان حاصل میکند، توانستند ارتباطی بین باکتری موجودت در مایع مجرای پستان و سرطان پستان پیدا کنند. از این روش تعیین توالی و تحلیل برای بررسی باکتریهای موجود در اتاقهای مونتاژ فضاپیما استفاده میشود.
دانشمندان آزمایشگاه جت پیشرانش ناسا در یک تحقیق جدید برای نخستین بار به بررسی میکروبهایی پرداختهاند که ممکن است با سرطان پستان مرتبط باشند. محققان با استفاده از تکنیکهای حفاظت سیارهای که از آلوده نشدن جهانهای دیگر توسط فضاپیماهای ناسا اطمینان حاصل میکند، توانستند ارتباطی بین باکتری موجودت در مایع مجرای پستان و سرطان پستان پیدا کنند. از این روش تعیین توالی و تحلیل برای بررسی باکتریهای موجود در اتاقهای مونتاژ فضاپیما استفاده میشود.  محققان به درک جدیدی از متاستاز دست یافتند که به توسعه روشهای درمانی بهبود یافته کمک کرده و از گسترش تومورها جلوگیری میکند. گروهی از محققان به رهبری دانشمندان دانشگاه کوئین ماری لندن، به موفقیتی بزرگ در درک چگونگی گسترش سلولهای سرطانی دست یافتند که در سراسر بدن گسترش یافته و تومورهای مرگبار جدیدی را شکل میدهند.
محققان به درک جدیدی از متاستاز دست یافتند که به توسعه روشهای درمانی بهبود یافته کمک کرده و از گسترش تومورها جلوگیری میکند. گروهی از محققان به رهبری دانشمندان دانشگاه کوئین ماری لندن، به موفقیتی بزرگ در درک چگونگی گسترش سلولهای سرطانی دست یافتند که در سراسر بدن گسترش یافته و تومورهای مرگبار جدیدی را شکل میدهند.  بررسی محققان دانشگاه تگزاس در آستین نشان داده است که مصرف منظم آسپرین میتواند عود سرطان پستان در زنان چاق و دچار اضافه وزن را به نصف کاهش دهد و طبق یافتههای جدید، مصرف یک آسپرین در روز ممکن است بتواند سدی بر سر راه عود سرطان پستان شود. البته هر فردی ممکن است واکنشهای مختلفی به دارودرمانی داشته باشد و باید قبل از شروع هر نوع برنامه دارویی از پزشک خود مشاوره بگیرد. در واقع تغذیه مناسب و ورزش منظم نیز از مواردی مهمی است که در پیشگیری از سرطان پستان باید به آن توجه شود. سرطان پستان پس از سرطان پوست، شایعترین سرطان برای زنان در آمریکا است و تخمین زده میشود که تا پایان سال جاری میلادی بیش از 230 هزار مورد سرطان پستان تشخیص داده شود که بیش از 40 هزار نفر از این بیماران فوت میکنند.
بررسی محققان دانشگاه تگزاس در آستین نشان داده است که مصرف منظم آسپرین میتواند عود سرطان پستان در زنان چاق و دچار اضافه وزن را به نصف کاهش دهد و طبق یافتههای جدید، مصرف یک آسپرین در روز ممکن است بتواند سدی بر سر راه عود سرطان پستان شود. البته هر فردی ممکن است واکنشهای مختلفی به دارودرمانی داشته باشد و باید قبل از شروع هر نوع برنامه دارویی از پزشک خود مشاوره بگیرد. در واقع تغذیه مناسب و ورزش منظم نیز از مواردی مهمی است که در پیشگیری از سرطان پستان باید به آن توجه شود. سرطان پستان پس از سرطان پوست، شایعترین سرطان برای زنان در آمریکا است و تخمین زده میشود که تا پایان سال جاری میلادی بیش از 230 هزار مورد سرطان پستان تشخیص داده شود که بیش از 40 هزار نفر از این بیماران فوت میکنند. محققان دانشگاه فلوریدا طی پژوهشی دریافتند که ترکیب داروی آزمایشی و داروی معمول مورد استفاده در درمان نوعی سرطان پانکراس (لوزالمعده) میتواند تاثیر بهتری را در مقایسه با استفادۀ تنها از یک داروی خاص برای درمان این نوع سرطان به وجود بیاورد. تومورهای سلولهای جزیرهای که در سلولهای تولید کننده هورمون تشکیل میشوند مسبب بروز 3 تا 5 درصدی بدخیمی پانکراس هستند و توانایی زنده ماندن پنج ساله را دارند. طی سرطان پانکراس نوعی پروتئین در تومورهای سلولهای جزیرهای پانکراس افزایش پیدا کرده و اجازه رشد را به تومور میدهند.
محققان دانشگاه فلوریدا طی پژوهشی دریافتند که ترکیب داروی آزمایشی و داروی معمول مورد استفاده در درمان نوعی سرطان پانکراس (لوزالمعده) میتواند تاثیر بهتری را در مقایسه با استفادۀ تنها از یک داروی خاص برای درمان این نوع سرطان به وجود بیاورد. تومورهای سلولهای جزیرهای که در سلولهای تولید کننده هورمون تشکیل میشوند مسبب بروز 3 تا 5 درصدی بدخیمی پانکراس هستند و توانایی زنده ماندن پنج ساله را دارند. طی سرطان پانکراس نوعی پروتئین در تومورهای سلولهای جزیرهای پانکراس افزایش پیدا کرده و اجازه رشد را به تومور میدهند. محققان موسسه فناوری ماساچوست (MIT) یک حسگر مبتنی بر پروتئین تولید کردهاند که میتواند یک توالی خاص دیانای را در یک سلول شناسایی کرده و سپس باعث واکنش ویژهای مانند مرگ سلول شود. محققان مدعی هستند که این سیستم را میتوان برای شناسایی هر نوع توالی دیانای در یک سلول پستاندار، اصلاح کرده و سپس یک واکنش خاص مانند کشتن سلولهای سرطانی یا سلولهای آلوده به ویروس را امکانپذیر کرد. این فناوری بر اساس گونهای از پروتئینهای متصل شونده به دیانای موسوم به انگشتان زینک است. این پروتئینها میتوانند برای شناسایی هر نوع توالی دیانای طراحی شوند.
محققان موسسه فناوری ماساچوست (MIT) یک حسگر مبتنی بر پروتئین تولید کردهاند که میتواند یک توالی خاص دیانای را در یک سلول شناسایی کرده و سپس باعث واکنش ویژهای مانند مرگ سلول شود. محققان مدعی هستند که این سیستم را میتوان برای شناسایی هر نوع توالی دیانای در یک سلول پستاندار، اصلاح کرده و سپس یک واکنش خاص مانند کشتن سلولهای سرطانی یا سلولهای آلوده به ویروس را امکانپذیر کرد. این فناوری بر اساس گونهای از پروتئینهای متصل شونده به دیانای موسوم به انگشتان زینک است. این پروتئینها میتوانند برای شناسایی هر نوع توالی دیانای طراحی شوند. محققان موسسه سلامت و تحقیقات پزشکی فرانسه میگویند زندگی در کنار بزرگراهها خطر ابتلا به نوعی سرطان خون را افزایش میدهد. پژوهشگران، رویارویی با بنزِن ناشی از تردد خودروها را یکی از توجیهات این رابطه میدانند. طی این پژوهش، محققان به مقایسه 2760 مورد کودک مبتلا به سرطان خون متعلق به سالهای 2002 تا 2007 با 30 هزار کودک سرطانی که در سالهای معاصر زندگی میکنند، پرداختند.
محققان موسسه سلامت و تحقیقات پزشکی فرانسه میگویند زندگی در کنار بزرگراهها خطر ابتلا به نوعی سرطان خون را افزایش میدهد. پژوهشگران، رویارویی با بنزِن ناشی از تردد خودروها را یکی از توجیهات این رابطه میدانند. طی این پژوهش، محققان به مقایسه 2760 مورد کودک مبتلا به سرطان خون متعلق به سالهای 2002 تا 2007 با 30 هزار کودک سرطانی که در سالهای معاصر زندگی میکنند، پرداختند. محققان اسپانیایی دانشگاه ناوارا معتقدند دنبال کردن رژیم مدیترانهای که با مصرف روغن زیتون ناب اضافی همراه باشد، میتواند خطر سرطان پستان را در زنان کاهش دهد. محققان طی این پژوهش 4282 زن 60 تا 80 ساله را که در خطر بیماریهای قلبی و عروقی قرار داشتند، مورد بررسی قرار دادند.
محققان اسپانیایی دانشگاه ناوارا معتقدند دنبال کردن رژیم مدیترانهای که با مصرف روغن زیتون ناب اضافی همراه باشد، میتواند خطر سرطان پستان را در زنان کاهش دهد. محققان طی این پژوهش 4282 زن 60 تا 80 ساله را که در خطر بیماریهای قلبی و عروقی قرار داشتند، مورد بررسی قرار دادند. یک پژوهش جدید بیانگر آن است که چگونه حرارت فلفلهای تند به مرگ سلولهای سرطانی کمک میکند. ترکیبات کاپسایسین که مسؤول حرارت فلفلهای تند است، در کرمهایی که برای تسکین درد به فروش میرسد، استفاده می شود و تحقیقات اخیر نشان داده که این ماده در دوزهای بالا، سلولهای سرطانی پروستات را از بین میبرد. در حال حاضر محققان در حال پیدا کردن سرنخهایی هستند که به چگونگی عملکرد این ماده کمک میکند. نتایج تحقیقات حاکی از آن است که در آینده میتوان این مواد را در شکل جدید و درمانی آن به کار برد.
یک پژوهش جدید بیانگر آن است که چگونه حرارت فلفلهای تند به مرگ سلولهای سرطانی کمک میکند. ترکیبات کاپسایسین که مسؤول حرارت فلفلهای تند است، در کرمهایی که برای تسکین درد به فروش میرسد، استفاده می شود و تحقیقات اخیر نشان داده که این ماده در دوزهای بالا، سلولهای سرطانی پروستات را از بین میبرد. در حال حاضر محققان در حال پیدا کردن سرنخهایی هستند که به چگونگی عملکرد این ماده کمک میکند. نتایج تحقیقات حاکی از آن است که در آینده میتوان این مواد را در شکل جدید و درمانی آن به کار برد. محققان آمریکایی استراتژی جدیدی را برای حمله به سلولهای سرطانی کشف کردهاند که از پتانسیل کاهش عوارض جانبی درمان برخوردار بوده و بطور بنیادی مسیر درمانی و شیوه جلوگیری پزشکان از پیشرفت این بیماری را تغییر میدهد. جان هر، یکی از محققان دانشکده پزشکی دانشگاه ویرجینیا اظهار کرد: ما معتقدیم در مسیری قرار داریم که نه تنها به طور خاص سلولهای سرطانی را هدف قرار میدهد، بلکه میتواند در خط مقدم درمان زنان مبتلا به سرطانهای مختلف که خواهان حفظ باروریشان هستند، قرار بگیرد.
محققان آمریکایی استراتژی جدیدی را برای حمله به سلولهای سرطانی کشف کردهاند که از پتانسیل کاهش عوارض جانبی درمان برخوردار بوده و بطور بنیادی مسیر درمانی و شیوه جلوگیری پزشکان از پیشرفت این بیماری را تغییر میدهد. جان هر، یکی از محققان دانشکده پزشکی دانشگاه ویرجینیا اظهار کرد: ما معتقدیم در مسیری قرار داریم که نه تنها به طور خاص سلولهای سرطانی را هدف قرار میدهد، بلکه میتواند در خط مقدم درمان زنان مبتلا به سرطانهای مختلف که خواهان حفظ باروریشان هستند، قرار بگیرد.  محققان دانشگاه پزشکی جنوب چین، مولکولی را کشف کردهاند که می تواند در پیش بینی شانس زنده ماندن افراد مبتلا به سرطان معده که در مراحل بحرانی قرار دارند، موثر باشد. محققان طی این پژوهش دریافتند بیمارانی که سطوح بالایی از miR-506 را دارند، در مقایسه با افراد فاقد که این مولکول، به طور چشمگیری شانس بیشتری برای زنده ماندن دارند. علاوه بر این، مولکول miR-506 باعث توقف تومور، تشکیل رگهای خونی و متاستاز شدن میشود.
محققان دانشگاه پزشکی جنوب چین، مولکولی را کشف کردهاند که می تواند در پیش بینی شانس زنده ماندن افراد مبتلا به سرطان معده که در مراحل بحرانی قرار دارند، موثر باشد. محققان طی این پژوهش دریافتند بیمارانی که سطوح بالایی از miR-506 را دارند، در مقایسه با افراد فاقد که این مولکول، به طور چشمگیری شانس بیشتری برای زنده ماندن دارند. علاوه بر این، مولکول miR-506 باعث توقف تومور، تشکیل رگهای خونی و متاستاز شدن میشود.  دانشمندان موفق به توضیح چگونگی توانایی سم نوعی زنبور برزیلی در نابودکردن سلولهای سرطانی بدون آسیبرساندن به سلولهای عادی شدند. زنبور اجتماعی Polybia paulista با تولیدکردن زهری که حاوی نوعی ماده مبارزهکننده قدرتمند با سرطان است، از خود محافظت میکند.
دانشمندان موفق به توضیح چگونگی توانایی سم نوعی زنبور برزیلی در نابودکردن سلولهای سرطانی بدون آسیبرساندن به سلولهای عادی شدند. زنبور اجتماعی Polybia paulista با تولیدکردن زهری که حاوی نوعی ماده مبارزهکننده قدرتمند با سرطان است، از خود محافظت میکند.  پژوهشگران تورنتو و بریتیش کلمبیا در پژوهش های خود دریافتهاند نرخ عود موضعی بیماران با خطر پایین لومینال زیرگروه مولکولی نوعSubtype A)A) که بدون رادیوتراپی پس از لامپکتومی تاموکسیفن دریافت کردهاند، تنها 1.3 درصد در 10 سال است. توانایی رادیوتراپی برای کاهش ریسک عود موضعی سرطان پستان پس از جراحی حفظ پستان، مسلم و اثبات شده است. اما برای بعضی زیرگروهها، این فایده آنقدرکم است که از رادیوتراپی اجتناب میشود.
پژوهشگران تورنتو و بریتیش کلمبیا در پژوهش های خود دریافتهاند نرخ عود موضعی بیماران با خطر پایین لومینال زیرگروه مولکولی نوعSubtype A)A) که بدون رادیوتراپی پس از لامپکتومی تاموکسیفن دریافت کردهاند، تنها 1.3 درصد در 10 سال است. توانایی رادیوتراپی برای کاهش ریسک عود موضعی سرطان پستان پس از جراحی حفظ پستان، مسلم و اثبات شده است. اما برای بعضی زیرگروهها، این فایده آنقدرکم است که از رادیوتراپی اجتناب میشود. محققان مراکز سرطان شناسی مختلف اروپایی در تازهترین تحقیقات خود دریافتهاند نشانگرهای زیستی خاص میتوانند در آزمایش تشخیصی برای شناسایی سرطان کولون و رکتوم (کولورکتال) نقش داشته باشند. این امر شناسایی سرطان کولورکتال را که سومین سرطان متداول در جهان و دومین عامل مرگومیر ناشی از سرطان در جهان است، در مراحل اولیه با استفاده از یک آزمایش خون ساده میسر میکند. اگر این سرطان سریع تشخیص داده شود شانس درمان آن بالا است، اما تشخیص سریع آن قطعی نیست.
محققان مراکز سرطان شناسی مختلف اروپایی در تازهترین تحقیقات خود دریافتهاند نشانگرهای زیستی خاص میتوانند در آزمایش تشخیصی برای شناسایی سرطان کولون و رکتوم (کولورکتال) نقش داشته باشند. این امر شناسایی سرطان کولورکتال را که سومین سرطان متداول در جهان و دومین عامل مرگومیر ناشی از سرطان در جهان است، در مراحل اولیه با استفاده از یک آزمایش خون ساده میسر میکند. اگر این سرطان سریع تشخیص داده شود شانس درمان آن بالا است، اما تشخیص سریع آن قطعی نیست.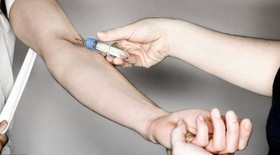 یک آزمایش خونی تجربی ممکن است بزودی بتواند امکان عود مجدد سرطان پستان را چندین ماه پیش از قابل تشخیص شدن تومورها توسط اسکن، پیشبینی کند. دستاورد جدید محققان موسسه تحقیقات سرطان در لندن با تشخیص دیانای سرطان موجود در جریان خون کار میکند. اگرچه این آزمایش خون هنوز برای استفاده عمومی در دسترس قرار نگرفته و احتمالا تا چند سال آینده نیز به بازار نیاید، محققان امیدوارند که این دستاورد بتواند به اصلاح درمانهای شخصی برای سرطان کمک کرده و حتی دانشمندان بتوانند راهی را برای درمان این بیماری پیدا کنند.
یک آزمایش خونی تجربی ممکن است بزودی بتواند امکان عود مجدد سرطان پستان را چندین ماه پیش از قابل تشخیص شدن تومورها توسط اسکن، پیشبینی کند. دستاورد جدید محققان موسسه تحقیقات سرطان در لندن با تشخیص دیانای سرطان موجود در جریان خون کار میکند. اگرچه این آزمایش خون هنوز برای استفاده عمومی در دسترس قرار نگرفته و احتمالا تا چند سال آینده نیز به بازار نیاید، محققان امیدوارند که این دستاورد بتواند به اصلاح درمانهای شخصی برای سرطان کمک کرده و حتی دانشمندان بتوانند راهی را برای درمان این بیماری پیدا کنند.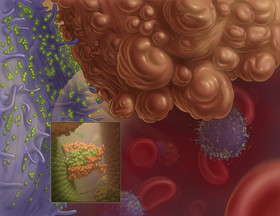 محققان ژاپنی با ادغام دانش زیستی و نانویی خود به کپسولهای جدیدی دست یافتند که علاوه بر تشخیص دقیق محل تومور، میتواند برای تحویل دارو نیز مورد استفاده قرار گیرد. پلیمرسامزها کپسولهایی توخالی، ترکیبی و نانویی هستند که پیش از این ظرفیت بالقوه آنها در حوزه تحویل دارو مورد بررسی قرار گرفته است. پیآیسیسامزها دسته جدیدی از پلیمرسامزها هستند و به تازگی در دانشگاه توکیو توسعه داده شدهاند. این مواد از اختلاط گروههای الکترولیتی متشکل از یونهای منفی و مثبت ساخته میشوند. پیآیسیسامزها میتوانند درون جریان خون به مدت زمان زیادی و بدون مشکل خاصی باقی بمانند. آنها همچنین میتوانند برای تحویل مواد انحلالپذیر در آب به اندامهای هدف (به عنوان مثال سایتهای تومور) مورد استفاده قرار گیرند.
محققان ژاپنی با ادغام دانش زیستی و نانویی خود به کپسولهای جدیدی دست یافتند که علاوه بر تشخیص دقیق محل تومور، میتواند برای تحویل دارو نیز مورد استفاده قرار گیرد. پلیمرسامزها کپسولهایی توخالی، ترکیبی و نانویی هستند که پیش از این ظرفیت بالقوه آنها در حوزه تحویل دارو مورد بررسی قرار گرفته است. پیآیسیسامزها دسته جدیدی از پلیمرسامزها هستند و به تازگی در دانشگاه توکیو توسعه داده شدهاند. این مواد از اختلاط گروههای الکترولیتی متشکل از یونهای منفی و مثبت ساخته میشوند. پیآیسیسامزها میتوانند درون جریان خون به مدت زمان زیادی و بدون مشکل خاصی باقی بمانند. آنها همچنین میتوانند برای تحویل مواد انحلالپذیر در آب به اندامهای هدف (به عنوان مثال سایتهای تومور) مورد استفاده قرار گیرند. محققان با قراردادن داروی شیمیدرمانی در یک نانوذره و پوششدهی آن با کیتوسان موفق به ارائه سیستم دارویی شدند که میتواند سلولهای شبه بنیادی سرطان را از بین ببرد. نتایج آزمونهای انجام شده روی حیوانات موفقیتآمیز بوده است. نتایج یافتههای اخیر محققان دانشگاه اوهایو نشان میدهد که نانوذرات بستهبندی شده به همراه داروهای شیمیدرمانی که دارای پوششی از جنس مواد الیگوساکارید است، میتواند برای درمان سرطان به کار رود. این بسته دارویی جدید قادر است سلولهای بنیادی سرطان را از بین ببرد.
محققان با قراردادن داروی شیمیدرمانی در یک نانوذره و پوششدهی آن با کیتوسان موفق به ارائه سیستم دارویی شدند که میتواند سلولهای شبه بنیادی سرطان را از بین ببرد. نتایج آزمونهای انجام شده روی حیوانات موفقیتآمیز بوده است. نتایج یافتههای اخیر محققان دانشگاه اوهایو نشان میدهد که نانوذرات بستهبندی شده به همراه داروهای شیمیدرمانی که دارای پوششی از جنس مواد الیگوساکارید است، میتواند برای درمان سرطان به کار رود. این بسته دارویی جدید قادر است سلولهای بنیادی سرطان را از بین ببرد. دانشمندان دانشگاه ایالتی فلوریدا معمای تقسیم سلولی را به شیوهای حل کردهاند که نویددهنده ارائه داروهای مبارزهکننده با سرطان در آینده باشد. کلید یافتههای محققان دپارتمان علوم زیستپزشکی در کالج پزشکی دانشگاه فلوریدا، پروتئینی به نام Treslin است. در حالی که شیمیدرمانی سلولهای عادی به سرعت تقسیمشونده را نیز هدف قرار میدهد، به نظر میرسد این پروتئین، سلولهای سرطانی را در تیررس خود قرار میدهد.
دانشمندان دانشگاه ایالتی فلوریدا معمای تقسیم سلولی را به شیوهای حل کردهاند که نویددهنده ارائه داروهای مبارزهکننده با سرطان در آینده باشد. کلید یافتههای محققان دپارتمان علوم زیستپزشکی در کالج پزشکی دانشگاه فلوریدا، پروتئینی به نام Treslin است. در حالی که شیمیدرمانی سلولهای عادی به سرعت تقسیمشونده را نیز هدف قرار میدهد، به نظر میرسد این پروتئین، سلولهای سرطانی را در تیررس خود قرار میدهد.

 دانشمندان انگلیسی مدعی هستند که یک واکسن جدید خواهد توانست از طیف گستردهای از سرطانهای دهانه رحم جلوگیری کند. واکسن جدید بطور چشمگیری به ارائه حفاظت بیشتر نسبت به واکسن کنونی موسوم به گارداسیل میپردازد؛ نمونه کنونی تنها میتواند از دو گونه سرطانزای ویروس پاپیلومای انسانی (HPV) جلوگیری کند. این واکسن در انگلستان برای کودکان 12-13 ساله و در آمریکا برای دختران 11-12 ساله عرضه میشود. واکسن جدید از انسان در برابر 9 سویه ویروس که هفت سویه آن عامل بسیاری از گونههای سرطان دهانه رحم است، محافظت میکند.
دانشمندان انگلیسی مدعی هستند که یک واکسن جدید خواهد توانست از طیف گستردهای از سرطانهای دهانه رحم جلوگیری کند. واکسن جدید بطور چشمگیری به ارائه حفاظت بیشتر نسبت به واکسن کنونی موسوم به گارداسیل میپردازد؛ نمونه کنونی تنها میتواند از دو گونه سرطانزای ویروس پاپیلومای انسانی (HPV) جلوگیری کند. این واکسن در انگلستان برای کودکان 12-13 ساله و در آمریکا برای دختران 11-12 ساله عرضه میشود. واکسن جدید از انسان در برابر 9 سویه ویروس که هفت سویه آن عامل بسیاری از گونههای سرطان دهانه رحم است، محافظت میکند. 

 کافئین موجود در قهوه، شکلات و چای خطر ابتلا به سرطان پوست را کاهش میدهد. پژوهشهای انجام شده در آمریکا نشان داد که کافئین موجود در قهوه، شکلات و چای، خطر ابتلا به سرطان پوست را کاهش میدهد. این ماده از سرعت رشد سلولهایی که به واسطهٔ اشعه ماورای بنفش خورشید آسیب دیدهاند، میکاهد.
کافئین موجود در قهوه، شکلات و چای خطر ابتلا به سرطان پوست را کاهش میدهد. پژوهشهای انجام شده در آمریکا نشان داد که کافئین موجود در قهوه، شکلات و چای، خطر ابتلا به سرطان پوست را کاهش میدهد. این ماده از سرعت رشد سلولهایی که به واسطهٔ اشعه ماورای بنفش خورشید آسیب دیدهاند، میکاهد.  پژوهشگران ایرلندی در تحقیقات خود دریافتند، زنانی که پیش از ابتلا به سرطان پستان بطور منظم از آسپیرین استفاده میکنند، نسبت به سایر زنان کمتر در معرض خطر مرگ در اثر این بیماری قرار دارند. محققان انجمن سرطان ایرلند، اثربخشی آسپیرین در پیشگیری از ابتلا به سرطان پستان و کاهش نرخ مرگ و میر در بین مبتلایان را مورد بررسی قرار دادند. نتایج بدست آمده نشان میدهد، مصرف منظم آسپیرین با جلوگیری از انتشار سرطان به غدد لنفاوی، به کاهش میزان مرگ و میر در بین مبتلایان به سرطان پستان کمک می کند.
پژوهشگران ایرلندی در تحقیقات خود دریافتند، زنانی که پیش از ابتلا به سرطان پستان بطور منظم از آسپیرین استفاده میکنند، نسبت به سایر زنان کمتر در معرض خطر مرگ در اثر این بیماری قرار دارند. محققان انجمن سرطان ایرلند، اثربخشی آسپیرین در پیشگیری از ابتلا به سرطان پستان و کاهش نرخ مرگ و میر در بین مبتلایان را مورد بررسی قرار دادند. نتایج بدست آمده نشان میدهد، مصرف منظم آسپیرین با جلوگیری از انتشار سرطان به غدد لنفاوی، به کاهش میزان مرگ و میر در بین مبتلایان به سرطان پستان کمک می کند.