تاثیر شیمی درمانی روی تومورها بیشتر میشود
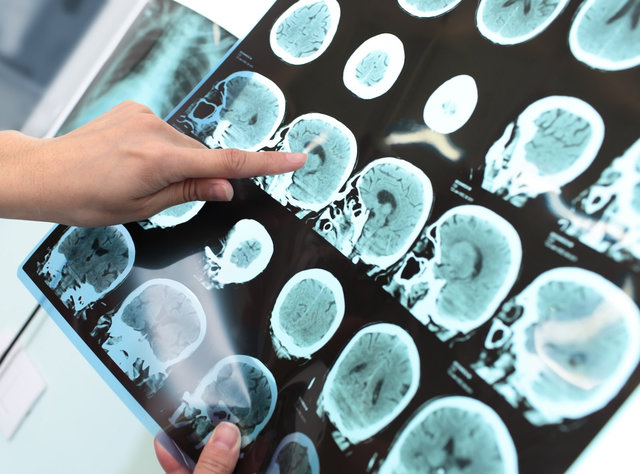 تیمی از دانشمندان فرانسوی به تازگی یه کاشت فراصوت را برای 15 نفر آزمایش کردهاند که به ارسال بهتر داروهای شیمیدرمانی به تومورهای مغزی کمک میکند. یکی از بزرگترین مشکلات در درمان سرطان مغز این است که تنها مقدار محدودی از داروهای شیمیدرمانی به داخل مغز راه مییابند زیرا رگهای خونی مغز شدیدا به سلولها پیوند خوردهاند تا از ورود مواد سمی و پاتوژنها جلوگیری کنند. اما این سد خونی همچنین از انتقال داروها به تومورها نیز جلوگیری میکند.
تیمی از دانشمندان فرانسوی به تازگی یه کاشت فراصوت را برای 15 نفر آزمایش کردهاند که به ارسال بهتر داروهای شیمیدرمانی به تومورهای مغزی کمک میکند. یکی از بزرگترین مشکلات در درمان سرطان مغز این است که تنها مقدار محدودی از داروهای شیمیدرمانی به داخل مغز راه مییابند زیرا رگهای خونی مغز شدیدا به سلولها پیوند خوردهاند تا از ورود مواد سمی و پاتوژنها جلوگیری کنند. اما این سد خونی همچنین از انتقال داروها به تومورها نیز جلوگیری میکند.
فناوری محققان شرکت CarThera در فرانسه شامل یک مبدل ۱۱.۵ میلیمتری موسوم به SonoCloud است که طی یک عمل جراحی درون حفرهای در جمجمه بیمار قرار میگیرد. در زمان تزریق داروی شیمیدرمانی، پزشکان میتوانند میکروحبابهایی را به درون جریان خون بیمار تزریق کنند که از میان سدخونی مغز عبور میکند. سپس دستگاه فعال شده و امواج فراصوت را برای دو دقیقه به مغز میتاباند تا میکروحبابها را فعال کند. این حبابهای در حال ارتعاش، سد خونی را برای حدود شش ساعت برای داروی شیمیدرمانی باز میکنند تا هفت برابر میزان داروی دریافتی در روشهای سنتی به تومور برسد. دانشمندان یک مطالعه آزمایشی را بر روی ۱۵ بیمار مبتلا به سرطان مغزی مرگبار گلیوبلاستوما انجام دادند و نتایج آنها نشان داد که این تکنیک بطور موفق به دارو اجازه عبور به سمت بافت مغزی را داد.
با وجود این نتایج، محققان باید کارآزمایی بالینی بزرگتری را انجام بدهند تا ثابت کنند که این روش باعث بروز عوارض جانبی نمیشود. برای مثال آنها باید نشان دهند که باکتری وارد مغز نشده و باعث بروز بیماری مرگبار مننژیت نمیشود. محققان قصد دارند در سال ۲۰۱۷ یک کارآزمایی بزرگتر را بر روی ۲۰۰ بیمار اروپایی و آمریکایی انجام دهند و در صورت موفق بودن نتایج، این کاشت ممکن است تا سال ۲۰۲۰ به بازار عرضه شود.

 محققان دانشگاه مینهسوتا با استفاده از نانوذرات به عنوان حامل، عوارض ماده شیمیایی TNF-a را که میتواند رگهای خونی اطراف تومور را از بین ببرد، به حداقل رساندهاند. در سالهای اخیر محققان موفق شدند روشی برای از بین بردن رگهای پیرامون تومورها پیدا کنند با این کار میتوان تومورها را از بین برد. برای این کار از مواد شیمیایی مختلف استفاده میشود. یکی از این ترکیبات کاچکسین یا TNF-a است که نتایج بسیار خوبی داده است، مشکل این ماده سمی بودن آن است که میتواند عوارض جانبی داشته باشد. برای کاهش سمیت این ماده میتوان از نانوذرات طلا استفاده کرد. این نانوذرات میتوانند به عنوان حامل این ماده دارو را در محل مورد نظر رهاسازی کنند. این فرآیند فاز اول تست بالینی را پشت سر گذاشته است.
محققان دانشگاه مینهسوتا با استفاده از نانوذرات به عنوان حامل، عوارض ماده شیمیایی TNF-a را که میتواند رگهای خونی اطراف تومور را از بین ببرد، به حداقل رساندهاند. در سالهای اخیر محققان موفق شدند روشی برای از بین بردن رگهای پیرامون تومورها پیدا کنند با این کار میتوان تومورها را از بین برد. برای این کار از مواد شیمیایی مختلف استفاده میشود. یکی از این ترکیبات کاچکسین یا TNF-a است که نتایج بسیار خوبی داده است، مشکل این ماده سمی بودن آن است که میتواند عوارض جانبی داشته باشد. برای کاهش سمیت این ماده میتوان از نانوذرات طلا استفاده کرد. این نانوذرات میتوانند به عنوان حامل این ماده دارو را در محل مورد نظر رهاسازی کنند. این فرآیند فاز اول تست بالینی را پشت سر گذاشته است. 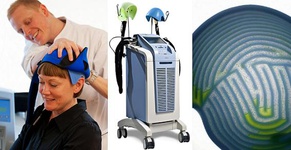 یک سیستم خنککننده جمجمه سر در بخشهایی از لندن مورد استفاده قرار گرفته که به بیماران شیمیدرمانی برای جلوگیری از ریزش مو در جریان این درمان کمک میکند. سیستم DigniCap توسط بنیاد مراقبت بهداشتی امپریال کالج لندن برای استفاده در واحدهای شیمیدرمای روزانه در بیمارستانهای چرینگ کراس و همراسمیت استفاده شده است. در این درمان، بیماران یک کلاه خاص را بر روی سر میگذارند که جمجمه آنها را خنک کرده و از ریزش موها جلوگیری میکند. این سیستم بطور مکرر دما را بررسی میکند تا از کاربرد مداوم درمان خنککننده اطمینان حاصل کند. این کلاهها به شکلی طراحی شدهاند که گوشها در کل این فرآیند بدون پوشش باقی میمانند. به گفته سخنگوی این شرکت، در کارآزماییهای بالینی هشت تن از 10 بیمار در اروپا و آسیا که از این سیستم در طول شیمی درمانی استفاده کردهاند، موهای خود را از دست ندادند. به گفته این سخنگو، کارآزماییهای بیشتر در مراکز پزشکی پیشتاز جهان ثابت کرده که این سیستم یک جایگزین ماندگار برای زنان و مردان از قومیتهای مختلف است.
یک سیستم خنککننده جمجمه سر در بخشهایی از لندن مورد استفاده قرار گرفته که به بیماران شیمیدرمانی برای جلوگیری از ریزش مو در جریان این درمان کمک میکند. سیستم DigniCap توسط بنیاد مراقبت بهداشتی امپریال کالج لندن برای استفاده در واحدهای شیمیدرمای روزانه در بیمارستانهای چرینگ کراس و همراسمیت استفاده شده است. در این درمان، بیماران یک کلاه خاص را بر روی سر میگذارند که جمجمه آنها را خنک کرده و از ریزش موها جلوگیری میکند. این سیستم بطور مکرر دما را بررسی میکند تا از کاربرد مداوم درمان خنککننده اطمینان حاصل کند. این کلاهها به شکلی طراحی شدهاند که گوشها در کل این فرآیند بدون پوشش باقی میمانند. به گفته سخنگوی این شرکت، در کارآزماییهای بالینی هشت تن از 10 بیمار در اروپا و آسیا که از این سیستم در طول شیمی درمانی استفاده کردهاند، موهای خود را از دست ندادند. به گفته این سخنگو، کارآزماییهای بیشتر در مراکز پزشکی پیشتاز جهان ثابت کرده که این سیستم یک جایگزین ماندگار برای زنان و مردان از قومیتهای مختلف است.
 دانشمندان دانشگاه کالیفرنیا در ساندیگو در مراحل ابتدایی شیوهای هستند که از حبابهای درون حباب برای انتقال داروهای شیمیدرمانی استفاده کرده و میتواند در آینده به کاهش عوارض جانبی چشمگیر این شیوه درمانی منجر شود. عوارض جانبی رایجترین درمانهای شیمی درمانی از چگونگی عملکرد آنها نشات میگیرند. سلولها در زمان تکثیر خارج از کنترل سرطانی میشوند از این رو داروهای شیمیدرمانی تمام سلولهای حاضر در فرآیند تکثیر را هدف قرار داده و میکشند.
دانشمندان دانشگاه کالیفرنیا در ساندیگو در مراحل ابتدایی شیوهای هستند که از حبابهای درون حباب برای انتقال داروهای شیمیدرمانی استفاده کرده و میتواند در آینده به کاهش عوارض جانبی چشمگیر این شیوه درمانی منجر شود. عوارض جانبی رایجترین درمانهای شیمی درمانی از چگونگی عملکرد آنها نشات میگیرند. سلولها در زمان تکثیر خارج از کنترل سرطانی میشوند از این رو داروهای شیمیدرمانی تمام سلولهای حاضر در فرآیند تکثیر را هدف قرار داده و میکشند.  شيمي درماني در دوران بارداري بيخطر است و خطري براي جنين ندارد. محققان آلماني دريافتند زناني که در دوران بارداري براي درمان سرطان شيمي درماني ميکنند، در معرض افزايش خطر تولد کودکان ناقص و يا ديگر مسائل مربوط به سلامتي قرار ندارند. محققان بر اساس نتايج اين تحقيق ميگويند: مادران نبايد به هر روشي اقدام به سقط جنين کنند، درمان را به تاخير انداخته و يا از داروهايي که قدرت کمتري دارند، استفاده کنند؛ زيرا شواهد کمي وجود دارد که کودک تحت تاثير شيمي درماني قرار بگيرد.
شيمي درماني در دوران بارداري بيخطر است و خطري براي جنين ندارد. محققان آلماني دريافتند زناني که در دوران بارداري براي درمان سرطان شيمي درماني ميکنند، در معرض افزايش خطر تولد کودکان ناقص و يا ديگر مسائل مربوط به سلامتي قرار ندارند. محققان بر اساس نتايج اين تحقيق ميگويند: مادران نبايد به هر روشي اقدام به سقط جنين کنند، درمان را به تاخير انداخته و يا از داروهايي که قدرت کمتري دارند، استفاده کنند؛ زيرا شواهد کمي وجود دارد که کودک تحت تاثير شيمي درماني قرار بگيرد.  دانشمندان در جديدترين تحقيقات خود شيميدرماني را عامل رشد تومورهاي سرطاني اعلام كردند. از زماني كه شيميدرماني به حوزه پزشكي غرب وارد شد، پزشكان و دانشمندان همواره در تلاش براي پاسخ به اين پرسش بودهاند كه چرا شيميدرماني در مراحل نخست كارساز است اما در ادامه سلولهاي تومور سرطاني حتي بدخيمتر از گذشته بازميگردند؟ به نظر ميرسد كه اين رويكرد درماني به سلولهاي سالم آسيب ميرساند و موجب ميشود كه آنها نوعي پروتئين را ترشح كنند كه رشد تومورهاي سرطاني را تسريع ميبخشد.
دانشمندان در جديدترين تحقيقات خود شيميدرماني را عامل رشد تومورهاي سرطاني اعلام كردند. از زماني كه شيميدرماني به حوزه پزشكي غرب وارد شد، پزشكان و دانشمندان همواره در تلاش براي پاسخ به اين پرسش بودهاند كه چرا شيميدرماني در مراحل نخست كارساز است اما در ادامه سلولهاي تومور سرطاني حتي بدخيمتر از گذشته بازميگردند؟ به نظر ميرسد كه اين رويكرد درماني به سلولهاي سالم آسيب ميرساند و موجب ميشود كه آنها نوعي پروتئين را ترشح كنند كه رشد تومورهاي سرطاني را تسريع ميبخشد. نتايج تحقيقات اوليه دانشمندان در آمريكا نشان ميدهد، استفاده از «سپر سلولهاي بنيادي» ميتواند از بدن در مقابل اثرات مخرب شيمي درماني محافظت كند. محققان در يك رويكرد كاملاً نوين از سلولهاي بنيادي ژنتيكي اصلاح شده براي حفاظت از مغز استخوان استفاده كردند. دكتر «جنيفر آداير» در تشريح اين روش ميگويد: اين درمان مشابه شليك به هر دو سلول سرطاني و سلولهاي مغز استخوان است، اما در اين حالت سلول هاي مغز استخوان مجهز به سپرهاي سلول بنيادي هستند. محققان در اين پژوهش تلاش كردند از مغز استخوان سه بيمار مبتلا به نوعي از سرطان مغز به نام «گلیوبلاستوما» در برابر آثار سوء شيمي درماني محفاظت كنند.
نتايج تحقيقات اوليه دانشمندان در آمريكا نشان ميدهد، استفاده از «سپر سلولهاي بنيادي» ميتواند از بدن در مقابل اثرات مخرب شيمي درماني محافظت كند. محققان در يك رويكرد كاملاً نوين از سلولهاي بنيادي ژنتيكي اصلاح شده براي حفاظت از مغز استخوان استفاده كردند. دكتر «جنيفر آداير» در تشريح اين روش ميگويد: اين درمان مشابه شليك به هر دو سلول سرطاني و سلولهاي مغز استخوان است، اما در اين حالت سلول هاي مغز استخوان مجهز به سپرهاي سلول بنيادي هستند. محققان در اين پژوهش تلاش كردند از مغز استخوان سه بيمار مبتلا به نوعي از سرطان مغز به نام «گلیوبلاستوما» در برابر آثار سوء شيمي درماني محفاظت كنند.