..:::: مصرف گوشت قرمز خطر ابتلا به سرطان سینه در زنان را افزایش می دهد ::::..
مطالعه محققان آمریکایی نشان می دهد،خطر ابتلا به سرطان سینه در زنانی که بطور مرتب گوشت قرمز مصرف می کنند، بیشتر است. محققان آمریکایی در این مطالعه 88 هزار و 803 زن 26 تا 45 ساله را برای مدت 20 سال از سال 1991 تا 2011 مورد ارزیابی قرار دادند. این مطالعه نشان می دهد، خطر ابتلا به سرطان سینه در زنانی که روزی یک وعده و نیم گوشت قرمز مصرف می کردند در مقایسه با افرادی که اصلا و یا به مقدار بسیار کم گوشت قرمز استفاده می کردند 22 درصد بیشتر بود.
در این مطالعه یک وعده گوشت قرمز 55 گرم در نظر گرفته شده است که تقریبا برابر با یک تکه کوچک استیک یا چند برش ژامبون است. محققان همچنین متوجه شدند که مصرف هر وعده اضافی گوشت قرمز در روز خطر ابتلای زنان به سرطان سینه را 13 درصد افزایش می دهد. به گفته محققان، مصرف گوشت مرغ، ماهی، حبوبات و سبزیجات به جای گوشت قرمز در یک وعده غذایی می تواند خطر ابتلا به سرطان سینه را در زنان 25 درصد کاهش دهد.
کارشناسان معتقدند که چربی اشباع شده موجود در گوشت قرمز موجب افزایش سطح کلسترول و به نوبه خود موجب تولید هورمون استروژن می شود که با ابتلا به سرطان سینه ارتباط دارد. دکتر مریم فروید (Maryam Farvid) از دانشکده بهداشت عمومی هاروارد در بوستون که ریاست این مطالعه را بر عهده داشت، می گوید: این مطالعه نشان داد که مصرف گوشت قرمز در اوایل بلوغ عامل خطر سازی برای ابتلا به سرطان سینه است. سرطان سینه شایع ترین بیماری در زنان به شمار می رود و مطالعات نشان می دهد که شیوه زندگی، چاقی، سیگار کشیدن و ورزش نکردن خطر ابتلا به سرطان سینه را افزایش می دهد. این مطالعه در مجله British Medical Journal چاپ شده است.
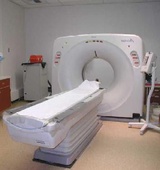 محققان آمریکایی بیمارستان Beaumont دریافتند که استفاده از سی تی اسکنهایی با منبع مضاعف (DSCT) خطر ابتلا به سرطان ناشی از مواجهه با پرتو درمانی را کاهش میدهد. با استفاه از DSCT، قرار گرفتن در برابر اشعههای پرتو درمانی در مقایسه با سی تی اسکنهای معمول تا 61 درصد کاهش مییابد و این در حالی است که کیفیت عکسهای به دست آمده از بیماران مبتلا به عروق کرونری، آمبولی ریه و یا بیماریهای آئورت با سی تی اسکنهای معمول تفاوت چشمگیری ندارد.
محققان آمریکایی بیمارستان Beaumont دریافتند که استفاده از سی تی اسکنهایی با منبع مضاعف (DSCT) خطر ابتلا به سرطان ناشی از مواجهه با پرتو درمانی را کاهش میدهد. با استفاه از DSCT، قرار گرفتن در برابر اشعههای پرتو درمانی در مقایسه با سی تی اسکنهای معمول تا 61 درصد کاهش مییابد و این در حالی است که کیفیت عکسهای به دست آمده از بیماران مبتلا به عروق کرونری، آمبولی ریه و یا بیماریهای آئورت با سی تی اسکنهای معمول تفاوت چشمگیری ندارد. 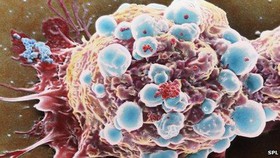 محققان اسپانیایی موفق به ساخت تراشهای شدند که قادر به شناسایی سلولهای سرطانی در مراحل اولیه است. در این تراشه از نانوذرات طلای حاوی آنتیبادی ویژهی پروتئینهای تولید شده توسط سلول سرطانی استفاده شدهاست. در حال حاضر تشخیص بیماری سرطان زمانی صورت میگیرد که تومور به قدری افزایش حجم داده که میلیونها سلول در آن رشد کرده و در حال وارد شدن به مرحلهی پیشرفتهی بیماری است. از نظر پزشکی، شناسایی سرطان را در مراحل اولیه و در حالی که هنوز چند سلول اولیه سرطانی تشکیل شده باشد اهمیت بسیاری دارد. با این کار میتوان از پیشرفت بیماری در مراحل بعدی جلوگیری کرد.
محققان اسپانیایی موفق به ساخت تراشهای شدند که قادر به شناسایی سلولهای سرطانی در مراحل اولیه است. در این تراشه از نانوذرات طلای حاوی آنتیبادی ویژهی پروتئینهای تولید شده توسط سلول سرطانی استفاده شدهاست. در حال حاضر تشخیص بیماری سرطان زمانی صورت میگیرد که تومور به قدری افزایش حجم داده که میلیونها سلول در آن رشد کرده و در حال وارد شدن به مرحلهی پیشرفتهی بیماری است. از نظر پزشکی، شناسایی سرطان را در مراحل اولیه و در حالی که هنوز چند سلول اولیه سرطانی تشکیل شده باشد اهمیت بسیاری دارد. با این کار میتوان از پیشرفت بیماری در مراحل بعدی جلوگیری کرد. 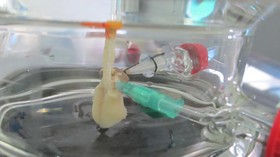
 محققان دانشگاه میشیگان، تنظیمگر مهمی را برای عملیات "اتوفاژی" کشف کردهاند؛ اتوفاژی فرآیند بازیافت سلولی است که در بسیاری از بیماریها یافت میشود. طی اوتوفاژی تعداد و اندازه محمولهای مورد استفاد سلول برای دفع زواید، موسوم به autophagosome کیفیت و کارآمدی این چرخه بازیافتی را تعیین میکند. محققان آمریکایی دریافتند مولکولی موسوم به Atg9 میتواند این تعداد autophagosome را در مخمر تنظیم کند. به گفته کلیونسکی سرپرست این پژوهش، افزایش یا کاهش اندازه و کیفیت autophagosome هدف اصلی برای خدمات درمانی محسوب میشود که تا پیش از این تحقیق، درک چگونگی تنظیم اندازه و شمار آن در سطح پایینی قرار داشت؛ در واقع کنترل Atg9 راهی را برای تنظیم اتوفاژی در اختیار میگذارد تا بتوان از آن در مقابله با بیماریها استفاده کرد.
محققان دانشگاه میشیگان، تنظیمگر مهمی را برای عملیات "اتوفاژی" کشف کردهاند؛ اتوفاژی فرآیند بازیافت سلولی است که در بسیاری از بیماریها یافت میشود. طی اوتوفاژی تعداد و اندازه محمولهای مورد استفاد سلول برای دفع زواید، موسوم به autophagosome کیفیت و کارآمدی این چرخه بازیافتی را تعیین میکند. محققان آمریکایی دریافتند مولکولی موسوم به Atg9 میتواند این تعداد autophagosome را در مخمر تنظیم کند. به گفته کلیونسکی سرپرست این پژوهش، افزایش یا کاهش اندازه و کیفیت autophagosome هدف اصلی برای خدمات درمانی محسوب میشود که تا پیش از این تحقیق، درک چگونگی تنظیم اندازه و شمار آن در سطح پایینی قرار داشت؛ در واقع کنترل Atg9 راهی را برای تنظیم اتوفاژی در اختیار میگذارد تا بتوان از آن در مقابله با بیماریها استفاده کرد.  پژوهشگران بریتانیایی اظهار کردند: استفاده بیش از اندازه از دهانشویهها باعث افزایش خطر ابتلا به سرطان دهان و گلو میشود. محصولات بهداشتی دهان و دندان خاصیت ضدباکتریایی دارند و باعث پیشگیری از ایجاد پلاک، ورم لثه و پوسیدگی دندان میشوند. به گفته دکتر دیوید کنوی، مدیر گروه تحقیقاتی دانشکده دندانپزشکی گلاسگو، کسانی که برای ایجاد حس تازگی در دهان به دفعات مکرر در طول روز از دهانشویهها استفاده میکنند، در معرض خطر ابتلا به سرطان هستند.
پژوهشگران بریتانیایی اظهار کردند: استفاده بیش از اندازه از دهانشویهها باعث افزایش خطر ابتلا به سرطان دهان و گلو میشود. محصولات بهداشتی دهان و دندان خاصیت ضدباکتریایی دارند و باعث پیشگیری از ایجاد پلاک، ورم لثه و پوسیدگی دندان میشوند. به گفته دکتر دیوید کنوی، مدیر گروه تحقیقاتی دانشکده دندانپزشکی گلاسگو، کسانی که برای ایجاد حس تازگی در دهان به دفعات مکرر در طول روز از دهانشویهها استفاده میکنند، در معرض خطر ابتلا به سرطان هستند.  محققان دانشگاه ویرجینیا نوع خاصی از سلول ایمنی را در مغز استخوان موش کشف کردهاند که مسؤول نوع تهاجمی سرطان خون است. سرطان متهاجم خون، بسیار مقاوم و اصطلاحا زیرک است، چرا که اگر سلولهای لوسمی (سرطان خون) در محیط آزمایشگاه کشت داده شوند، در کمترین شرایط مورد نیاز نیز میتوانند به بقای خود ادامه دهند. به تعبیر محققان، از آنجا که این سلولها از حیث سیستم رشد و بقا بسیار متهاجم هستند، به گونهای خود را «جاودانه» نیز کردهاند.
محققان دانشگاه ویرجینیا نوع خاصی از سلول ایمنی را در مغز استخوان موش کشف کردهاند که مسؤول نوع تهاجمی سرطان خون است. سرطان متهاجم خون، بسیار مقاوم و اصطلاحا زیرک است، چرا که اگر سلولهای لوسمی (سرطان خون) در محیط آزمایشگاه کشت داده شوند، در کمترین شرایط مورد نیاز نیز میتوانند به بقای خود ادامه دهند. به تعبیر محققان، از آنجا که این سلولها از حیث سیستم رشد و بقا بسیار متهاجم هستند، به گونهای خود را «جاودانه» نیز کردهاند.  محققان دانشگاه مسی نیوزلند طی یک بررسی نشان دادند داروی آزمایشی «Dinaciclib» میتواند تاثیر سودمندی در درمان میلوم متعدد خاصی و لوسمی میلوییدی، دو سرطان شایع خون که معمولا در مغز استخوانها وجود دارند، بر جای بگذارد. داروی "Dinaciclib" توانسته است مکانیزم بقای سلولی موسوم به «پاسخ پروتئین واتابیده (UPR)» را مختل کند؛ بدون «UPR» سلولهای میلوم متعدد و لوسمی میلوییدی قادر به مبارزه با آسیبهای ناشی از عوامل ضد سرطانی نبودند. محققان میگویند گرچه این دارو توانسته در فاز یک و دو آزمایشات بالینی موفقیت از خود نشان دهد، اما هنوز مکانیزم فعالیت آنتی تومور این دارو به طور کامل مشخص نشده است.
محققان دانشگاه مسی نیوزلند طی یک بررسی نشان دادند داروی آزمایشی «Dinaciclib» میتواند تاثیر سودمندی در درمان میلوم متعدد خاصی و لوسمی میلوییدی، دو سرطان شایع خون که معمولا در مغز استخوانها وجود دارند، بر جای بگذارد. داروی "Dinaciclib" توانسته است مکانیزم بقای سلولی موسوم به «پاسخ پروتئین واتابیده (UPR)» را مختل کند؛ بدون «UPR» سلولهای میلوم متعدد و لوسمی میلوییدی قادر به مبارزه با آسیبهای ناشی از عوامل ضد سرطانی نبودند. محققان میگویند گرچه این دارو توانسته در فاز یک و دو آزمایشات بالینی موفقیت از خود نشان دهد، اما هنوز مکانیزم فعالیت آنتی تومور این دارو به طور کامل مشخص نشده است.  محققان دانشگاه جورجیا در آمریکا به روش جدیدی برای خارج کردن سلول های سرطانی از مغز با استفاده از میله های کوچک دست یافتند. این سیستم با استفاده از نانو الیافی سلول های تومور را از مغز خارج می کند. محققان می گویند دستیابی به این روش جدید می تواند زندگی افراد مبتلا به سرطان های غیر قابل جراحی را به زندگی افراد دیابتی یا افراد مبتلا به فشار خون بالا شبیه کند.
محققان دانشگاه جورجیا در آمریکا به روش جدیدی برای خارج کردن سلول های سرطانی از مغز با استفاده از میله های کوچک دست یافتند. این سیستم با استفاده از نانو الیافی سلول های تومور را از مغز خارج می کند. محققان می گویند دستیابی به این روش جدید می تواند زندگی افراد مبتلا به سرطان های غیر قابل جراحی را به زندگی افراد دیابتی یا افراد مبتلا به فشار خون بالا شبیه کند. دانشمندان «آزمایشگاه رشد و زیستشناسی پستانداران» دانشگاه راکفلر تکنیک جدیدی را طراحی کردهاند که بر موانع موجود در شناسایی ژنهای سرکوبگر سرطان غلبه میکند. با استفاده از تکنیک جدید، آنها توانستهاند هفت ژن جدید سرکوبگر تومور سرطانهای سر و گردن را کشف کنند که نقش آنها تاکنون ناشناخته بود. رویکرد ابداعی آنها زمان و منابع کمتری را در مقایسه با شیوه سنتی تعیینکننده نقش ژن میطلبد.
دانشمندان «آزمایشگاه رشد و زیستشناسی پستانداران» دانشگاه راکفلر تکنیک جدیدی را طراحی کردهاند که بر موانع موجود در شناسایی ژنهای سرکوبگر سرطان غلبه میکند. با استفاده از تکنیک جدید، آنها توانستهاند هفت ژن جدید سرکوبگر تومور سرطانهای سر و گردن را کشف کنند که نقش آنها تاکنون ناشناخته بود. رویکرد ابداعی آنها زمان و منابع کمتری را در مقایسه با شیوه سنتی تعیینکننده نقش ژن میطلبد.  محققان دانشگاه و انستیتو تکنولوژی رویال ملبورن موفق به تولید ترکیب امیدبخشی برای درمان سرطان شدند. در این تحقیق محصول دریایی طبیعی و شگفتانگیزی به نام «Salicylihalamid» تولید شده که از اسفنجی موسوم به «Halicona» مشتق شده است؛ این نوع اسفنج در خلیج فارس نیز موجود است. «Salicylihalamide A» یک سیتوتوکسیک یا به عبارتی سمی است که سلولها را از بین میبرد و نوعی سد دفاعی را برای اسفنج دریایی فراهم میآورد.
محققان دانشگاه و انستیتو تکنولوژی رویال ملبورن موفق به تولید ترکیب امیدبخشی برای درمان سرطان شدند. در این تحقیق محصول دریایی طبیعی و شگفتانگیزی به نام «Salicylihalamid» تولید شده که از اسفنجی موسوم به «Halicona» مشتق شده است؛ این نوع اسفنج در خلیج فارس نیز موجود است. «Salicylihalamide A» یک سیتوتوکسیک یا به عبارتی سمی است که سلولها را از بین میبرد و نوعی سد دفاعی را برای اسفنج دریایی فراهم میآورد.