..:::: دستگاه تشخیص سرطان ریه در مرحله آزمون بالینی ::::..

محققان دانشگاه لیسستر با همکاری بیمارستان گلینفیلد اقدام به انجام آزمون بالینی روی دستگاه تشخیص سرطان ریه با استفاده از آزمون تنفسی کرده است؛ محققان این پروژه امیدوارند که با استفاده از برنامه تشخیص علائم سرطان ریه (LuCID) بتوانند روشی غیرتهاجمی برای تشخیص سرطان ارائه کنند. شرکت Owlstone Nanotech Ltd آنالیزهای اقتصادی این پروژه را انجام میدهد. نتایج بررسیهای این شرکت نشان میدهد که شناسایی زودهنگام سرطان ریه از 14.5 درصد به 25 درصد در سال 2020 خواهد رسید. پیشبینی میشود که با سرمایهگذاری 250 میلیون پوندی وزارت بهداشت انگلستان، این تشخیص زودهنگام بتواند جان 10 هزار نفر را نجات دهد.
دستگاه تشخیص سرطان ریه با استفاده از غلظتهای بسیار کم مواد آلی فرار موجود در بازدم افراد میتواند فرآیند شناسایی زودهنگام سرطان ریه را انجام دهد. این فناوری، ابزاری ارزان و سریع برای شناسایی سرطان ریه است که میتواند جایگزینی مناسب برای فناوریهای فعلی باشد. این دستگاه برخلاف روشهایی نظیر تصویربرداری اشعه ایکس، بیخطر است.
شرکت Owlstone Nanotech Ltd با حمایت مالی یک میلیون پوندی، پیشگامی تحقیقات کسب و کار کوچک در حوزه درمان (SBRI) و همچنین با کمک تیم توسعه کسب و کار و کارآفرینی دانشگاه لیسستر، فاز دوم این آزمون بالینی را به زودی آغاز خواهد کرد. هدف از این آزمون، بررسی حسگرهای این دستگاه (کروماتوگرافی گازی- طیفسنجی حرکت یونی) در بیماران سرطانی است. در صورتی که این آزمون با موفقیت به پایان برسد، مسیر ورود این دستگاه به بیمارستانها هموار خواهد شد. یکی از بنیانگذاران این شرکت میگوید: اگر شما بتوانید با تغییر چیزی موفق به شناسایی زودهنگام سرطان ریه شوید، آنگاه با روشهای درمانی فعلی میتوان جان بیمار را نجات داد. احتمالا بتوان از این فناوری برای شناسایی سرطان پستان نیز استفاده کرد. ما لحظهای آرام نخواهیم گرفت تا روزی که بتوانیم این فناوری را به بیمارستانها وارد کنیم.
پیشبینی میشود که نتایج این آزمون بالینی در ابتدای سال 2016 کامل شود. سرطان ریه یکی از بیماریهایی است که نرخ زنده ماندن در آن بسیار پایین است و تشخیص زودهنگام بیماری میتواند تأثیر زیادی در افزایش نرخ زنده ماندن داشته باشد. در حال حاضر از سیتی اسکن و رادیولوژی برای شناسایی این بیماری استفاده میشود که بسیار پرهزینه است و خطراتی را نیز برای بیمار به همراه دارد.
 نتایج یک مطالعه که به تازگی انجام شده است نشان می دهد که قرار گرفتن در معرض سیلیکا خطر ابتلا به سرطان ریه را افزایش می دهد. سیلیکا یک ماده معدنی است که در موادی مانند شن، سنگ، بتون و آجر یافت می شود که این مواد در ساخت و سازها، حفاری و تولید صنعتی مورد استفاده قرار می گیرند. محققان انجمن سرطان آمریکا و دانشگاه ˈاموریˈ در آتلانتا گفتند که سرطان ریه علت عمده مرگ و میر میان زنان و مردان است و دود سیگار بزرگترین عامل خطر ساز ابتلا به این سرطان است. با این حال، قرار گرفتن در معرض رادون، آزبست، سیلیس و آلودگی هوا نیز خطر ابتلا به سرطان ریه را افزایش می دهد.
نتایج یک مطالعه که به تازگی انجام شده است نشان می دهد که قرار گرفتن در معرض سیلیکا خطر ابتلا به سرطان ریه را افزایش می دهد. سیلیکا یک ماده معدنی است که در موادی مانند شن، سنگ، بتون و آجر یافت می شود که این مواد در ساخت و سازها، حفاری و تولید صنعتی مورد استفاده قرار می گیرند. محققان انجمن سرطان آمریکا و دانشگاه ˈاموریˈ در آتلانتا گفتند که سرطان ریه علت عمده مرگ و میر میان زنان و مردان است و دود سیگار بزرگترین عامل خطر ساز ابتلا به این سرطان است. با این حال، قرار گرفتن در معرض رادون، آزبست، سیلیس و آلودگی هوا نیز خطر ابتلا به سرطان ریه را افزایش می دهد.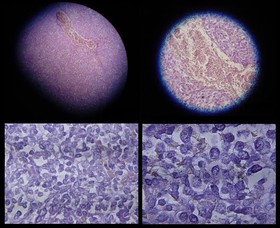 پژوهشگران مایوکلینیک ثابت کردهاند که یک جفت پروتئین اختصاصی برای شناسایی سرطانهای ریهی مرتبط با سیگار بعنوان نشانگر زیستی موفق پیشآگهی دهنده عمل میکند. این پروتئین که ASCL1 نام دارد، با افزایش تجلی انکوژن RET که یک ژن مخصوص ایجادکنندهی سرطان موسوم به RET بوده، همراه است، به گفته محققان این یافته شگفتیآور است. این ژن، نشانگر زیستی آدنوکارسینومهای تهاجمی است. آدنوکارسینوم از جمله یاختههای سرطانی با رشد سریع هستند که در افراد سیگاری یافت میشوند. محققان این پژوهش میگویند: میدانیم که ASCL1 رشد یاختهی نوروآندوکرین را کنترل میکند و پیش از این با تنظیم تیروئید و رشد سرطان ریهی سلول کوچک در ارتباط بوده است، ولی ارتباطی با سرطان ریهی مرتبط با سیگار نداشته است.
پژوهشگران مایوکلینیک ثابت کردهاند که یک جفت پروتئین اختصاصی برای شناسایی سرطانهای ریهی مرتبط با سیگار بعنوان نشانگر زیستی موفق پیشآگهی دهنده عمل میکند. این پروتئین که ASCL1 نام دارد، با افزایش تجلی انکوژن RET که یک ژن مخصوص ایجادکنندهی سرطان موسوم به RET بوده، همراه است، به گفته محققان این یافته شگفتیآور است. این ژن، نشانگر زیستی آدنوکارسینومهای تهاجمی است. آدنوکارسینوم از جمله یاختههای سرطانی با رشد سریع هستند که در افراد سیگاری یافت میشوند. محققان این پژوهش میگویند: میدانیم که ASCL1 رشد یاختهی نوروآندوکرین را کنترل میکند و پیش از این با تنظیم تیروئید و رشد سرطان ریهی سلول کوچک در ارتباط بوده است، ولی ارتباطی با سرطان ریهی مرتبط با سیگار نداشته است.  پژوهشگران دانشگاه سيدني استراليا موفق به ساخت نانوذراتي شدند که احتمالا ميتواند در درمان سرطان ريه مفيد باشد. اين گروه تحقيقاتي در تازهترين مطالعات خود نانوذراتي توليد کردهاند که به تومورها حمله ميکند و در عين حال آسيبي به سلولهاي سالم نميرساند؛ بنابراين در درمان سرطان کمترين اثرات جانبي را خواهد داشت. درون اين نانوذرات از چربيهايي پر شده است که در صورت قرار گرفتن در ميدان مغناطيسي فعال ميشوند.
پژوهشگران دانشگاه سيدني استراليا موفق به ساخت نانوذراتي شدند که احتمالا ميتواند در درمان سرطان ريه مفيد باشد. اين گروه تحقيقاتي در تازهترين مطالعات خود نانوذراتي توليد کردهاند که به تومورها حمله ميکند و در عين حال آسيبي به سلولهاي سالم نميرساند؛ بنابراين در درمان سرطان کمترين اثرات جانبي را خواهد داشت. درون اين نانوذرات از چربيهايي پر شده است که در صورت قرار گرفتن در ميدان مغناطيسي فعال ميشوند.  محققان موفق شدند ژن عامل بروز سرطان ریه را شناسایی كنند. به گزارش شینهوا، سلول های بنیادی سرطان یا سلول های آغازگر تومور، عامل رشد سرطان هستند. اكنون دانشمندان نشانگری موسوم به CD166 شناسایی كرده اند كه به تشخیص این سلول ها كمك می كند. پژوهشگران زیست شناسی سلول بنیادی سرطان در موسسه ژنوم سنگاپور، ژنهای متعددی را یافتند كه برای رشد سلول های سرطانی مهم و ضروری هستند. آنها موارد غیرطبیعی یافتند كه میزان آنزیم متابولیك موسوم به گلیسین دكربوكسیلاز به طور چشمگیری در آنها افزایش می یابد و این امر موجب تغییراتی در رفتار سلول و موجب سرطانی شدن آن می شود. این آنزیم، آنزیمی است كه به طور طبیعی در سلول در مقادیر اندك وجود دارد. نتایج این تحقیقات در نشریه سلول منتشر شده است. این كشف می تواند گام مهمی به سوی شیوه های درمانی جدید برای سرطان باشد.
محققان موفق شدند ژن عامل بروز سرطان ریه را شناسایی كنند. به گزارش شینهوا، سلول های بنیادی سرطان یا سلول های آغازگر تومور، عامل رشد سرطان هستند. اكنون دانشمندان نشانگری موسوم به CD166 شناسایی كرده اند كه به تشخیص این سلول ها كمك می كند. پژوهشگران زیست شناسی سلول بنیادی سرطان در موسسه ژنوم سنگاپور، ژنهای متعددی را یافتند كه برای رشد سلول های سرطانی مهم و ضروری هستند. آنها موارد غیرطبیعی یافتند كه میزان آنزیم متابولیك موسوم به گلیسین دكربوكسیلاز به طور چشمگیری در آنها افزایش می یابد و این امر موجب تغییراتی در رفتار سلول و موجب سرطانی شدن آن می شود. این آنزیم، آنزیمی است كه به طور طبیعی در سلول در مقادیر اندك وجود دارد. نتایج این تحقیقات در نشریه سلول منتشر شده است. این كشف می تواند گام مهمی به سوی شیوه های درمانی جدید برای سرطان باشد.  دانشمندان زیست حسگرهایی ساخته اند كه نشانگرهای سرطان ریه را در بازدم بیمار شناسایی می كنند. به گزارش دیلی میل، به گفته پژوهشگران تغییرات ایجاد شده در ارگانیسم های یك بیمار در بازدم وی انعكاس می یابد و این زیست حسگر نوین ، تشخیص وجود نشانگرهای سرطان را در مراحل اولیه بیماری امكان پذیر می كند. نفس انسان سالم یا بیمار متشكل از صدها تركیب ارگانیك مانند استون، متانول، بوتانول و هیدروكربن هاست. در بازدم یك تركیب خاص و واحد، نقش نشانگر را برای تشخیص سرطان ریه ایفا نمی كند.بلكه گستره ای از زیست نشانگرها و تركیب آنها برای تشخیص سرطان به كار می رود. این تركیبات را می توان در 20-1 واحد در هر میلیارد در تنفس انسان سالم یافت اما این میزان در تنفس افراد بیمار10 تا 100 برابر می شود. به منظور شناسایی این تغییرات ارایه مواد جدید لازم است. در طول مرحله نخست این پروژه نمونه بازدم كاركنان یك بیمارستان تهیه شد. محققان با استفاده از كروماتوگرافی گازی تركیبات ارگانیك آنها را بررسی كردند. در حال حاضر مواد نوین برای تشخیص تركیبات ارگانیك منتخب به منظور افزایش حساسیت ابزارهای تشخیصی ساخته شده اند. این زیست حسگرها می توانند مجموعه ای از بیماری های خاص عمدتا بیماری های مربوط به ریه را در مراحل اولیه بیماری تشخیص دهند.
دانشمندان زیست حسگرهایی ساخته اند كه نشانگرهای سرطان ریه را در بازدم بیمار شناسایی می كنند. به گزارش دیلی میل، به گفته پژوهشگران تغییرات ایجاد شده در ارگانیسم های یك بیمار در بازدم وی انعكاس می یابد و این زیست حسگر نوین ، تشخیص وجود نشانگرهای سرطان را در مراحل اولیه بیماری امكان پذیر می كند. نفس انسان سالم یا بیمار متشكل از صدها تركیب ارگانیك مانند استون، متانول، بوتانول و هیدروكربن هاست. در بازدم یك تركیب خاص و واحد، نقش نشانگر را برای تشخیص سرطان ریه ایفا نمی كند.بلكه گستره ای از زیست نشانگرها و تركیب آنها برای تشخیص سرطان به كار می رود. این تركیبات را می توان در 20-1 واحد در هر میلیارد در تنفس انسان سالم یافت اما این میزان در تنفس افراد بیمار10 تا 100 برابر می شود. به منظور شناسایی این تغییرات ارایه مواد جدید لازم است. در طول مرحله نخست این پروژه نمونه بازدم كاركنان یك بیمارستان تهیه شد. محققان با استفاده از كروماتوگرافی گازی تركیبات ارگانیك آنها را بررسی كردند. در حال حاضر مواد نوین برای تشخیص تركیبات ارگانیك منتخب به منظور افزایش حساسیت ابزارهای تشخیصی ساخته شده اند. این زیست حسگرها می توانند مجموعه ای از بیماری های خاص عمدتا بیماری های مربوط به ریه را در مراحل اولیه بیماری تشخیص دهند.  متخصصان يك شركت تجهيزات تشخيص پزشكي در آمريكا موفق شدهاند يك تست جديد تنفسي توليد كنند كه به شناسايي و تعيين نوع سرطان ريه در انسان با دقت فوق العاده بالا، كمك ميكند. به گزارش ايسنا، متخصصان اين شركت تحت عنوان «متابولومكس» در واقع روي شناسايي نشانههاي متابولوميكز سرطان كه در بازدم وجود دارند، متمركز شدهاند. دكتر پيتر مازون در كلينيك كليولند كه سرپرستي اين مطالعه را برعهده دارد ميگويد: دقت تست جديد در تشخيص سرطان ريه 80 درصد بيشتر از روشهاي فعلي است. شركت متابولومكس به اين ترتيب نسل اول «مجموعه حسگر كالريمتريك» را توليد ميكند.
متخصصان يك شركت تجهيزات تشخيص پزشكي در آمريكا موفق شدهاند يك تست جديد تنفسي توليد كنند كه به شناسايي و تعيين نوع سرطان ريه در انسان با دقت فوق العاده بالا، كمك ميكند. به گزارش ايسنا، متخصصان اين شركت تحت عنوان «متابولومكس» در واقع روي شناسايي نشانههاي متابولوميكز سرطان كه در بازدم وجود دارند، متمركز شدهاند. دكتر پيتر مازون در كلينيك كليولند كه سرپرستي اين مطالعه را برعهده دارد ميگويد: دقت تست جديد در تشخيص سرطان ريه 80 درصد بيشتر از روشهاي فعلي است. شركت متابولومكس به اين ترتيب نسل اول «مجموعه حسگر كالريمتريك» را توليد ميكند.