..:::: نانوحامل جدید برای توقف رشد تومورهای سرطانی ::::..
محققان نانوحامل جدیدی با ساختار هستهیی پوستهیی طراحی کردهاند که توانسته رشد تومورهای سرطان ریه و پستان را در موش متوقف کرده و موجب چروکیدگی این تومورها شود. یک گروه تحقیقاتی از مؤسسه فناوری ماساچوست، روش جدیدی برای از بین بردن تومورهای سرطانی ارائه کرده است. این گروه از نانوذرات بهعنوان حامل دارو استفاده کردند به طوری که دو داروی متفاوت درون این نانوذرات قرار داده میشوند. این دو دارو در دو زمان مختلف رهاسازی میشوند.
پژوهشگران این نانوحامل جدید را روی موشهای مبتلا به سرطان ریه و پستان آزمایش کردند. نتایج نشان داد که ابعاد تومور به شکل قابل توجهی کاهش یافته است. نتایج این پژوهش در نشریه Science Signaling به چاپ رسیده است. هاموند از محققان این گروه میگوید: «ما در حال توسعهی نانوداروهای جدید هستیم به طوری که ابتدا نانوذرات سادهای که حامل تنها یک دارو بودند ساخته میشد اما در حال حاضر پژوهشها به سوی ساخت نانوحاملهای دارویی هوشمند کشیده شده است. این نانوحاملهای هوشمند میتوانند تومورهای سرطانی را از بین ببرند.
پزشکان معمولاً برای درمان سرطان دو یا چند داروی شیمیدرمانی مختلف را برای بیمار تجویز میکنند با این امید که این ترکیب دارویی بتواند مؤثرتر از یک دارو باشد. تحقیقات متعددی روی ترکیب داروها انجام شده است که نشان میدهد این ترکیب کردن اثربخشی دارو را افزایش میدهد. در سال 2012 مقالهای منتشر شد که نشان میداد زمان رهاسازی دارو به شدت روی نتیجهی نهایی کار مؤثر است.
در این پژوهش محققان از دارویی که موجب توقف رشد کنترل نشدهی تومور میشود، استفاده کردند تا تومور را تضعیف کنند. در واقع داروی اول موجب مهار تومور شده و داروی دوم برای از بین بردن تومور وارد عمل میشود. «ارلوتینیب»، یکی از داروهای مورد استفاده در این پژوهش است. این دارو گیرندههای رشد را روی دیواره سلول هدفگیری کرده و برای درمان سرطان پانکراس و ریه استفاده میشود. «دوکسوروبیسین» نیز داروی دیگر مورد استفاده در این پژوهش بود. این دارو معمولاً برای تومورهای رحم، ریه، پستان، لنف و لگن استفاده میشود. این گروه لیپوزومی طراحی کردند که در مرکز آن دوکسوروبیسین و در لایه خارجی ارلوتینیب قرار داده شدهاست. سطح این لیپوزم با استفاده از یک لایهی پلیمری به نام PEG پوشانده شدهاست. این پلیمر دارو را از گزند سیستم ایمنی بدن محافظت کرده و اجازه فیلتر شدن آن را توسط کبد و کلیه نمیدهد.

 یک جراح اهل اورگان که در جوانی خود در جنگ ویتنام خدمت کرده بود، شریانبند جدیدی را طراحی کرده است که از خونریزی شدید در زمان آسیبدیدگی جلوگیری میکند. در آسیبدیدگیهای جنگی، پرشکان تنها 90 ثانیه فرصت دارند خونریزی را بند آورده و از مرگ فرد جلوگیری کنند. دکتر سم شاینبرگ، جراحی که در ویتنام نیز خدمت کرده بود، اولین شریانبند بادی جهان را طراحی کرده که با استقرار در ناحیه کمر، گردش خون را کنترل و خونریزیهای ناشی از انفجار بمب یا سایر آسیبدیدگیها را قطع میکند. این دستگاه طی 25 ثانیه قابل اعمال است. شاینبرگ بر اساس تجربیات خود و با همکاری شرکت طراحی زیبا در پورتلند این شریانبند را ساخته که بطور ویژه برای نجات جان سربازان در میادین جنگ طراحی شده است.
یک جراح اهل اورگان که در جوانی خود در جنگ ویتنام خدمت کرده بود، شریانبند جدیدی را طراحی کرده است که از خونریزی شدید در زمان آسیبدیدگی جلوگیری میکند. در آسیبدیدگیهای جنگی، پرشکان تنها 90 ثانیه فرصت دارند خونریزی را بند آورده و از مرگ فرد جلوگیری کنند. دکتر سم شاینبرگ، جراحی که در ویتنام نیز خدمت کرده بود، اولین شریانبند بادی جهان را طراحی کرده که با استقرار در ناحیه کمر، گردش خون را کنترل و خونریزیهای ناشی از انفجار بمب یا سایر آسیبدیدگیها را قطع میکند. این دستگاه طی 25 ثانیه قابل اعمال است. شاینبرگ بر اساس تجربیات خود و با همکاری شرکت طراحی زیبا در پورتلند این شریانبند را ساخته که بطور ویژه برای نجات جان سربازان در میادین جنگ طراحی شده است. 
 همه از افراد بدخلق که از همه چیز بدشان میآید، متنفرند اما نقطه خوشایند این است که بدخلقها کمتر در فعالیتها شرکت میکنند. اگرچه نتایج دور از انتظار یک پژوهش جدید نشان داده، افراد بدخلق و حسود در کارهای خود عملکرد بهتری نشان میدهند چرا که زمان بیشتری را برای تعداد فعالیتهای کمتر صرف میکنند.
همه از افراد بدخلق که از همه چیز بدشان میآید، متنفرند اما نقطه خوشایند این است که بدخلقها کمتر در فعالیتها شرکت میکنند. اگرچه نتایج دور از انتظار یک پژوهش جدید نشان داده، افراد بدخلق و حسود در کارهای خود عملکرد بهتری نشان میدهند چرا که زمان بیشتری را برای تعداد فعالیتهای کمتر صرف میکنند. 
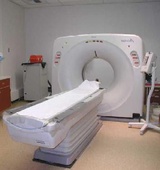 محققان آمریکایی بیمارستان Beaumont دریافتند که استفاده از سی تی اسکنهایی با منبع مضاعف (DSCT) خطر ابتلا به سرطان ناشی از مواجهه با پرتو درمانی را کاهش میدهد. با استفاه از DSCT، قرار گرفتن در برابر اشعههای پرتو درمانی در مقایسه با سی تی اسکنهای معمول تا 61 درصد کاهش مییابد و این در حالی است که کیفیت عکسهای به دست آمده از بیماران مبتلا به عروق کرونری، آمبولی ریه و یا بیماریهای آئورت با سی تی اسکنهای معمول تفاوت چشمگیری ندارد.
محققان آمریکایی بیمارستان Beaumont دریافتند که استفاده از سی تی اسکنهایی با منبع مضاعف (DSCT) خطر ابتلا به سرطان ناشی از مواجهه با پرتو درمانی را کاهش میدهد. با استفاه از DSCT، قرار گرفتن در برابر اشعههای پرتو درمانی در مقایسه با سی تی اسکنهای معمول تا 61 درصد کاهش مییابد و این در حالی است که کیفیت عکسهای به دست آمده از بیماران مبتلا به عروق کرونری، آمبولی ریه و یا بیماریهای آئورت با سی تی اسکنهای معمول تفاوت چشمگیری ندارد. 
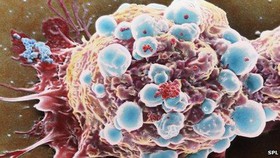 محققان اسپانیایی موفق به ساخت تراشهای شدند که قادر به شناسایی سلولهای سرطانی در مراحل اولیه است. در این تراشه از نانوذرات طلای حاوی آنتیبادی ویژهی پروتئینهای تولید شده توسط سلول سرطانی استفاده شدهاست. در حال حاضر تشخیص بیماری سرطان زمانی صورت میگیرد که تومور به قدری افزایش حجم داده که میلیونها سلول در آن رشد کرده و در حال وارد شدن به مرحلهی پیشرفتهی بیماری است. از نظر پزشکی، شناسایی سرطان را در مراحل اولیه و در حالی که هنوز چند سلول اولیه سرطانی تشکیل شده باشد اهمیت بسیاری دارد. با این کار میتوان از پیشرفت بیماری در مراحل بعدی جلوگیری کرد.
محققان اسپانیایی موفق به ساخت تراشهای شدند که قادر به شناسایی سلولهای سرطانی در مراحل اولیه است. در این تراشه از نانوذرات طلای حاوی آنتیبادی ویژهی پروتئینهای تولید شده توسط سلول سرطانی استفاده شدهاست. در حال حاضر تشخیص بیماری سرطان زمانی صورت میگیرد که تومور به قدری افزایش حجم داده که میلیونها سلول در آن رشد کرده و در حال وارد شدن به مرحلهی پیشرفتهی بیماری است. از نظر پزشکی، شناسایی سرطان را در مراحل اولیه و در حالی که هنوز چند سلول اولیه سرطانی تشکیل شده باشد اهمیت بسیاری دارد. با این کار میتوان از پیشرفت بیماری در مراحل بعدی جلوگیری کرد. 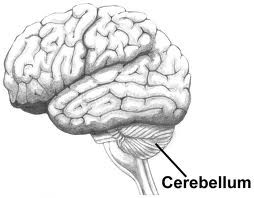 تیمی از محققان به رهبری دانشگاه اوتاوا نقش نوعی ژن خاص را در رشد مخچه کشف کردند. بر اساس یافتههای جدید، ژن Snf2h برای رشد مخچه سالم حیاتی است. این عضو مرکز کنترل تعادل، کنترل حرکات فیزیکی پیچیده و کنترل حرکات ریز است. همچنین مخچه برای انجام فعالیتهای روزانه مانند قدمزدن، خوردن و رانندگی مهم است. با حذف ژن Snf2h، محققان دریافتند مخچه کوچکتر از حد نرمال بود و تعادل و حرکات کنترلشده نیز کاهش یافت. این عضو حاوی تقریبا نیمی از عصبهای مغز است. ژن کشفشده در سلولهای بنیادی عصبی مغز قرار دارد و به عنوان یک تنظیمکننده ارجح ایفای نقش میکند. جزئیات این مطالعه در مجله Nature Communications منتشر شده است.
تیمی از محققان به رهبری دانشگاه اوتاوا نقش نوعی ژن خاص را در رشد مخچه کشف کردند. بر اساس یافتههای جدید، ژن Snf2h برای رشد مخچه سالم حیاتی است. این عضو مرکز کنترل تعادل، کنترل حرکات فیزیکی پیچیده و کنترل حرکات ریز است. همچنین مخچه برای انجام فعالیتهای روزانه مانند قدمزدن، خوردن و رانندگی مهم است. با حذف ژن Snf2h، محققان دریافتند مخچه کوچکتر از حد نرمال بود و تعادل و حرکات کنترلشده نیز کاهش یافت. این عضو حاوی تقریبا نیمی از عصبهای مغز است. ژن کشفشده در سلولهای بنیادی عصبی مغز قرار دارد و به عنوان یک تنظیمکننده ارجح ایفای نقش میکند. جزئیات این مطالعه در مجله Nature Communications منتشر شده است. دانشمندان، موفق به کشف راهی برای درمان بیماری صرع شدند. محققان دانشگاه کارولینای جنوبی، موفق به کشف شبکه پیچیدهای از پروتئین شدند که در درمان اختلالات عصبی مانند صرع، اختلال طیف اوتیسم و اسکیزوفرنی موثر است. این مجموعه شامل سه پروتئین کلیدی KCC2، Neto2 و GluK2 مورد نیاز برای ارتباطات سیناپسی مهارکننده و تحریک کننده است. KCC2 برای مهار کننده مورد نیاز است، GluK2 یک گیرنده برای فرستنده تحریکی است و Neto2 پروتئین کمکی به KCC2 و GluK2 است. پیش از این اعتقاد بر این بود که KCC2 و GluK2 در محفظههای جداگانه ایاز سلول هستند و مستقل از یکدیگر عمل میکنند، اما محققان دریافتند عملکرد آنها در تعامل با هم است.
دانشمندان، موفق به کشف راهی برای درمان بیماری صرع شدند. محققان دانشگاه کارولینای جنوبی، موفق به کشف شبکه پیچیدهای از پروتئین شدند که در درمان اختلالات عصبی مانند صرع، اختلال طیف اوتیسم و اسکیزوفرنی موثر است. این مجموعه شامل سه پروتئین کلیدی KCC2، Neto2 و GluK2 مورد نیاز برای ارتباطات سیناپسی مهارکننده و تحریک کننده است. KCC2 برای مهار کننده مورد نیاز است، GluK2 یک گیرنده برای فرستنده تحریکی است و Neto2 پروتئین کمکی به KCC2 و GluK2 است. پیش از این اعتقاد بر این بود که KCC2 و GluK2 در محفظههای جداگانه ایاز سلول هستند و مستقل از یکدیگر عمل میکنند، اما محققان دریافتند عملکرد آنها در تعامل با هم است.  بر پایه اطلاعات پژوهشی که به تازگی در نشریه نورولوژی به چاپ رسیده، مشخص شده که پرفشاری خون منجر به مشکلات حافظه در افراد بالای 45 سال میشود. این مطالعه معتقد است افراد با فشار خون دیاستولیک بالا، از اختلال شناختی یا مشکلات حافظهای و تواناییهای فکری بیشتری نسبت به افرادی که فشار دیاستولیک طبیعی دارند، رنج میبرند. به ازای هر 10 میلیمتر جیوه افزایش در این نوع فشار، شانس ابتلا به مشکلات شناختی هفت درصد بیشتر میشود. این نتایج معتبر پس از تعدیل سایر عواملی که میتوانند بر تواناییهای شناختی تاثیر بگذارند، مانند سن، سیگار کشیدن، فعالیت فیزیکی، سطح تحصیلات، دیابت یا کلسترول بالا منتشر شدهاند.
بر پایه اطلاعات پژوهشی که به تازگی در نشریه نورولوژی به چاپ رسیده، مشخص شده که پرفشاری خون منجر به مشکلات حافظه در افراد بالای 45 سال میشود. این مطالعه معتقد است افراد با فشار خون دیاستولیک بالا، از اختلال شناختی یا مشکلات حافظهای و تواناییهای فکری بیشتری نسبت به افرادی که فشار دیاستولیک طبیعی دارند، رنج میبرند. به ازای هر 10 میلیمتر جیوه افزایش در این نوع فشار، شانس ابتلا به مشکلات شناختی هفت درصد بیشتر میشود. این نتایج معتبر پس از تعدیل سایر عواملی که میتوانند بر تواناییهای شناختی تاثیر بگذارند، مانند سن، سیگار کشیدن، فعالیت فیزیکی، سطح تحصیلات، دیابت یا کلسترول بالا منتشر شدهاند.