..:::: نخستین کاشت پمپ در بدن برای مبارزه با سرطان ::::..
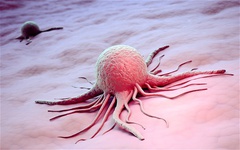 یک بیمار انگلیسی مبتلا به سرطان به عنوان اولین فرد در جهان در فرآیندی که به باور پزشکان میتواند یک دستاورد بزرگ برای درمان این بیماری باشد، موفق به کاشت یک پمپ در بدن خود شد. به ادعای متخصصان، این تجربه میتواند نقش مهمی را در زندگی هزاران بیمار سرطانی ایفا کند. این پمپ برای خلاصی از مایع خطرناک ساخته شده در بسیاری از سرطانها طراحی شده که میتواند منجر به نیاز به مراجعه کمتر بیمار به بیمارستان شود. در طولانی مدت امید است که این دستگاه بتواند پیگیری شیوههای تغییر سرطان را تسهیل کرده تا پزشکان بتوانند با درمانهای جدید واکنش نشان دهند.
یک بیمار انگلیسی مبتلا به سرطان به عنوان اولین فرد در جهان در فرآیندی که به باور پزشکان میتواند یک دستاورد بزرگ برای درمان این بیماری باشد، موفق به کاشت یک پمپ در بدن خود شد. به ادعای متخصصان، این تجربه میتواند نقش مهمی را در زندگی هزاران بیمار سرطانی ایفا کند. این پمپ برای خلاصی از مایع خطرناک ساخته شده در بسیاری از سرطانها طراحی شده که میتواند منجر به نیاز به مراجعه کمتر بیمار به بیمارستان شود. در طولانی مدت امید است که این دستگاه بتواند پیگیری شیوههای تغییر سرطان را تسهیل کرده تا پزشکان بتوانند با درمانهای جدید واکنش نشان دهند.
این بیمار انگلیسی یک زن 62 ساله بود که طی یک عمل پیوند یک ساعته در بیمارستان هامراسمیت لندن این پمپ را در زیر پوست خود قرار داد. سرطان تخمدان باعث آزار این بیمار شده بود که مجبور بود هر سه هفته یکبار برای تخلیه چهار تا پنج لیتر از مایع ایجاد شده توسط این بیماری از بدن به بیمارستان مراجعه کند. این مایع بدین معنی است که بیمار قادر به خوردن غذا نبود. حدود یک سوم زنان مبتلا به سرطان تخمدان با مایع آسیت در بدن خود دست و پنجه نرم میکنند که یک تجمع مایع در شکم بوده و بیماران مبتلا به سرطانهای روده، پانکراس، رحم و پستان نیز ممکن است مشکلات مایع را تجربه کنند. در حال حاضر بیماران باید به بیمارستان رفته و در فرآیندی که ممکن است چند روز به طول بینجامد، این مایع را تخلیه کنند. این امر میتواند منجر به مرگ شود.
یک کارآزمایی بالینی کامل قرار است به زودی آغاز شده و این کاشت فعلا بطور دائمی در دسترس نخواهد بود اما در صورت اثبات موفق بودن آن، میتواند درمان بسیاری از سرطانها را با تغییر مواجه کند. دستگاه «alfapump»مایعات را از شکم بیمار به درون مثانه پمپاژ کرده تا از طریق ادرار از بدن خارج شود. پزشکان سپس میتوانند ادرار را برای ارزیابی پیشرفت سرطان و واکنش متعاقب بررسی کنند. این رویکرد بر روی بیماران کبدی آزمایش شده اما این عمل جراحی پیشگامانه نشانگر اولین استفاده از این دستگاه برای درمان سرطان بوده است.
 محققان با مقایسه موشهای آزمایشگاهی تغذیه شده با یک جزء اصلی از رژیم غذایی با فیبر بالا به نام اینوزیتول هگزافسفات (IP6)و موشهای گروه شاهد مشاهده کردند رژیمهای غذایی سرشار از فیبر، پتانسیل بالینی لازم برای کنترل پیشروی سرطان پروستات در بیمارانی که در مرحله اول تشخیص این بیماری هستند را دارد. محققان مرکز سرطان در دانشگاه کلرادو با هدایت ام آر آی در گروه موشهای مورد آزمایش دریافتند به دلیل اثرات آنتی آنژیوژنیک IP6و در واقع تغذیه با جزء تشکیل دهنده فعالی از یک رژیم غذایی با فیبر بالا، حجم تومورها بهطور چشمگیری کاهش یافته و IP6تومور پروستات را از ساخت عروق خونی جدید که برای تامین انرژی نیاز است نگه می دارد که بدون این انرژی، سرطان پروستات نمی تواند توسعه یابد و به همین ترتیب درمان با IP6 روند متابولیسم گلوکز در سرطان پروستات را کند میکند.
محققان با مقایسه موشهای آزمایشگاهی تغذیه شده با یک جزء اصلی از رژیم غذایی با فیبر بالا به نام اینوزیتول هگزافسفات (IP6)و موشهای گروه شاهد مشاهده کردند رژیمهای غذایی سرشار از فیبر، پتانسیل بالینی لازم برای کنترل پیشروی سرطان پروستات در بیمارانی که در مرحله اول تشخیص این بیماری هستند را دارد. محققان مرکز سرطان در دانشگاه کلرادو با هدایت ام آر آی در گروه موشهای مورد آزمایش دریافتند به دلیل اثرات آنتی آنژیوژنیک IP6و در واقع تغذیه با جزء تشکیل دهنده فعالی از یک رژیم غذایی با فیبر بالا، حجم تومورها بهطور چشمگیری کاهش یافته و IP6تومور پروستات را از ساخت عروق خونی جدید که برای تامین انرژی نیاز است نگه می دارد که بدون این انرژی، سرطان پروستات نمی تواند توسعه یابد و به همین ترتیب درمان با IP6 روند متابولیسم گلوکز در سرطان پروستات را کند میکند.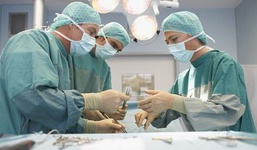 محققان دانشگاه کالیفرنیا در ساندیگو توانستند شیوه پیشگامانهای را ابداع کنند که میزان گسترش سرطان در غدد لنفاوی را نشان میدهد. این شیوه که از مولکولهای فلورسنت استفاده میکند، به جراحان اجازه خواهد داد تا غدد لنفاوی سرطانی را شناسایی کرده و بافتهای سالم را نجات دهند. غدد لنفاوی که در سراسر بدن گسترش یافتهاند، نقش مهمی را در کمک به بدن در شناسایی و مبارزه با میکروبها ایفا میکنند. این غدهها به عنوان فیلترهایی عمل میکنند که حاوی سلولهای ایمنی برای مبارزه با عفونت و پاکسازی پوست هستند. هنگامی که سلولهای سرطانی از یک تومور در هر قسمت از بدن جدا میشوند، میتوانند در سیستم لنفاوی حرکت کرده و در این اندام کوچک پنهان شوند. جراحان این غدد را برای اطمینان از امکان گسترش سرطان و میزان آن برمیدارند.
محققان دانشگاه کالیفرنیا در ساندیگو توانستند شیوه پیشگامانهای را ابداع کنند که میزان گسترش سرطان در غدد لنفاوی را نشان میدهد. این شیوه که از مولکولهای فلورسنت استفاده میکند، به جراحان اجازه خواهد داد تا غدد لنفاوی سرطانی را شناسایی کرده و بافتهای سالم را نجات دهند. غدد لنفاوی که در سراسر بدن گسترش یافتهاند، نقش مهمی را در کمک به بدن در شناسایی و مبارزه با میکروبها ایفا میکنند. این غدهها به عنوان فیلترهایی عمل میکنند که حاوی سلولهای ایمنی برای مبارزه با عفونت و پاکسازی پوست هستند. هنگامی که سلولهای سرطانی از یک تومور در هر قسمت از بدن جدا میشوند، میتوانند در سیستم لنفاوی حرکت کرده و در این اندام کوچک پنهان شوند. جراحان این غدد را برای اطمینان از امکان گسترش سرطان و میزان آن برمیدارند.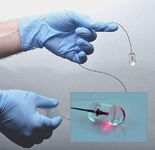 محققان بیمارستان عمومی ماساچوست، نوعی دوربین قرصی بلعیدنی را ساختهاند که میتواند به پزشکان در تشخیص نشانههای اولیه سرطان مری کمک کند. این دستگاه شفاف فناوری پیشرفته، به اندازه یک قرص مولتی ویتامین بزرگ بوده و حاوی لیزری با سرعت چرخش بالاست که یک پرتو نور نزدیک مادون قرمز را به دیواره مری میتاباند. سپس حسگرها بازتاب نور را ثبت کرده و تصاویر دقیق میکروسکوپی را تولید میکنند که میتواند تغییرات سلولی مرتبط با سندروم «بارت» را که شرایط پیش سرطانی مرتبط با سوزش سردل و رفلکس اسید است، آشکار سازد.
محققان بیمارستان عمومی ماساچوست، نوعی دوربین قرصی بلعیدنی را ساختهاند که میتواند به پزشکان در تشخیص نشانههای اولیه سرطان مری کمک کند. این دستگاه شفاف فناوری پیشرفته، به اندازه یک قرص مولتی ویتامین بزرگ بوده و حاوی لیزری با سرعت چرخش بالاست که یک پرتو نور نزدیک مادون قرمز را به دیواره مری میتاباند. سپس حسگرها بازتاب نور را ثبت کرده و تصاویر دقیق میکروسکوپی را تولید میکنند که میتواند تغییرات سلولی مرتبط با سندروم «بارت» را که شرایط پیش سرطانی مرتبط با سوزش سردل و رفلکس اسید است، آشکار سازد. محققان ژاپنی برای نخستین بار موفق به تولید سلولهای قاتلی شدهاند که با تزریق به بدن بیمار میتوانند سلول های سرطانی خاص را نابود کنند. بدن انسان حاوی سلول های ایمنی برنامه ریزی شده برای مقابله با سرطان و عفونت های ویروسی است، اما تعداد کم و عمر کوتاه این سلول ها باعث ناکامی در مقابله با بیماری های تهاجمی مانند سرطان و ایدز می شود. محققان مرکز تحقیقات آلرژی و ایمونولوژی RIKEN ژاپن به سرپرستی پروفسور «هیروشی کاواموتو» برای نخستین بار با استفاده از فناوری سلول های بنیادی، موفق به بازسازی سلول های ایمنی بدن و تولید تعداد فراوانی سلول قاتل شدند. این سلول های سیستم ایمنی، لنفوسیت های تی قاتل (T lymphocytes) نامیده می شوند.
محققان ژاپنی برای نخستین بار موفق به تولید سلولهای قاتلی شدهاند که با تزریق به بدن بیمار میتوانند سلول های سرطانی خاص را نابود کنند. بدن انسان حاوی سلول های ایمنی برنامه ریزی شده برای مقابله با سرطان و عفونت های ویروسی است، اما تعداد کم و عمر کوتاه این سلول ها باعث ناکامی در مقابله با بیماری های تهاجمی مانند سرطان و ایدز می شود. محققان مرکز تحقیقات آلرژی و ایمونولوژی RIKEN ژاپن به سرپرستی پروفسور «هیروشی کاواموتو» برای نخستین بار با استفاده از فناوری سلول های بنیادی، موفق به بازسازی سلول های ایمنی بدن و تولید تعداد فراوانی سلول قاتل شدند. این سلول های سیستم ایمنی، لنفوسیت های تی قاتل (T lymphocytes) نامیده می شوند.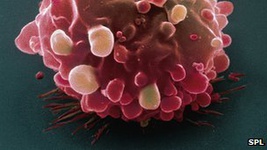 محققان انگلیسی به تازگی موفق به کشف دو ژن شدهاند که از والد به فرزند منتقل میشود و به طور قابل توجهی خطر تشکیل تومور سرطان روده را افزایش میدهد. دانشمندان دانشگاه آکسفورد و مؤسسه تحقیقات سرطان در لندن مدعیاند با این کشف خواهند توانست دلیل آسیبپذیری خانوادهها در مقابل این نوع سرطان را توضیح دهند. آنها در مطالعاتشان دی ان ای 20 بیمار مبتلا به سرطان روده و دارای سابقه خانوادگی ابتلا به آن را مورد بررسی قرار دادند. این متخصصان با مطالعه کد ژنتیکی نمونه موردیهای مزبور به خطاهایی در دو ژن پی بردند که شانس ابتلا به این بیماری مهلک را افزایش میدهد. به گفته آنها، در این مطالعه افراد دارای نسخه اشتباه POLE یا POLD1 به سرطان روده مبتلا بودند یا یک رشد پیشسرطانی را در رودههایشان داشتند. دانشمندان سپس چهار هزار بیمار مبتلا به سرطان مزبور و شش هزار و 700 فرد سالم را بررسی کردند و دریافتند که این جهشها در هیچ یک از افراد سالم حاضر در نمونه موردی مشاهده نشدند. به گفته «ایان توملینسون» رهبر ارشد تیم تحقیقاتی، این جهشها نادرند اما وجود یکی از آنها برای ابتلا به سرطان روده کافی است. جزئیات این مطالعه در Nature Genetics انتشار یافت.
محققان انگلیسی به تازگی موفق به کشف دو ژن شدهاند که از والد به فرزند منتقل میشود و به طور قابل توجهی خطر تشکیل تومور سرطان روده را افزایش میدهد. دانشمندان دانشگاه آکسفورد و مؤسسه تحقیقات سرطان در لندن مدعیاند با این کشف خواهند توانست دلیل آسیبپذیری خانوادهها در مقابل این نوع سرطان را توضیح دهند. آنها در مطالعاتشان دی ان ای 20 بیمار مبتلا به سرطان روده و دارای سابقه خانوادگی ابتلا به آن را مورد بررسی قرار دادند. این متخصصان با مطالعه کد ژنتیکی نمونه موردیهای مزبور به خطاهایی در دو ژن پی بردند که شانس ابتلا به این بیماری مهلک را افزایش میدهد. به گفته آنها، در این مطالعه افراد دارای نسخه اشتباه POLE یا POLD1 به سرطان روده مبتلا بودند یا یک رشد پیشسرطانی را در رودههایشان داشتند. دانشمندان سپس چهار هزار بیمار مبتلا به سرطان مزبور و شش هزار و 700 فرد سالم را بررسی کردند و دریافتند که این جهشها در هیچ یک از افراد سالم حاضر در نمونه موردی مشاهده نشدند. به گفته «ایان توملینسون» رهبر ارشد تیم تحقیقاتی، این جهشها نادرند اما وجود یکی از آنها برای ابتلا به سرطان روده کافی است. جزئیات این مطالعه در Nature Genetics انتشار یافت. محققان دانشگاه ایالتی پنسیلوانیا طی پژوهشی دریافتند که میتوان گسترش سلولهای سرطانی را با هدف قرار دادن پروتئینی محرک موسوم به "km23-1" که در حرکت و جابهجایی سلولی نیز دخیل است، کاهش داد. حرکت سلولی جنبه مهمی در فرآیند گسترش یک تومور است. تغییرات به وجود آمده طی این فرآیند میتواند سلول تومور را از سلولهای محلی، غیرتهاجمی و محدود به سوی سلولهای سرطانی متاستاتیک (جا به جا شونده) انتقال دهد. سلولها با استفاده از پروتئین اکتین که چارچوب ساختاری سلول را میسازد، در بدن حرکت میکند. اکتین با ایجاد رشتههایی از فیبرهای ریسمانی شکل بر لبه سلول، برآمدگی را در غشای سلول به وجود میآورد که باعث به جلو راندن سلول میشود. چندین پروتئین شناخته شده، سازماندهی مجدد چارچوب سلول را تنظیم میکنند که نشان داده شده است این پروتئینها در بعضی سرطانها نیز فعالتر هستند.
محققان دانشگاه ایالتی پنسیلوانیا طی پژوهشی دریافتند که میتوان گسترش سلولهای سرطانی را با هدف قرار دادن پروتئینی محرک موسوم به "km23-1" که در حرکت و جابهجایی سلولی نیز دخیل است، کاهش داد. حرکت سلولی جنبه مهمی در فرآیند گسترش یک تومور است. تغییرات به وجود آمده طی این فرآیند میتواند سلول تومور را از سلولهای محلی، غیرتهاجمی و محدود به سوی سلولهای سرطانی متاستاتیک (جا به جا شونده) انتقال دهد. سلولها با استفاده از پروتئین اکتین که چارچوب ساختاری سلول را میسازد، در بدن حرکت میکند. اکتین با ایجاد رشتههایی از فیبرهای ریسمانی شکل بر لبه سلول، برآمدگی را در غشای سلول به وجود میآورد که باعث به جلو راندن سلول میشود. چندین پروتئین شناخته شده، سازماندهی مجدد چارچوب سلول را تنظیم میکنند که نشان داده شده است این پروتئینها در بعضی سرطانها نیز فعالتر هستند.  محققان انگلیسی از گاز منجمد برای از بین بردن تومورهای سرطان کلیه استفاده کردند که این امر به معنای عدم نیاز به استفاده از بخیه و بستری طولانی مدت در بیمارستان است. در جراحی لاپاراسکوپی که به جراحی سوراخ کلید (keyhole surgery) نیز معروف است، جراح با ایجاد یک حفره کوچک، تومور را از کلیه خارج میکند. محققان دانشگاه ساوت هامپتون روش دمای فوق سرد را برای نابود کردن سلولهای سرطان کلیه مورد آزمایش قرار داده اند؛ با استفاده از دستگاه سی تی اسکن، تصویری از تومور تهیه شده و بین چهار تا پنج سوزن نازک تر از سر مداد وارد بافت سرطانی میشود.
محققان انگلیسی از گاز منجمد برای از بین بردن تومورهای سرطان کلیه استفاده کردند که این امر به معنای عدم نیاز به استفاده از بخیه و بستری طولانی مدت در بیمارستان است. در جراحی لاپاراسکوپی که به جراحی سوراخ کلید (keyhole surgery) نیز معروف است، جراح با ایجاد یک حفره کوچک، تومور را از کلیه خارج میکند. محققان دانشگاه ساوت هامپتون روش دمای فوق سرد را برای نابود کردن سلولهای سرطان کلیه مورد آزمایش قرار داده اند؛ با استفاده از دستگاه سی تی اسکن، تصویری از تومور تهیه شده و بین چهار تا پنج سوزن نازک تر از سر مداد وارد بافت سرطانی میشود. پژوهشگران آمریکایی روشی برای افزایش تاثیر داروی ضدتومور سرطانی یافتهاند. در این روش آنها یک شبکه مغناطیسی شونده را در محل نزدیک تومور قرار داده و سپس نانوذرات اکسید آهن حاوی دارو را به بدن تزریق و میدان مغناطیسی اعمال میکنند. مدتهاست که پژوهشگران به دنبال استفاده از میدان مغناطیسی برای افزایش غلظت وارد شدن نانوذرات اکسید آهن در تومورها هستند. با این حال، میدانهای مغناطیسی با افزایش فاصله دچار زوال میشوند، بنابراین در صورتی که تومورها در بخشهای عمیق بدن باشند، بیش از چند سانتیمتر عمق، تاثیر میدان مغناطیسی زیاد نخواهد بود.
پژوهشگران آمریکایی روشی برای افزایش تاثیر داروی ضدتومور سرطانی یافتهاند. در این روش آنها یک شبکه مغناطیسی شونده را در محل نزدیک تومور قرار داده و سپس نانوذرات اکسید آهن حاوی دارو را به بدن تزریق و میدان مغناطیسی اعمال میکنند. مدتهاست که پژوهشگران به دنبال استفاده از میدان مغناطیسی برای افزایش غلظت وارد شدن نانوذرات اکسید آهن در تومورها هستند. با این حال، میدانهای مغناطیسی با افزایش فاصله دچار زوال میشوند، بنابراین در صورتی که تومورها در بخشهای عمیق بدن باشند، بیش از چند سانتیمتر عمق، تاثیر میدان مغناطیسی زیاد نخواهد بود.  استفاده از نانوذرات جدید جهت درمان سرطانها، تحویل دارو به بافتهای سالم را کاهش میدهد. محققان دانشگاه کیس وسترن با انجام بررسیهای خود توانستند به نانوذرات جدیدی دستیابی پیدا کنند که ضمن رساندن داروها به سلولهای تومورال، انتقال آنها به سلولهای غیرهدف و سالم را به حداقل میرساند. استفاده از این نانو ذرات در مدل حیوانی توانست به مدت بیشتری در گردش خون گروه مورد آزمایش باقی بماند و رسوب بیشتری را در داخل تومورها نشان دهد. تحقیقات قبلی نشان دادهاند داروهای وابسته به نانوذرات در بسیاری از سلولهای سرطانی انتقال نمییابند زیرا تحویل آنها به سلولهای تومورال به طور یکنواخت نبوده و در نتیجه مقادیر عظیمی از آنها در اطراف عروق جمع میشوند. به گفته محققان استفاده از این نانو ذرات جدید بر اساس نانو زنجیرههای چند بخشی منجر به رساندن داروها به بیشتر سلولهای سرطانی شده و باعث از بین رفتن سلولهای توموری میشود. یافتههای این تحقیق در نشریه نانو ACS منتشر شده است.
استفاده از نانوذرات جدید جهت درمان سرطانها، تحویل دارو به بافتهای سالم را کاهش میدهد. محققان دانشگاه کیس وسترن با انجام بررسیهای خود توانستند به نانوذرات جدیدی دستیابی پیدا کنند که ضمن رساندن داروها به سلولهای تومورال، انتقال آنها به سلولهای غیرهدف و سالم را به حداقل میرساند. استفاده از این نانو ذرات در مدل حیوانی توانست به مدت بیشتری در گردش خون گروه مورد آزمایش باقی بماند و رسوب بیشتری را در داخل تومورها نشان دهد. تحقیقات قبلی نشان دادهاند داروهای وابسته به نانوذرات در بسیاری از سلولهای سرطانی انتقال نمییابند زیرا تحویل آنها به سلولهای تومورال به طور یکنواخت نبوده و در نتیجه مقادیر عظیمی از آنها در اطراف عروق جمع میشوند. به گفته محققان استفاده از این نانو ذرات جدید بر اساس نانو زنجیرههای چند بخشی منجر به رساندن داروها به بیشتر سلولهای سرطانی شده و باعث از بین رفتن سلولهای توموری میشود. یافتههای این تحقیق در نشریه نانو ACS منتشر شده است. محققان سنگاپوری با استفاده از خودآرایی نانوذراتی تهیه کردهاند که میتواند پزشکان را برای تشخیص بیماریها بینیاز از نمونهبرداری کند. برای این که بتوان وجود یک بیماری نظیر سرطان را روی بافتهای نرم تشخیص داد باید نمونه برداری از آن بافت انجام شود. اخیرا محققان سنگاپوری موسسه آاستار با استفاده از خودآرایی نانوذراتی تهیه کردهاند که میتواند پزشکان را بینیاز از نمونهبرداری کند. با این روش، ایمنی میکروسکوپ دو فوتونی، که روشی فلورسانس برای مشاهده سلولهای سرطانی است، افزایش مییابد.
محققان سنگاپوری با استفاده از خودآرایی نانوذراتی تهیه کردهاند که میتواند پزشکان را برای تشخیص بیماریها بینیاز از نمونهبرداری کند. برای این که بتوان وجود یک بیماری نظیر سرطان را روی بافتهای نرم تشخیص داد باید نمونه برداری از آن بافت انجام شود. اخیرا محققان سنگاپوری موسسه آاستار با استفاده از خودآرایی نانوذراتی تهیه کردهاند که میتواند پزشکان را بینیاز از نمونهبرداری کند. با این روش، ایمنی میکروسکوپ دو فوتونی، که روشی فلورسانس برای مشاهده سلولهای سرطانی است، افزایش مییابد. تحقیقات صورت گرفته توسط محققان دانشگاه آلاباما نشان میدهد، ترکیب مشتق از سم عقرب میتواند به تشخیص بافتهای سالم از بافت تومور مغزی کمک کند. بافت سرطانی و سالم با چشمان غیرمسلح یکسان به نظر میرسند و متخصصان بدنبال ابداع روشی مؤثر برای ایجاد تمایز بین بافت سالم و سرطانی مغز هستند.
تحقیقات صورت گرفته توسط محققان دانشگاه آلاباما نشان میدهد، ترکیب مشتق از سم عقرب میتواند به تشخیص بافتهای سالم از بافت تومور مغزی کمک کند. بافت سرطانی و سالم با چشمان غیرمسلح یکسان به نظر میرسند و متخصصان بدنبال ابداع روشی مؤثر برای ایجاد تمایز بین بافت سالم و سرطانی مغز هستند.  پژوهش انجام شده توسط انجمن سرطان آمریکا رابطهای معکوس و مشهود را بین مصرف قهوه کافئیندار و مرگ و میر ناشی از سرطانهای حلق و دهان نشان میدهد. محققان میگویند نوشیدن روزانه بیش از چهار فنجان در روز قهوه خطر مرگ ناشی از سرطانهای اغلب کشنده دهانی را تا 50 درصد کاهش میدهد. محققان به منظور درک رابطه مصرف قهوه کافئین دار، قهوه بدون کافئین، چای و سرطان حلق و دهان کشنده، مطالعهای آینده نگر را از سال 1982 بر روی 968 هزار و 432 مرد و زن سالم انجام دادند. طی 26 سال مطالعه، 868 مورد مرگ ناشی از سرطان حلق و دهان رخ داد.
پژوهش انجام شده توسط انجمن سرطان آمریکا رابطهای معکوس و مشهود را بین مصرف قهوه کافئیندار و مرگ و میر ناشی از سرطانهای حلق و دهان نشان میدهد. محققان میگویند نوشیدن روزانه بیش از چهار فنجان در روز قهوه خطر مرگ ناشی از سرطانهای اغلب کشنده دهانی را تا 50 درصد کاهش میدهد. محققان به منظور درک رابطه مصرف قهوه کافئین دار، قهوه بدون کافئین، چای و سرطان حلق و دهان کشنده، مطالعهای آینده نگر را از سال 1982 بر روی 968 هزار و 432 مرد و زن سالم انجام دادند. طی 26 سال مطالعه، 868 مورد مرگ ناشی از سرطان حلق و دهان رخ داد.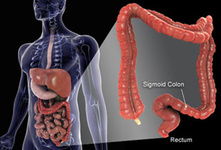 آنالیز عملکرد تنفسی میتواند برای غربالگری سرطان کولون (روده بزرگ) و رکتوم (مقعد) مورد استفاده قرار گیرد. گروهی از محققان که یافتههای پژوهشی آنها در نشریه انگلیسی جراحی منتشر شده است، با جمعآوری و پردازش نمونههای بازدم 37 بیمار مبتلا به سرطان کولورکتال و نیز 41 فرد سالم دریافتند الگوهای مختلف ترکیبات آلی فرار (VOC) قادر است بیماران مبتلا به این سرطان را از گروه شاهد متمایز کند. محققان از شبکه عصبی احتمالاتی برای شناسایی الگوی فرآیند ترکیبات آلی فرار در دو گروه مورد مطالعه استفاده کردند که این روش قادر به تعیین بیماران مبتلا با دقت بیش از 75 درصد بود. به گفته محققان اگرچه روش نمونهگیری تنفسی، روشی بسیار آسان و غیرتهاجمی است و هنوز در مرحله اولیه توسعه خود است اما یافتههای این مطالعه ما را به حمایت بیشتری از ارزش این تست به عنوان یک ابزار برای غربالگری کمک میکند. سرطان کولورکتال شایعترین سرطان دستگاه گوارش است و هنگامی رخ میدهد که سلولهای غیرطبیعی در دیواره روده بزرگ یا مقعد رشد کنند.
آنالیز عملکرد تنفسی میتواند برای غربالگری سرطان کولون (روده بزرگ) و رکتوم (مقعد) مورد استفاده قرار گیرد. گروهی از محققان که یافتههای پژوهشی آنها در نشریه انگلیسی جراحی منتشر شده است، با جمعآوری و پردازش نمونههای بازدم 37 بیمار مبتلا به سرطان کولورکتال و نیز 41 فرد سالم دریافتند الگوهای مختلف ترکیبات آلی فرار (VOC) قادر است بیماران مبتلا به این سرطان را از گروه شاهد متمایز کند. محققان از شبکه عصبی احتمالاتی برای شناسایی الگوی فرآیند ترکیبات آلی فرار در دو گروه مورد مطالعه استفاده کردند که این روش قادر به تعیین بیماران مبتلا با دقت بیش از 75 درصد بود. به گفته محققان اگرچه روش نمونهگیری تنفسی، روشی بسیار آسان و غیرتهاجمی است و هنوز در مرحله اولیه توسعه خود است اما یافتههای این مطالعه ما را به حمایت بیشتری از ارزش این تست به عنوان یک ابزار برای غربالگری کمک میکند. سرطان کولورکتال شایعترین سرطان دستگاه گوارش است و هنگامی رخ میدهد که سلولهای غیرطبیعی در دیواره روده بزرگ یا مقعد رشد کنند.  شناسایی پروتئینهای دخیل در توسعه سرطان کلیه، به طور بالقوه میتواند به پیشبینی متاستاز این سرطان کمک کند. تیمی از محققان که یافتههای آنها در نشریه «مولکولی و پروتئومیکس سلولی» منتشر شده، با استفاده از طیف سنجی جرمی توانستند 29 پروتئین را که به احتمال زیاد در گسترش سرطان کلیه نقش دارند، شناسایی کنند که تمامی این پروتئینها به بدخیمیهای دیگر مرتبط بودهاند. محققان با اشاره به نتایج این تحقیق اظهار کردند: این کشف میتواند در تشخیص تومورهای تهاجمی مؤثر باشد و اقدامات درمانی فشردهتری را با اقدامهای به موقع برای بیماران مبتلا فراهم کند.
شناسایی پروتئینهای دخیل در توسعه سرطان کلیه، به طور بالقوه میتواند به پیشبینی متاستاز این سرطان کمک کند. تیمی از محققان که یافتههای آنها در نشریه «مولکولی و پروتئومیکس سلولی» منتشر شده، با استفاده از طیف سنجی جرمی توانستند 29 پروتئین را که به احتمال زیاد در گسترش سرطان کلیه نقش دارند، شناسایی کنند که تمامی این پروتئینها به بدخیمیهای دیگر مرتبط بودهاند. محققان با اشاره به نتایج این تحقیق اظهار کردند: این کشف میتواند در تشخیص تومورهای تهاجمی مؤثر باشد و اقدامات درمانی فشردهتری را با اقدامهای به موقع برای بیماران مبتلا فراهم کند.  محققان دانشگاه تنسي يك فرآيند ليزري فوق سريع ايجاد كردهاند كه ميتواند به عنوان درمان غير تهاجمي براي سرطان بويژه در سرطانهاي مغزي مورد استفاده قرار بگيرد. اين فناوري در مركز كابردهاي ليزر دانشگاه تنسي ايجاد شده و به بررسي و تخريب تومورهاي سرطاني ميپردازد. اين شيوه از يك ليزر فمتوثانيه استفاده كرده كه بسيار پر سرعت بوده و در سرعت يك كوادريليوم ثانيه، پالس ارسال ميكند. چنين سرعت بالايي، زوم كردن در يك منطقه خاص براي بررسي و نقشهبرداري دقيق از يك تومور را ممكن ميسازد.
محققان دانشگاه تنسي يك فرآيند ليزري فوق سريع ايجاد كردهاند كه ميتواند به عنوان درمان غير تهاجمي براي سرطان بويژه در سرطانهاي مغزي مورد استفاده قرار بگيرد. اين فناوري در مركز كابردهاي ليزر دانشگاه تنسي ايجاد شده و به بررسي و تخريب تومورهاي سرطاني ميپردازد. اين شيوه از يك ليزر فمتوثانيه استفاده كرده كه بسيار پر سرعت بوده و در سرعت يك كوادريليوم ثانيه، پالس ارسال ميكند. چنين سرعت بالايي، زوم كردن در يك منطقه خاص براي بررسي و نقشهبرداري دقيق از يك تومور را ممكن ميسازد. آسپرین میتواند خطر ابتلا به سرطان کبد و مرگ و میر ناشی از بیماریهای کبدی را کاهش دهد. مطالعات جدید حاکی از آن است که مصرف روزانه آسپرین با کاهش خطر ابتلا به سرطان کبد و مرگ و میر ناشی از بیماریهای مزمن کبدی همراه است. این مطالعه بر روی بیش از 300 هزار نفر که درسنین50 تا 71 سالگی بودند به مدت 10 تا 12 سال انجام گرفت. این افراد آسپرین و داروهای ضدالتهابی غیراستروئیدی (NSAID) را استفاده میکردند. در این بررسی، بیش از 400 شرکتکننده به علت بیماری مزمن کبدی درگذشتند و همچنین 250 فرد مبتلا به سرطان کبد تشخیص داده شدند. در مقایسه با افرادی که داروهای ضدالتهابی غیراستروئیدی مصرف نمیکنند، افرادی که آسپرین مصرف میکنند، مشخص شد 45 درصد کمتر احتمال دارد در اثر بیماری کبدی مزمن جان خود را از دست دهند و 41 درصد کمتر احتمال دارد که مبتلا به سرطان کبد شوند.
آسپرین میتواند خطر ابتلا به سرطان کبد و مرگ و میر ناشی از بیماریهای کبدی را کاهش دهد. مطالعات جدید حاکی از آن است که مصرف روزانه آسپرین با کاهش خطر ابتلا به سرطان کبد و مرگ و میر ناشی از بیماریهای مزمن کبدی همراه است. این مطالعه بر روی بیش از 300 هزار نفر که درسنین50 تا 71 سالگی بودند به مدت 10 تا 12 سال انجام گرفت. این افراد آسپرین و داروهای ضدالتهابی غیراستروئیدی (NSAID) را استفاده میکردند. در این بررسی، بیش از 400 شرکتکننده به علت بیماری مزمن کبدی درگذشتند و همچنین 250 فرد مبتلا به سرطان کبد تشخیص داده شدند. در مقایسه با افرادی که داروهای ضدالتهابی غیراستروئیدی مصرف نمیکنند، افرادی که آسپرین مصرف میکنند، مشخص شد 45 درصد کمتر احتمال دارد در اثر بیماری کبدی مزمن جان خود را از دست دهند و 41 درصد کمتر احتمال دارد که مبتلا به سرطان کبد شوند.  پژوهش محققان سوئدی نشان میدهد مردانی که روزانه میزان معمولی از نوشیدنیهای شیرین را مصرف میکنند در خطر افزایش ابتلا به نوع تهاجمی سرطان پروستات قرار دارند. محققان به منظور درک رابطه بین نوشیدنیهای شیرین و خطر سرطان پروستات، هشت هزار مرد 45 تا 75 ساله را به مدت تقریبا 15 سال مورد بررسی قرار دادند. بر اساس این گزارش، افرادی که روزانه 330 میلی لیتر نوشیدنی شیرین مصرف میکردند، 40 درصد بیش از سایرین در خطر ابتلا به نوع مزمن سرطان پروستات که مستلزم درمان است، قرار دارند. مصرف رژیم غذایی غنی از برنج و پاستا خطر ابتلا به نوع خفیفتر این بیماری را که نیازی به درمان ندارد، 31 درصد و مصرف بالای غلات صبحانهای شیرین این درصد را به 38 درصد افزایش میدهد.
پژوهش محققان سوئدی نشان میدهد مردانی که روزانه میزان معمولی از نوشیدنیهای شیرین را مصرف میکنند در خطر افزایش ابتلا به نوع تهاجمی سرطان پروستات قرار دارند. محققان به منظور درک رابطه بین نوشیدنیهای شیرین و خطر سرطان پروستات، هشت هزار مرد 45 تا 75 ساله را به مدت تقریبا 15 سال مورد بررسی قرار دادند. بر اساس این گزارش، افرادی که روزانه 330 میلی لیتر نوشیدنی شیرین مصرف میکردند، 40 درصد بیش از سایرین در خطر ابتلا به نوع مزمن سرطان پروستات که مستلزم درمان است، قرار دارند. مصرف رژیم غذایی غنی از برنج و پاستا خطر ابتلا به نوع خفیفتر این بیماری را که نیازی به درمان ندارد، 31 درصد و مصرف بالای غلات صبحانهای شیرین این درصد را به 38 درصد افزایش میدهد. پژوهشگران در تحقيقات اخير خود دريافتند: ميان آلرژي و خطر ابتلا به نوعي سرطان مغز رابطه مستقيم وجود دارد. اين مطالعات حاكي از آن است كه اين رابطه در زنان قويتر است، اگرچه خطر ابتلا به تومور مغزي در مردان با انواع خاص آلرژي نيز كمتر است. تومورهاي مغزي موسوم به glioma داراي پتانسل لازم جهت سركوب سيستم ايمني را دارا هستند. دانشمندان در اين پژوهش توانستند نمونههاي ذخيره شده خون بيماراني را كه دههها قبل از تشخيص ابتلا به تومور مزبور از آنها گرفته شده بود، تحليل كنند. آنها از نمونه خونهاي بانك جانوس سرم (Janus Serum) در نروژ استفاده كردند كه داراي نمونهخونهاي گردآوري شده از شهروندان طي سنجشهاي پزشكي سالانه يا اهداكنندگان خون در 40 سال گذشته است.
پژوهشگران در تحقيقات اخير خود دريافتند: ميان آلرژي و خطر ابتلا به نوعي سرطان مغز رابطه مستقيم وجود دارد. اين مطالعات حاكي از آن است كه اين رابطه در زنان قويتر است، اگرچه خطر ابتلا به تومور مغزي در مردان با انواع خاص آلرژي نيز كمتر است. تومورهاي مغزي موسوم به glioma داراي پتانسل لازم جهت سركوب سيستم ايمني را دارا هستند. دانشمندان در اين پژوهش توانستند نمونههاي ذخيره شده خون بيماراني را كه دههها قبل از تشخيص ابتلا به تومور مزبور از آنها گرفته شده بود، تحليل كنند. آنها از نمونه خونهاي بانك جانوس سرم (Janus Serum) در نروژ استفاده كردند كه داراي نمونهخونهاي گردآوري شده از شهروندان طي سنجشهاي پزشكي سالانه يا اهداكنندگان خون در 40 سال گذشته است. محققان مؤسسه سرطان دانشگاه پيتزبورگ با استفاده از يك تركيبي گياهي به نام فنيتيل ايزوتيوسيانات يا PEITC توانستند مانع از رشد تومورهاي پستاني در يك مدل موش مبتلا به سرطان پستان شوند. محققان به منظور تعيين اثربخشي PEITC بر روي تومورهاي پستاني موشها، آنها را تحت يك رژيم غذايي همراه با PEITC به مدت 29 هفته قرار دادند و سپس ارزيابيهاي آسيبشناسي، اندازه تومور و ميزان شيوع آن همراه با تكثير سلولي و آپوپتوزيس را بررسي كردند. نتايج حاصل از اين تحقيق نشان داد: تجويز فنيتيل ايزوتيوسيانات توانست تا 56.3 درصد رشد سرطان پستان در موشها را كاهش دهد.
محققان مؤسسه سرطان دانشگاه پيتزبورگ با استفاده از يك تركيبي گياهي به نام فنيتيل ايزوتيوسيانات يا PEITC توانستند مانع از رشد تومورهاي پستاني در يك مدل موش مبتلا به سرطان پستان شوند. محققان به منظور تعيين اثربخشي PEITC بر روي تومورهاي پستاني موشها، آنها را تحت يك رژيم غذايي همراه با PEITC به مدت 29 هفته قرار دادند و سپس ارزيابيهاي آسيبشناسي، اندازه تومور و ميزان شيوع آن همراه با تكثير سلولي و آپوپتوزيس را بررسي كردند. نتايج حاصل از اين تحقيق نشان داد: تجويز فنيتيل ايزوتيوسيانات توانست تا 56.3 درصد رشد سرطان پستان در موشها را كاهش دهد.  محققان نانوزنجیرهایی ساختهاند که قبل از تبدیل شدن سلولهای متاستاز به یک بافت جدید، روی آنها قرار گرفته و با استفاده از تصویربرداری تشدید مغناطیسی (MRI) محل آنها را شناسایی میکنند. سلولهای بدخیم که از تومور اولیه جدا میشوند، در کل بدن به شکلی غیرقابل کنترل پخش شده و با ایجاد تومورهای جدید در نقاط دیگر، موجب مرگ بیمار میشوند. حال گروهی از محققان دانشگاه «Case Western Reserve» روشی برای تشخیص این متاستازها در سرطان سینه موش یافتهاند که میتواند بسیار زودتر از روشهای فعلی، این سلولهای جابهجاشونده را شناسایی کند؛ با استفاده از این روش امکان تشخیص زودهنگام متاستاز و نجات بیماران سرطانی ایجاد میشود.
محققان نانوزنجیرهایی ساختهاند که قبل از تبدیل شدن سلولهای متاستاز به یک بافت جدید، روی آنها قرار گرفته و با استفاده از تصویربرداری تشدید مغناطیسی (MRI) محل آنها را شناسایی میکنند. سلولهای بدخیم که از تومور اولیه جدا میشوند، در کل بدن به شکلی غیرقابل کنترل پخش شده و با ایجاد تومورهای جدید در نقاط دیگر، موجب مرگ بیمار میشوند. حال گروهی از محققان دانشگاه «Case Western Reserve» روشی برای تشخیص این متاستازها در سرطان سینه موش یافتهاند که میتواند بسیار زودتر از روشهای فعلی، این سلولهای جابهجاشونده را شناسایی کند؛ با استفاده از این روش امکان تشخیص زودهنگام متاستاز و نجات بیماران سرطانی ایجاد میشود. محققان برای نخستین بار در انگلیس نوعی شیوه درمانی معرفی کردهاند که در آن کبد سرطانی را ایزوله میکنند در حالی که این عضو در حال گرفتن "حمام شیمیایی" است. این فرایند کبد را با دوز بالایی از شیمیدرمانی و بدون اثرگذاری بر سایر اندامهای بدن اشباع میکند. برایان استدمن این روش موسوم به CS-PHP را بر روی دو بیمار مبتلا به سرطان کبد به مدت 60 دقیقه با موفقیت آزمایش کرد.
محققان برای نخستین بار در انگلیس نوعی شیوه درمانی معرفی کردهاند که در آن کبد سرطانی را ایزوله میکنند در حالی که این عضو در حال گرفتن "حمام شیمیایی" است. این فرایند کبد را با دوز بالایی از شیمیدرمانی و بدون اثرگذاری بر سایر اندامهای بدن اشباع میکند. برایان استدمن این روش موسوم به CS-PHP را بر روی دو بیمار مبتلا به سرطان کبد به مدت 60 دقیقه با موفقیت آزمایش کرد.  مطالعات صورت گرفته توسط پژوهشگران آمریکایی نشان میدهد، والدینی که فرزندان خود را تنبیه می کنند یا بر سرآنها فریاد می زنند، کودکان خود را با ریسک بالای ابتلا به بیماری های مختلف از جمله سرطان و بیماری های قلبی مواجه میسازند. پژوهشگران روانشناسی دانشگاه پلیموت تأثیر تنبیه بدنی و رفتارهای خشن والدین با کودکان و احتمال بروز بیماری های مختلف را مورد مطالعه قرار داده اند. محققان تأکید می کنند، هرگونه تنبیه بدنی اعم از ضعیف یا شدید در دوران کودکی می تواند خطر ابتلا به بیماری های مختلف در آینده را افزایش دهد. تحقیقات جدید نشان می دهد، والدین با فریاد زدن بر سر کودکان یا تنبیه کردن آنها، فرزندان خود را در معرض مشکلات جدی سلامتی از جمله احتمال ابتلا به سرطان، بیماری های قلبی و آسم قرار می دهند.
مطالعات صورت گرفته توسط پژوهشگران آمریکایی نشان میدهد، والدینی که فرزندان خود را تنبیه می کنند یا بر سرآنها فریاد می زنند، کودکان خود را با ریسک بالای ابتلا به بیماری های مختلف از جمله سرطان و بیماری های قلبی مواجه میسازند. پژوهشگران روانشناسی دانشگاه پلیموت تأثیر تنبیه بدنی و رفتارهای خشن والدین با کودکان و احتمال بروز بیماری های مختلف را مورد مطالعه قرار داده اند. محققان تأکید می کنند، هرگونه تنبیه بدنی اعم از ضعیف یا شدید در دوران کودکی می تواند خطر ابتلا به بیماری های مختلف در آینده را افزایش دهد. تحقیقات جدید نشان می دهد، والدین با فریاد زدن بر سر کودکان یا تنبیه کردن آنها، فرزندان خود را در معرض مشکلات جدی سلامتی از جمله احتمال ابتلا به سرطان، بیماری های قلبی و آسم قرار می دهند. گروهی از پژوهشگران انجمن مهندسی و پژوهشی مواد «A*STAR» خانوادهای از رنگدانهها طراحی کردهاند که خاصیت فلورسانسی آنها با تودهای شدن افزایش مییابد. انتظار میرود نانوذرات فلورسانسی پرشده با رنگدانههای آلی گسیلنده نور، انقلابی در فناوریهای تصویربرداری زیستی ایجاد کنند. هنگامی که رنگدانههای متداول با غلظت زیاد همراه نانوذرات استفاده میشوند، به صورت توده درآمده و شدت گسیل خود را از دست میدهند. درون رنگدانههای متداول یک کروموفور (عامل رنگی مولکولی) تخت به نام دیسیانومتیلن اصلاح شده- تریفنیلآمین وجود دارد که در محلولهای رقیق نور قرمز گسیل میکند، ولی به هنگام تودهای شدن فلورسانس ضعیفی دارد.
گروهی از پژوهشگران انجمن مهندسی و پژوهشی مواد «A*STAR» خانوادهای از رنگدانهها طراحی کردهاند که خاصیت فلورسانسی آنها با تودهای شدن افزایش مییابد. انتظار میرود نانوذرات فلورسانسی پرشده با رنگدانههای آلی گسیلنده نور، انقلابی در فناوریهای تصویربرداری زیستی ایجاد کنند. هنگامی که رنگدانههای متداول با غلظت زیاد همراه نانوذرات استفاده میشوند، به صورت توده درآمده و شدت گسیل خود را از دست میدهند. درون رنگدانههای متداول یک کروموفور (عامل رنگی مولکولی) تخت به نام دیسیانومتیلن اصلاح شده- تریفنیلآمین وجود دارد که در محلولهای رقیق نور قرمز گسیل میکند، ولی به هنگام تودهای شدن فلورسانس ضعیفی دارد.  یافته محققان دانشگاه روچستر مبنی بر خودکشی سلولهای سرطانی در بدن موشهای کور، میتواند به ابداع روشهای درمانی جدید و مؤثر سرطان منجر شود. موشهای کور برهنه تنها پستاندار خونسرد محسوب میشوند که درد را احساس نمیکنند و مانند مورچه و زنبور، در اجتماعات بزرگ دارای سلسله مراتب ملکه و کارگر زندگی میکنند. پژوهشگران در سال 2011 دریافتند که موش کور Damaraland با کمک یک ژن خاص، قادر به توقف شکلگیری سلولهای سرطانی است. پیش از این تصور میشد که دو گونه دیگر موشهای کور نیز احتمالا دارای ژن هایی با همین خاصیت هستند، اما مطالعات جدید نشان می دهد، سلولهای سرطانی در بدن این موجودات به گونهای برنامهریزی شدهاند که در صورت خطرناک شدن دست به خودکشی میزنند.
یافته محققان دانشگاه روچستر مبنی بر خودکشی سلولهای سرطانی در بدن موشهای کور، میتواند به ابداع روشهای درمانی جدید و مؤثر سرطان منجر شود. موشهای کور برهنه تنها پستاندار خونسرد محسوب میشوند که درد را احساس نمیکنند و مانند مورچه و زنبور، در اجتماعات بزرگ دارای سلسله مراتب ملکه و کارگر زندگی میکنند. پژوهشگران در سال 2011 دریافتند که موش کور Damaraland با کمک یک ژن خاص، قادر به توقف شکلگیری سلولهای سرطانی است. پیش از این تصور میشد که دو گونه دیگر موشهای کور نیز احتمالا دارای ژن هایی با همین خاصیت هستند، اما مطالعات جدید نشان می دهد، سلولهای سرطانی در بدن این موجودات به گونهای برنامهریزی شدهاند که در صورت خطرناک شدن دست به خودکشی میزنند. تحقیقات حاکی از این است که بیماران مبتلا به نارسایی قلبی بیشتر در معرض ابتلا به سرطان قرار دارند.محققان امریکایی با بررسی 961 فرد مبتلا به نارسایی قلبی و پیگیری آن در طول بیش از شش سال دریافتند خطر ابتلا به سرطان در میان بیماران مبتلا به نارسایی قلبی بهطور قابل توجهی بالاتر از سایر افراد است. نتایج این تحقیق نشان میدهد: افرادی که از نارسایی قلبی رنج میبرند نزدیک به 60 درصد بیشتر در معرض خطر ابتلا به سرطان قرار دارند.
تحقیقات حاکی از این است که بیماران مبتلا به نارسایی قلبی بیشتر در معرض ابتلا به سرطان قرار دارند.محققان امریکایی با بررسی 961 فرد مبتلا به نارسایی قلبی و پیگیری آن در طول بیش از شش سال دریافتند خطر ابتلا به سرطان در میان بیماران مبتلا به نارسایی قلبی بهطور قابل توجهی بالاتر از سایر افراد است. نتایج این تحقیق نشان میدهد: افرادی که از نارسایی قلبی رنج میبرند نزدیک به 60 درصد بیشتر در معرض خطر ابتلا به سرطان قرار دارند. محققان «BWH» اولين گروهي هستند که طراحي منطقي دارو را با نانوشيمي ابرمولکولي ترکيب کرده و از آن در درمان سرطان استفاده کردهاند. شيمي ابرمولکولي به معني توليد سامانههاي پيچيده شيميايي با استفاده از واحدهاي ساختماني مولکولي است. محققان بيمارستان بريگام و زنان (BWH) از اين روشها براي ايجاد نانوذراتي استفاده کردهاند که در حين دارا بودن سميت پايين، فعاليت ضدتوموري بالايي روي سرطان سينه و رحم از خود نشان ميدهند. «شيلاديتيا سنگوپتا»، استاديار مهندسي زيستي «BWH» و نويسنده ارشد مقاله مربوط به اين کار ميگويد: اين کار فراتر از استفاده از فناوري نانو به عنوان حاملهاي رسانش دارو است و در حقيقت در حوزه مهندسي مجدد خود دارو و تبديل آن به نانودارو قرار ميگيرد.
محققان «BWH» اولين گروهي هستند که طراحي منطقي دارو را با نانوشيمي ابرمولکولي ترکيب کرده و از آن در درمان سرطان استفاده کردهاند. شيمي ابرمولکولي به معني توليد سامانههاي پيچيده شيميايي با استفاده از واحدهاي ساختماني مولکولي است. محققان بيمارستان بريگام و زنان (BWH) از اين روشها براي ايجاد نانوذراتي استفاده کردهاند که در حين دارا بودن سميت پايين، فعاليت ضدتوموري بالايي روي سرطان سينه و رحم از خود نشان ميدهند. «شيلاديتيا سنگوپتا»، استاديار مهندسي زيستي «BWH» و نويسنده ارشد مقاله مربوط به اين کار ميگويد: اين کار فراتر از استفاده از فناوري نانو به عنوان حاملهاي رسانش دارو است و در حقيقت در حوزه مهندسي مجدد خود دارو و تبديل آن به نانودارو قرار ميگيرد.  دانشمندان دانشگاه کالیفرنیا در ساندیگو در مراحل ابتدایی شیوهای هستند که از حبابهای درون حباب برای انتقال داروهای شیمیدرمانی استفاده کرده و میتواند در آینده به کاهش عوارض جانبی چشمگیر این شیوه درمانی منجر شود. عوارض جانبی رایجترین درمانهای شیمی درمانی از چگونگی عملکرد آنها نشات میگیرند. سلولها در زمان تکثیر خارج از کنترل سرطانی میشوند از این رو داروهای شیمیدرمانی تمام سلولهای حاضر در فرآیند تکثیر را هدف قرار داده و میکشند.
دانشمندان دانشگاه کالیفرنیا در ساندیگو در مراحل ابتدایی شیوهای هستند که از حبابهای درون حباب برای انتقال داروهای شیمیدرمانی استفاده کرده و میتواند در آینده به کاهش عوارض جانبی چشمگیر این شیوه درمانی منجر شود. عوارض جانبی رایجترین درمانهای شیمی درمانی از چگونگی عملکرد آنها نشات میگیرند. سلولها در زمان تکثیر خارج از کنترل سرطانی میشوند از این رو داروهای شیمیدرمانی تمام سلولهای حاضر در فرآیند تکثیر را هدف قرار داده و میکشند.  پژوهش محققان برزیلی نشان میدهد که زهر مار میتواند در مبارزه با سرطان پوست بسیار موثر واقع شود. محققان موسسه علمی «بوتان تان» برزیل طی گزارشی اعلام کردند پروتئین «کروماتین» که از زهر مار به دست میآید، میزان بقای موشهای مبتلا به سرطان پوست را 70 درصد افزایش میدهد. علاوه بر این، پروتئین مذکور به طور قابل توجهی گسترش تومورها را به تاخیر انداخته و حتی به طور کامل از تشکیل آنها جلوگیری میکند. محققان، طی این پژوهش بی سابقه همچنین کشف کردند که فعالیتهای سمی «کروماتین» در کشتن سلولها تنها منحصر به سلولهای ملانوم است و هیچ گونه آسیبی را به سایر سلولهای جاندار نمیرساند. گذشته از این، کروماتین تنها به مدت 24 ساعت در تومور سرطانی باقی میماند. پژوهشگران اظهار کردهاند که پیش از هرگونه اندیشه در رابطه با تولید دارویی جدید، باید آزمایشات دیگری روی سایر حیوانات و در نهایت بر سلولهای انسانی صورت گیرد. گرچه بنا بر این گزارش، پیش از انجام هر گونه آزمایش بر روی انسان، اولویت با سنتز و تولید کردن این پروتئین در محیط آزمایشگاه است، بدون این که زهر مار واقعی را مورد استفاده قرار دهیم.
پژوهش محققان برزیلی نشان میدهد که زهر مار میتواند در مبارزه با سرطان پوست بسیار موثر واقع شود. محققان موسسه علمی «بوتان تان» برزیل طی گزارشی اعلام کردند پروتئین «کروماتین» که از زهر مار به دست میآید، میزان بقای موشهای مبتلا به سرطان پوست را 70 درصد افزایش میدهد. علاوه بر این، پروتئین مذکور به طور قابل توجهی گسترش تومورها را به تاخیر انداخته و حتی به طور کامل از تشکیل آنها جلوگیری میکند. محققان، طی این پژوهش بی سابقه همچنین کشف کردند که فعالیتهای سمی «کروماتین» در کشتن سلولها تنها منحصر به سلولهای ملانوم است و هیچ گونه آسیبی را به سایر سلولهای جاندار نمیرساند. گذشته از این، کروماتین تنها به مدت 24 ساعت در تومور سرطانی باقی میماند. پژوهشگران اظهار کردهاند که پیش از هرگونه اندیشه در رابطه با تولید دارویی جدید، باید آزمایشات دیگری روی سایر حیوانات و در نهایت بر سلولهای انسانی صورت گیرد. گرچه بنا بر این گزارش، پیش از انجام هر گونه آزمایش بر روی انسان، اولویت با سنتز و تولید کردن این پروتئین در محیط آزمایشگاه است، بدون این که زهر مار واقعی را مورد استفاده قرار دهیم.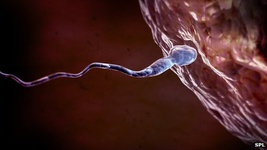 تحقیقات جدید دانشمندان بر روی میمونها نشان میدهد مردانی که بر اثر درمان سرطان در کودکی عقیم شدهاند ممکن است با استفاده از سلولهای بنیادی ذخیره شده روزی قادر به تولید اسپرمهای سالم باشند. شیمیدرمانی و پرتودرمانی میتوانند تومورها و سلولهای تولیدکننده اسپرم را نابود سازند. دانشمندان دانشگاه پترزبورگ و موسسه تحقیقاتی زنان مگی در آزمایشات خود، سلولهای بنیادی تولیدکننده اسپرم را قبل از درمان سرطان استخراج و آنها را در یک فریزر منجمد کردند و پس از اتمام روند درمان سرطان این اسپرمها را دوباره در بدن میمونها به کار بردند. طی این فرایند اسپرمهایی که قادر به بارور کردن تخمک بودند تولید شدند. محققان این اسپرمها را "مرحله برجسته" (milestone) نام نهادند.
تحقیقات جدید دانشمندان بر روی میمونها نشان میدهد مردانی که بر اثر درمان سرطان در کودکی عقیم شدهاند ممکن است با استفاده از سلولهای بنیادی ذخیره شده روزی قادر به تولید اسپرمهای سالم باشند. شیمیدرمانی و پرتودرمانی میتوانند تومورها و سلولهای تولیدکننده اسپرم را نابود سازند. دانشمندان دانشگاه پترزبورگ و موسسه تحقیقاتی زنان مگی در آزمایشات خود، سلولهای بنیادی تولیدکننده اسپرم را قبل از درمان سرطان استخراج و آنها را در یک فریزر منجمد کردند و پس از اتمام روند درمان سرطان این اسپرمها را دوباره در بدن میمونها به کار بردند. طی این فرایند اسپرمهایی که قادر به بارور کردن تخمک بودند تولید شدند. محققان این اسپرمها را "مرحله برجسته" (milestone) نام نهادند.  دانشمندان هلند در تلاش برای بررسی چگونگی گسترش سلولهای سرطانی دست به ابداع یک شیوه عجیب برای مشاهده رفتار آنها با کاشت پنجرههایی در شکم موشهای زنده زدهاند. این دریچههای شیشهیی که به طور مستقیم در دیواره شکم موشها بخیه شده قرار است به محققان موسسه زیستشناسی رشد و تحقیقات سلول بنیادی هوبرشت هلند در پیگیری چگونگی گسترش سلولهای سرطانی و شکلگیری تومورهای ثانویه کمک کند. این پدیده که به متاستاز تومور موسوم است در حال حاضر به خوبی درک نشده اما توزیع مرگبار این سلولها مسبب بیشتر مرگهای ناشی از سرطان است.
دانشمندان هلند در تلاش برای بررسی چگونگی گسترش سلولهای سرطانی دست به ابداع یک شیوه عجیب برای مشاهده رفتار آنها با کاشت پنجرههایی در شکم موشهای زنده زدهاند. این دریچههای شیشهیی که به طور مستقیم در دیواره شکم موشها بخیه شده قرار است به محققان موسسه زیستشناسی رشد و تحقیقات سلول بنیادی هوبرشت هلند در پیگیری چگونگی گسترش سلولهای سرطانی و شکلگیری تومورهای ثانویه کمک کند. این پدیده که به متاستاز تومور موسوم است در حال حاضر به خوبی درک نشده اما توزیع مرگبار این سلولها مسبب بیشتر مرگهای ناشی از سرطان است.  دانشمندان موفق به طراحي مچبندي شدهاند كه به فرد در خصوص آفتابسوختگي و احتمال ابتلا به سرطان پوست، هشدار بصري ميدهد. تاكنون 200 هزار مورد ملانوم بدخيم در سراسر جهان گزارش شده است. در اين بين محدود كردن قرارگيري در معرض نور خورشيد از اهميت شاياني برخوردار است. فناوري ارائه شده در دانشگاه استراتكلايد اسكاتلند با ارائه هشدار بصري در مورد يافتن سايه يا استفاده از كرم ضد آفتاب بيشتر از ميزان اين معضل كاسته است. اكنون دانشمندان اين دانشگاه مچبندي جديد طراحي كردهاند كه مجهز به يك عامل انتشار اسيد حساس به نور فرابنفش و يك رنگ است. اين رنگ به سطوح pH در نشانگر واكنش نشان ميدهد.
دانشمندان موفق به طراحي مچبندي شدهاند كه به فرد در خصوص آفتابسوختگي و احتمال ابتلا به سرطان پوست، هشدار بصري ميدهد. تاكنون 200 هزار مورد ملانوم بدخيم در سراسر جهان گزارش شده است. در اين بين محدود كردن قرارگيري در معرض نور خورشيد از اهميت شاياني برخوردار است. فناوري ارائه شده در دانشگاه استراتكلايد اسكاتلند با ارائه هشدار بصري در مورد يافتن سايه يا استفاده از كرم ضد آفتاب بيشتر از ميزان اين معضل كاسته است. اكنون دانشمندان اين دانشگاه مچبندي جديد طراحي كردهاند كه مجهز به يك عامل انتشار اسيد حساس به نور فرابنفش و يك رنگ است. اين رنگ به سطوح pH در نشانگر واكنش نشان ميدهد.