..:::: صندلی پزشکی دیجیتال با قابلیت بررسی فشار خون و علائم حیاتی بدن ::::..
![]() محققان صندلی پزشکی دیجیتالی طراحی کردهاند که با بررسی علائم حیاتی و وضعیت سلامت فرد، نیاز به مراجعه متعدد به مطب پزشک را بر طرف میکند. صندلی پزشکی دیجیتال Emperore1510 شرکت شارپ قادر به بررسی همزمان فشار خون، دمای بدن، ضربان قلب و علائم حیاتی فرد است. این صندلی مجهز به حسگرهای مختلفی است که گزارشی از وضعیت سلامت فرد را در حافظه ابری خود ذخیره میکند و در صورت لزوم توسط پزشک معالج قابل دسترسی خواهد بود.
محققان صندلی پزشکی دیجیتالی طراحی کردهاند که با بررسی علائم حیاتی و وضعیت سلامت فرد، نیاز به مراجعه متعدد به مطب پزشک را بر طرف میکند. صندلی پزشکی دیجیتال Emperore1510 شرکت شارپ قادر به بررسی همزمان فشار خون، دمای بدن، ضربان قلب و علائم حیاتی فرد است. این صندلی مجهز به حسگرهای مختلفی است که گزارشی از وضعیت سلامت فرد را در حافظه ابری خود ذخیره میکند و در صورت لزوم توسط پزشک معالج قابل دسترسی خواهد بود.
با کمک تجهیزات مختلف تعبیه شده بر روی این صندلی پزشکی هوشمند، نیاز به استفاده از دستگاههای مختلف برای بررسی علائم حیاتی بر طرف میشود. سه صفحه نمایش در قسمت بالای صندلی نصب شده است که وضعیت بررسی علائم حیاتی در حال اسکن را به فرد نشان میدهد. دستگاه اندازهگیری فشار خون بر روی دسته سمت راست صندلی قرار داده شده و در بخش چپ صندلی نیز محلی برای قرار گرفتن انگشت برای اندازهگیری ضربان قلب و دمای بدن در نظر گرفته شده است.
با کمک صندلی پزشکی Emperore1510 امکان اسکن و ضبط وضعیت سلامت افراد در کوتاهترین زمان، شناسایی نشانههای اولیه بیماری، تسریع تداخل پزشک در روند درمانی و در نتیجه کاهش طول درمان فراهم میشود. این فناوری در نمایشگاه CEATEC2013 به نمایش گذاشته شده و با قیمت نسبتا بالای پنج هزار و 950 دلار به بازار عرضه میشود.
 پژوهشها بر روی بیماران سرطانی نشان میدهد: 70 درصد بیماران پس از درمان، احساس متفاوتی نسبت به طعم و مزه غذاها دارند. محققان موسسه پلیتکنیک فرانسه عادات غذایی 160 بیمار سرطانی را مورد بررسی قرار دادند. بر اساس یافتههای این تحقیق عوارض ناشی از بیماری و فرایند درمان، باعث ایجاد برخی حساسیتها نسبت به مواد غذایی میشود. برای مثال در اثر سوزش یا خشکی دهان و خستگی، 67 درصد بیماران گرایش به خوردن غذاهای میکس شده دارند که خوردن آن راحتتر است.
پژوهشها بر روی بیماران سرطانی نشان میدهد: 70 درصد بیماران پس از درمان، احساس متفاوتی نسبت به طعم و مزه غذاها دارند. محققان موسسه پلیتکنیک فرانسه عادات غذایی 160 بیمار سرطانی را مورد بررسی قرار دادند. بر اساس یافتههای این تحقیق عوارض ناشی از بیماری و فرایند درمان، باعث ایجاد برخی حساسیتها نسبت به مواد غذایی میشود. برای مثال در اثر سوزش یا خشکی دهان و خستگی، 67 درصد بیماران گرایش به خوردن غذاهای میکس شده دارند که خوردن آن راحتتر است.  مردانی که بیش از اندازه مینشینند، در معرض خطر پولیپ روده قرار دارند؛ حتی اگر این افراد در طول نشستن وقفه ایجاد کنند و فعالیتهای تفریحی مانند پیاده روی و دویدن نرم داشته باشند و یا گلف بازی کنند. محققان امریکایی میزان فعالیت 1700 مرد و زن را مورد بررسی قرار دادند. آنان دریافتند سبک زندگی مردان آرامتر آنان را در معرض خطر بیشتر پولیپهای پیش سرطانی قرار میدهد. مردانی که 11 ساعت یا بیشتر در طول روز نشسته بسر میبرند، مانند زمان نوشتن و یا خواندن، 45 درصد بیشتر از افرادی که 7 ساعت و یا کمتر مینشینند در معرض خطر هستند.
مردانی که بیش از اندازه مینشینند، در معرض خطر پولیپ روده قرار دارند؛ حتی اگر این افراد در طول نشستن وقفه ایجاد کنند و فعالیتهای تفریحی مانند پیاده روی و دویدن نرم داشته باشند و یا گلف بازی کنند. محققان امریکایی میزان فعالیت 1700 مرد و زن را مورد بررسی قرار دادند. آنان دریافتند سبک زندگی مردان آرامتر آنان را در معرض خطر بیشتر پولیپهای پیش سرطانی قرار میدهد. مردانی که 11 ساعت یا بیشتر در طول روز نشسته بسر میبرند، مانند زمان نوشتن و یا خواندن، 45 درصد بیشتر از افرادی که 7 ساعت و یا کمتر مینشینند در معرض خطر هستند.  بر اساس یافتههای پژوهشی جدید احتمال ابتلا به بیماریهای قلبی و یائسگی زودرس در بیماران مبتلا به آرتریت روماتوئید یا روماتیسم مفصلی بیشتر است. اریک متسون، یکی از نویسندگان این تحقیق و پزشک کلینیک مایو در روچستر آمریکا اظهار کرد: فشار بسیاری که در سال اول ابتلا به روماتیسم مفصلی بر مفاصل وارد میشود، باعث افزایش خطر ابتلا به بیماری قلبی میشود و به نظر میرسد اگر این فشار کاهش یابد، از میزان خطر ابتلا به بیماری قلبی نیز کاسته میشود.
بر اساس یافتههای پژوهشی جدید احتمال ابتلا به بیماریهای قلبی و یائسگی زودرس در بیماران مبتلا به آرتریت روماتوئید یا روماتیسم مفصلی بیشتر است. اریک متسون، یکی از نویسندگان این تحقیق و پزشک کلینیک مایو در روچستر آمریکا اظهار کرد: فشار بسیاری که در سال اول ابتلا به روماتیسم مفصلی بر مفاصل وارد میشود، باعث افزایش خطر ابتلا به بیماری قلبی میشود و به نظر میرسد اگر این فشار کاهش یابد، از میزان خطر ابتلا به بیماری قلبی نیز کاسته میشود.  محققان آزمایش بالینی داروی آنتیبادی جدیدی را آغاز کردهاند که قادر به هدف قرار دادن اختصاصی سلولهای سرطانی است. محققان دانشکده علوم بیوپزشکی دانشگاه موناش به سرپرستی پروفسور «مارتین لکمان» موفق به شناسایی نشانگری بر روی سلولهای بنیادی لوکمی شده اند که داروی جدید ضد سرطان به این نشانگر متصل میشود.
محققان آزمایش بالینی داروی آنتیبادی جدیدی را آغاز کردهاند که قادر به هدف قرار دادن اختصاصی سلولهای سرطانی است. محققان دانشکده علوم بیوپزشکی دانشگاه موناش به سرپرستی پروفسور «مارتین لکمان» موفق به شناسایی نشانگری بر روی سلولهای بنیادی لوکمی شده اند که داروی جدید ضد سرطان به این نشانگر متصل میشود. 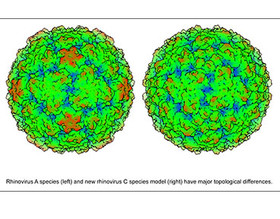 دانشمندان دانشگاه ویسکانسین منسون موفق به ساخت یک مدل سهبعدی از عامل بیماریزایی شدهاند که نشان میدهد چرا درمانی برای سرماخوردگی وجود ندارد. این محققان یک مدل توپوگرافی دقیق از کپسید یا پوسته پروتئین یک ویروس سرماخوردگی را ارائه کردهاند که تا سال 2006 برای علم ناشناخته باقی مانده بود.
دانشمندان دانشگاه ویسکانسین منسون موفق به ساخت یک مدل سهبعدی از عامل بیماریزایی شدهاند که نشان میدهد چرا درمانی برای سرماخوردگی وجود ندارد. این محققان یک مدل توپوگرافی دقیق از کپسید یا پوسته پروتئین یک ویروس سرماخوردگی را ارائه کردهاند که تا سال 2006 برای علم ناشناخته باقی مانده بود.  تحقیقات محققان ایتالیایی نشان میدهد مصرف قهوه 40 تا 50 درصد خطر ابتلا به سرطان کبد را کاهش میدهد. از سال 2007 محققان در تلاشند تا دریابند آیا قهوه از بروز سرطان کبد پیشگیری میکند؟ نتایج تحقیقات چندگانه و متعدد در این زمینه نشان میدهد که قهوه برای پیشگیری از این نوع سرطان مفید است. با وجود پژوهشهای متعدد در گذشته، محققان ایتالیایی برای به روز رسانی تحقیقات در این زمینه اقدام کردند. به همین منظور محققان دانشگاه میلان نتایج 16 پژوهش برتر از سال 1996 تا سپتامبر 2012 را که بر روی بیش از سه هزار بیمار انجام شده بود، مورد بررسی قرار دادند. سرطان کبد ششمین سرطان رایج در دنیاست که عفونتهای خونی ناشی از ویروس هپاتیت B و C اصلیترین عامل ابتلا به این بیماری است. از دیگر عوامل موثر در بروز سرطان کبد میتوان به مصرف الکل، سیگار کشیدن، چاقی و دیابت اشاره کرد. به گفته محققان ایتالیایی مصرف روزانه سه فنجان قهوه تا 50 درصد خطر ابتلا به سرطان کبد را کاهش میدهد و برای حفظ سلامتی مفید است.
تحقیقات محققان ایتالیایی نشان میدهد مصرف قهوه 40 تا 50 درصد خطر ابتلا به سرطان کبد را کاهش میدهد. از سال 2007 محققان در تلاشند تا دریابند آیا قهوه از بروز سرطان کبد پیشگیری میکند؟ نتایج تحقیقات چندگانه و متعدد در این زمینه نشان میدهد که قهوه برای پیشگیری از این نوع سرطان مفید است. با وجود پژوهشهای متعدد در گذشته، محققان ایتالیایی برای به روز رسانی تحقیقات در این زمینه اقدام کردند. به همین منظور محققان دانشگاه میلان نتایج 16 پژوهش برتر از سال 1996 تا سپتامبر 2012 را که بر روی بیش از سه هزار بیمار انجام شده بود، مورد بررسی قرار دادند. سرطان کبد ششمین سرطان رایج در دنیاست که عفونتهای خونی ناشی از ویروس هپاتیت B و C اصلیترین عامل ابتلا به این بیماری است. از دیگر عوامل موثر در بروز سرطان کبد میتوان به مصرف الکل، سیگار کشیدن، چاقی و دیابت اشاره کرد. به گفته محققان ایتالیایی مصرف روزانه سه فنجان قهوه تا 50 درصد خطر ابتلا به سرطان کبد را کاهش میدهد و برای حفظ سلامتی مفید است.  خواب نیمروزی کوتاه به افزایش انرژی و هوشیاری در طول روز کمک میکند، اما افرادی که خواب نیمروزی طولانی مدت دارند در معرض خطر ابتلا به دیابت قرار دارند. این تحقیق توسط متخصصان خواب مرکز پزشکی دانشگاه لیدن در هلند انجام شده است. در این تحقیق 27 هزار زن و مرد چینی که بیش از یک ساعت خواب نیمروزی داشتند و احتمال اختلالات متابولیسم در این افراد وجود داشت، شرکت کردند.
خواب نیمروزی کوتاه به افزایش انرژی و هوشیاری در طول روز کمک میکند، اما افرادی که خواب نیمروزی طولانی مدت دارند در معرض خطر ابتلا به دیابت قرار دارند. این تحقیق توسط متخصصان خواب مرکز پزشکی دانشگاه لیدن در هلند انجام شده است. در این تحقیق 27 هزار زن و مرد چینی که بیش از یک ساعت خواب نیمروزی داشتند و احتمال اختلالات متابولیسم در این افراد وجود داشت، شرکت کردند.  محققان دانشگاه مینهسوتا با استفاده از نانوذرات به عنوان حامل، عوارض ماده شیمیایی TNF-a را که میتواند رگهای خونی اطراف تومور را از بین ببرد، به حداقل رساندهاند. در سالهای اخیر محققان موفق شدند روشی برای از بین بردن رگهای پیرامون تومورها پیدا کنند با این کار میتوان تومورها را از بین برد. برای این کار از مواد شیمیایی مختلف استفاده میشود. یکی از این ترکیبات کاچکسین یا TNF-a است که نتایج بسیار خوبی داده است، مشکل این ماده سمی بودن آن است که میتواند عوارض جانبی داشته باشد. برای کاهش سمیت این ماده میتوان از نانوذرات طلا استفاده کرد. این نانوذرات میتوانند به عنوان حامل این ماده دارو را در محل مورد نظر رهاسازی کنند. این فرآیند فاز اول تست بالینی را پشت سر گذاشته است.
محققان دانشگاه مینهسوتا با استفاده از نانوذرات به عنوان حامل، عوارض ماده شیمیایی TNF-a را که میتواند رگهای خونی اطراف تومور را از بین ببرد، به حداقل رساندهاند. در سالهای اخیر محققان موفق شدند روشی برای از بین بردن رگهای پیرامون تومورها پیدا کنند با این کار میتوان تومورها را از بین برد. برای این کار از مواد شیمیایی مختلف استفاده میشود. یکی از این ترکیبات کاچکسین یا TNF-a است که نتایج بسیار خوبی داده است، مشکل این ماده سمی بودن آن است که میتواند عوارض جانبی داشته باشد. برای کاهش سمیت این ماده میتوان از نانوذرات طلا استفاده کرد. این نانوذرات میتوانند به عنوان حامل این ماده دارو را در محل مورد نظر رهاسازی کنند. این فرآیند فاز اول تست بالینی را پشت سر گذاشته است.  محققان مؤسسه تحقیقات کاربردی پلیمر فرانهوفر آلمان شیوه جدیدی ابداع کردهاند که به نمایش مواد حاوی نانوذرات با قابلیت کشتن انتخابی سلولهای تومور میپردازد. محققان از آبگریزها یا وزیکولهای چربی نامحلول در آب به عنوان حاملهای دارویی کوچک 200 تا 250 نانومتری استفاده کردند. این حاملها از لحاظ زیستی در بدن پس از استقرار قابل تخریب و تجزیه هستند. از پلیمرها برای تثبیت نانوپوشش استفاده میشود که از مولکولهای بسیار خاص و به رسمیت شناخته شده توسط سلولهای تومور برخوردارند. این پوشش نانوذرات که متخصصان آن را ویزکول مینامند، از ساختاری شبیه سلول برخوردارند.
محققان مؤسسه تحقیقات کاربردی پلیمر فرانهوفر آلمان شیوه جدیدی ابداع کردهاند که به نمایش مواد حاوی نانوذرات با قابلیت کشتن انتخابی سلولهای تومور میپردازد. محققان از آبگریزها یا وزیکولهای چربی نامحلول در آب به عنوان حاملهای دارویی کوچک 200 تا 250 نانومتری استفاده کردند. این حاملها از لحاظ زیستی در بدن پس از استقرار قابل تخریب و تجزیه هستند. از پلیمرها برای تثبیت نانوپوشش استفاده میشود که از مولکولهای بسیار خاص و به رسمیت شناخته شده توسط سلولهای تومور برخوردارند. این پوشش نانوذرات که متخصصان آن را ویزکول مینامند، از ساختاری شبیه سلول برخوردارند. 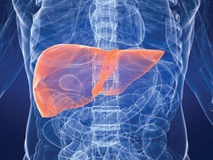 محققان دانشگاه بینالمللی سنگاپور طی پژوهشی دریافتند فعال کردن خانوادهای از پروتئین خاص کوچک موسوم به "Rho" میتواند سرطان کبد را سرکوب کند. این برای نخستین بار است که محققان توانستهاند شواهدی را مبنی بر تاثیر سیگنال دهی مخابراتی بین سوئیچهای پروتئین متفاوت بر توسعه بافت سرطانی نشان دهند.
محققان دانشگاه بینالمللی سنگاپور طی پژوهشی دریافتند فعال کردن خانوادهای از پروتئین خاص کوچک موسوم به "Rho" میتواند سرطان کبد را سرکوب کند. این برای نخستین بار است که محققان توانستهاند شواهدی را مبنی بر تاثیر سیگنال دهی مخابراتی بین سوئیچهای پروتئین متفاوت بر توسعه بافت سرطانی نشان دهند.  افزایش وزن معمولا یکی از عوارض بیماری کمکاری تیروئید است، اما نتایج تحقیقات جدید نشان میدهد درمان این بیماری کمکی به کاهش وزن نمیکند. یافتههای پژوهشی جدید حاکی از آن است که درمان کمکاری تیروئید با استفاده از لووتیروکسین باعث کاهش وزن چشمگیری در افراد مبتلا به این بیماری نمیشود. لووتیروکسین دارویی است که از طریق بازگرداندن میزان طبیعی هورمون تیروئید در درمان کمکاری تیروئید به کار میرود. محققان برای انجام این تحقیق در طول هشت سال اطلاعات مربوط به بیمارانی را که کمکاری تیروئید در آنان تشخیص داده شده بود، بررسی کردند.
افزایش وزن معمولا یکی از عوارض بیماری کمکاری تیروئید است، اما نتایج تحقیقات جدید نشان میدهد درمان این بیماری کمکی به کاهش وزن نمیکند. یافتههای پژوهشی جدید حاکی از آن است که درمان کمکاری تیروئید با استفاده از لووتیروکسین باعث کاهش وزن چشمگیری در افراد مبتلا به این بیماری نمیشود. لووتیروکسین دارویی است که از طریق بازگرداندن میزان طبیعی هورمون تیروئید در درمان کمکاری تیروئید به کار میرود. محققان برای انجام این تحقیق در طول هشت سال اطلاعات مربوط به بیمارانی را که کمکاری تیروئید در آنان تشخیص داده شده بود، بررسی کردند.  محققان در لندن برای اولین بار موفق به اجرای یک شیوه پیشگامانه پیوند مغز استخوان بر روی انسان شدهاند. به گفته محققان، این روش میتواند به مشکل کمبود اهداکننده کمک کند؛ چراکه نیازمند تطابق کامل سلولی نیست. محمد احمد پنج ساله در میان سه کودکی است که برای اولین بار در جهان این درمان جدید را انجام میدهند. محمد به سندرم نقص ایمنی ترکیبی شدید مبتلا بوده و چند سال است که منتظر یک اهداکننده مناسب است.
محققان در لندن برای اولین بار موفق به اجرای یک شیوه پیشگامانه پیوند مغز استخوان بر روی انسان شدهاند. به گفته محققان، این روش میتواند به مشکل کمبود اهداکننده کمک کند؛ چراکه نیازمند تطابق کامل سلولی نیست. محمد احمد پنج ساله در میان سه کودکی است که برای اولین بار در جهان این درمان جدید را انجام میدهند. محمد به سندرم نقص ایمنی ترکیبی شدید مبتلا بوده و چند سال است که منتظر یک اهداکننده مناسب است.  محققان مرکز پزشکی دانشگاه راش واقع در شیکاگو دریافتند عملکرد کبد در انسان های چاق منجر به زوال عقل و اختلال حافظه می شود. محققان دانشگاه راش در تحقیقی دریافتند که کبد انسان برای سوزاندن چربی موجود در شکم و سایر اندام ها از نوعی پروتئین موسوم به PPARalpha استفاده می کند؛ این در حالی است که بخش هیپوکمپوس مغز نیز برای پردازش حافظه و یادگیری از همین پروتئین بهره می برد. در بدن افرادی که دچار چاقی مفرط هستند، کبد پروتئین PPARalpha را ابتدا از اندام های مجاور و سپس از کل اندام های بدن جمع آوری می کند و برای سوزاندن چربی اضافه به کار می گیرد. بدین ترتیب هیپوکمپوس برای پردازش حافظه به میزان کافی این پروتئین را در اختیار نخواهد داشت و فرآیند یادگیری و یادآوری شخص با اختلال مواجه می شود.
محققان مرکز پزشکی دانشگاه راش واقع در شیکاگو دریافتند عملکرد کبد در انسان های چاق منجر به زوال عقل و اختلال حافظه می شود. محققان دانشگاه راش در تحقیقی دریافتند که کبد انسان برای سوزاندن چربی موجود در شکم و سایر اندام ها از نوعی پروتئین موسوم به PPARalpha استفاده می کند؛ این در حالی است که بخش هیپوکمپوس مغز نیز برای پردازش حافظه و یادگیری از همین پروتئین بهره می برد. در بدن افرادی که دچار چاقی مفرط هستند، کبد پروتئین PPARalpha را ابتدا از اندام های مجاور و سپس از کل اندام های بدن جمع آوری می کند و برای سوزاندن چربی اضافه به کار می گیرد. بدین ترتیب هیپوکمپوس برای پردازش حافظه به میزان کافی این پروتئین را در اختیار نخواهد داشت و فرآیند یادگیری و یادآوری شخص با اختلال مواجه می شود.  محققان دانشکده پزشکی هاروارد موفق به ساخت ایمپلنتی شده اند که با استفاده از نور، دیابت را درمان می کند. این ایمپلنت درمانی که به صورت یک ژل شفاف است، از تعداد زیادی سلول حساس به نور تشکیل شده است که از نظر ژنتیکی اصلاح شده اند. نور یک ابزار عالی برای ارتباط با سیستم های بیولوژیک است، ولی هنگام استفاده از آن یک مشکل اساسی وجود دارد؛ نور هنگام برخورد با بافت های بدن و عبور از آن پراکنده می شود که ایمپلنت ژله مانند این مشکل را حل کرده است و باعث تمرکز نور می شود.
محققان دانشکده پزشکی هاروارد موفق به ساخت ایمپلنتی شده اند که با استفاده از نور، دیابت را درمان می کند. این ایمپلنت درمانی که به صورت یک ژل شفاف است، از تعداد زیادی سلول حساس به نور تشکیل شده است که از نظر ژنتیکی اصلاح شده اند. نور یک ابزار عالی برای ارتباط با سیستم های بیولوژیک است، ولی هنگام استفاده از آن یک مشکل اساسی وجود دارد؛ نور هنگام برخورد با بافت های بدن و عبور از آن پراکنده می شود که ایمپلنت ژله مانند این مشکل را حل کرده است و باعث تمرکز نور می شود. یافتههای پژوهشی جدید نشان میدهد مصرف مکملهای ویتامین D خطر ابتلا به سنگ کلیه را افزایش نمیدهد. بر اساس نتایج این پژوهش جدید، مصرف مکملهای ویتامین D باعث افزایش خطر احتمال ابتلا به سنگ کلیه نمیشود بلکه سن افراد، جنسیت و وزن ممکن است در این امر تاثیر بسزایی داشته باشند.
یافتههای پژوهشی جدید نشان میدهد مصرف مکملهای ویتامین D خطر ابتلا به سنگ کلیه را افزایش نمیدهد. بر اساس نتایج این پژوهش جدید، مصرف مکملهای ویتامین D باعث افزایش خطر احتمال ابتلا به سنگ کلیه نمیشود بلکه سن افراد، جنسیت و وزن ممکن است در این امر تاثیر بسزایی داشته باشند.  تحقیقات جدید شواهد بیشتری از ارتباط بین سلامت قلب، دهان و دندان را ارائه میدهند. استاتین با دوز بالا میتواند التهاب لثه را در بیماران مبتلا به بیماری قلب پس از چهار هفته کاهش دهد. محققان امریکایی با اشاره به نتایج حاصل از پژوهش انجام شده میگویند: استاتین معمولا برای کاهش کلسترول خون تجویز میشود. اگر چه ما به مقداری کلسترول برای حفظ سلامت نیاز داریم، ولی مصرف بیش از حد از مواد چرب باعث گرفتگی سرخرگها و تصلب شرایین شده که منجر به حملات قلبی، سکته مغزی و بیماری عروق محیطی میشود.
تحقیقات جدید شواهد بیشتری از ارتباط بین سلامت قلب، دهان و دندان را ارائه میدهند. استاتین با دوز بالا میتواند التهاب لثه را در بیماران مبتلا به بیماری قلب پس از چهار هفته کاهش دهد. محققان امریکایی با اشاره به نتایج حاصل از پژوهش انجام شده میگویند: استاتین معمولا برای کاهش کلسترول خون تجویز میشود. اگر چه ما به مقداری کلسترول برای حفظ سلامت نیاز داریم، ولی مصرف بیش از حد از مواد چرب باعث گرفتگی سرخرگها و تصلب شرایین شده که منجر به حملات قلبی، سکته مغزی و بیماری عروق محیطی میشود.  تحقیقات حاکی از آن است که نوعی پروتئین در صفرا در تشخیص سرطان پانکراس موثر است. تحقیقات نشان میدهد که این روش میتواند از آزمایش خون هم بهتر عمل کند و در تشخیص زودهنگام این سرطان موثر باشد. بر اساس مطالعات جدید نوعی پروتئین در صفرا در شناسایی سرطان لوزالمعده نیز موثر است. محققان دریافتند که این نشانگر که عروق عامل رشد اندوتلیال (VEGF) نامیده میشود، در 93 درصد موارد به شناسایی سرطان لوزالمعده کمک میکند. بیماران مبتلا به سرطان پانکراس یا مجرای صفراوی معمولا انسداد مجرای صفرا و یرقان دارند. محققان افزودند: انسداد مجرای صفراوی از نشانههای غیرسرطانی مانند سنگ مجرای صفراوی هم ناشی میشود. انسداد مجرای صفراوی انسداد در لولههای حمل کننده صفرا از کبد به کیسه صفرا و روده کوچک است. صفرا به هضم کمک میکند.
تحقیقات حاکی از آن است که نوعی پروتئین در صفرا در تشخیص سرطان پانکراس موثر است. تحقیقات نشان میدهد که این روش میتواند از آزمایش خون هم بهتر عمل کند و در تشخیص زودهنگام این سرطان موثر باشد. بر اساس مطالعات جدید نوعی پروتئین در صفرا در شناسایی سرطان لوزالمعده نیز موثر است. محققان دریافتند که این نشانگر که عروق عامل رشد اندوتلیال (VEGF) نامیده میشود، در 93 درصد موارد به شناسایی سرطان لوزالمعده کمک میکند. بیماران مبتلا به سرطان پانکراس یا مجرای صفراوی معمولا انسداد مجرای صفرا و یرقان دارند. محققان افزودند: انسداد مجرای صفراوی از نشانههای غیرسرطانی مانند سنگ مجرای صفراوی هم ناشی میشود. انسداد مجرای صفراوی انسداد در لولههای حمل کننده صفرا از کبد به کیسه صفرا و روده کوچک است. صفرا به هضم کمک میکند.  گاهی اوقات عفونت توسط کاتر به بیماران مبتلا به نارسایی کلیه که تحت درمان دیالیز قرار دارند، منتقل میشود. این عفونتها با آنتیبیوتیک درمان میشود اما عسل میتواند جایگزینی موثر در درمان باشد. در تحقیق جدید انجام شده مشخص شد استفاده از عسل در زخمهای ناشی از کاتر در بیماران دیالیزی موثرتر از مصرف آنتیبیوتیک در جلوگیری از عفونت دیالیز صفاقی (دیالیز از طریق لوله در شکم) است. محقق این تحقیق «دیوید جانسون» از دانشگاه کوئیزلند و بیمارستان پرنسس الکساندرا استرالیا اظهار کرد: برخی از بیماران از استعمال روزانه عسل بر زخم احساس خوشایندی ندارند. این زخمها تهدیدکننده زندگی است و درمان آنتیبیوتیکی میشوند، اما آنتیبیوتیک در درمان برخی از عفونتها موثر است و مصرف بیش از حد آن مقاومت میکروبی در برابر آنتی بیوتیک ایجاد میکند.
گاهی اوقات عفونت توسط کاتر به بیماران مبتلا به نارسایی کلیه که تحت درمان دیالیز قرار دارند، منتقل میشود. این عفونتها با آنتیبیوتیک درمان میشود اما عسل میتواند جایگزینی موثر در درمان باشد. در تحقیق جدید انجام شده مشخص شد استفاده از عسل در زخمهای ناشی از کاتر در بیماران دیالیزی موثرتر از مصرف آنتیبیوتیک در جلوگیری از عفونت دیالیز صفاقی (دیالیز از طریق لوله در شکم) است. محقق این تحقیق «دیوید جانسون» از دانشگاه کوئیزلند و بیمارستان پرنسس الکساندرا استرالیا اظهار کرد: برخی از بیماران از استعمال روزانه عسل بر زخم احساس خوشایندی ندارند. این زخمها تهدیدکننده زندگی است و درمان آنتیبیوتیکی میشوند، اما آنتیبیوتیک در درمان برخی از عفونتها موثر است و مصرف بیش از حد آن مقاومت میکروبی در برابر آنتی بیوتیک ایجاد میکند.  محققان دانشگاه ییل دریافتهاند ژنی که خون را از وجود سرطان مصون میدارد، توسط ذرات ریز RNA کنترل میشود؛ این یافته میتواند راهها و حتی درمانهای جدیدی را برای تشخیص سرطان خون پیش رو بگذارد. محققان چند سال پیش متوجه نقش اساسی ژن "TET2" در حفظ سلامت سلولهای خونی شدند. جهشهای این ژن، در حدود 20 درصد سرطانهای خون مشاهده شده بود و باور بر این میرفت که در 80 درصد بیماران، این ژن با سرطان خون مرتبط نیست و در نتیجه به عنوان شاخص ضعیفی در تشخیص این بیماری در نظر گرفته میشد.
محققان دانشگاه ییل دریافتهاند ژنی که خون را از وجود سرطان مصون میدارد، توسط ذرات ریز RNA کنترل میشود؛ این یافته میتواند راهها و حتی درمانهای جدیدی را برای تشخیص سرطان خون پیش رو بگذارد. محققان چند سال پیش متوجه نقش اساسی ژن "TET2" در حفظ سلامت سلولهای خونی شدند. جهشهای این ژن، در حدود 20 درصد سرطانهای خون مشاهده شده بود و باور بر این میرفت که در 80 درصد بیماران، این ژن با سرطان خون مرتبط نیست و در نتیجه به عنوان شاخص ضعیفی در تشخیص این بیماری در نظر گرفته میشد.  مطالعات اخير محققان دانشگاه آرهوس دانمارك نشان مي دهد كه برخلاف تصور عموم، زندگي در مزرعه و محيط هاي كشاورزي در پيشگيري از آلرژي و تعديل و درمان آن موثر است. زماني كه بيماران مبتلا به انواع آلرژي در محيط هاي كشاورزي و مزارع زندگي مي كنند، علايم حساسيت و آلرژي آنان به ميزان قابل توجهي كاهش پيدا مي كند. سيستم ايمني افرادي كه در مزارع زندگي و فعاليت مي كنند، غالبا در معرض طيف گسترده اي از باكتري ها، قارچ ها، گرده ها و ساير مواد محرك قرار مي گيرد. تمام اين عوامل پاسخ بدن را تحريك مي كند و بدن را درمقابل حساسيت ايمن مي كند.
مطالعات اخير محققان دانشگاه آرهوس دانمارك نشان مي دهد كه برخلاف تصور عموم، زندگي در مزرعه و محيط هاي كشاورزي در پيشگيري از آلرژي و تعديل و درمان آن موثر است. زماني كه بيماران مبتلا به انواع آلرژي در محيط هاي كشاورزي و مزارع زندگي مي كنند، علايم حساسيت و آلرژي آنان به ميزان قابل توجهي كاهش پيدا مي كند. سيستم ايمني افرادي كه در مزارع زندگي و فعاليت مي كنند، غالبا در معرض طيف گسترده اي از باكتري ها، قارچ ها، گرده ها و ساير مواد محرك قرار مي گيرد. تمام اين عوامل پاسخ بدن را تحريك مي كند و بدن را درمقابل حساسيت ايمن مي كند.  تحقیقات جدید محققان دانشگاه پوردوی آمریکا نشان میدهد: مصرف روزانه بادام برشته شده منجر به کاهش گرسنگی بدون افزایش وزن میشود. این تحقیق در زمینه تاثیر میان وعده بادام بر اشتها و وزن انجام شده است. شرکتکنندگان این تحقیق با خوردن سه قاشق غذاخوری بادام برشتهشده کم نمک میزان ویتامین E و چربی اشباع نشده (چربی خوب) رژیم غذایی خود را افزایش دادند. در حال حاضر مصرف میان وعده عمومیت یافته است و حداقل روزانه یک میان وعده سرو میشود. افزایش مقدار میان وعده موجب چاقی و کمبود مواد غذایی مغذی میشود و دقت در انتخاب میانوعده مناسب برای سلامتی مفید است و خطر افزایش وزن را کاهش میدهد.
تحقیقات جدید محققان دانشگاه پوردوی آمریکا نشان میدهد: مصرف روزانه بادام برشته شده منجر به کاهش گرسنگی بدون افزایش وزن میشود. این تحقیق در زمینه تاثیر میان وعده بادام بر اشتها و وزن انجام شده است. شرکتکنندگان این تحقیق با خوردن سه قاشق غذاخوری بادام برشتهشده کم نمک میزان ویتامین E و چربی اشباع نشده (چربی خوب) رژیم غذایی خود را افزایش دادند. در حال حاضر مصرف میان وعده عمومیت یافته است و حداقل روزانه یک میان وعده سرو میشود. افزایش مقدار میان وعده موجب چاقی و کمبود مواد غذایی مغذی میشود و دقت در انتخاب میانوعده مناسب برای سلامتی مفید است و خطر افزایش وزن را کاهش میدهد.  تحقیقات دانشگاهی در لندن حاکی از آن است که آنتی اکسیدان موجود در گریپ فروت و سایر مرکبات از تشکیل کیست در کلیهها جلوگیری میکند. براساس نتایج این تحقیقات که در مجله بریتانیایی فارموکولوژی به چاپ رسیده، مادهای به نام نارنژنین که در گریپ فروت و سایر مرکبات وجود دارد، قادر است تشکیل کیست در کلیه را متوقف سازد.
تحقیقات دانشگاهی در لندن حاکی از آن است که آنتی اکسیدان موجود در گریپ فروت و سایر مرکبات از تشکیل کیست در کلیهها جلوگیری میکند. براساس نتایج این تحقیقات که در مجله بریتانیایی فارموکولوژی به چاپ رسیده، مادهای به نام نارنژنین که در گریپ فروت و سایر مرکبات وجود دارد، قادر است تشکیل کیست در کلیه را متوقف سازد.  محققین نشان دادند که در افراد مبتلا به دیابت، احتمال اریتمی قلبی هم افزایش می یابد که می تواند به دلیل اتصال پروتئین کیناز II وابسته به کلسیم/کالمودولین به N-استیل گلوکز آمین باشد که منجر به افزایش سمیت گلوکز می شود. محققین برای اولین بار مسیر بیولوژیکی را کشف کرده اند که زمانی که سطوح قند خون به صورت غیر طبیعی بالاست فعال است و موجب ضربان غیر طبیعی قلب می شود. شرایطی که تحت عنوان آریتمی قلبی شناخته می شود و با نارسایی قلبی و مرگ ناگهانی قلبی مرتبط است.
محققین نشان دادند که در افراد مبتلا به دیابت، احتمال اریتمی قلبی هم افزایش می یابد که می تواند به دلیل اتصال پروتئین کیناز II وابسته به کلسیم/کالمودولین به N-استیل گلوکز آمین باشد که منجر به افزایش سمیت گلوکز می شود. محققین برای اولین بار مسیر بیولوژیکی را کشف کرده اند که زمانی که سطوح قند خون به صورت غیر طبیعی بالاست فعال است و موجب ضربان غیر طبیعی قلب می شود. شرایطی که تحت عنوان آریتمی قلبی شناخته می شود و با نارسایی قلبی و مرگ ناگهانی قلبی مرتبط است. شیوه جدید دانشمندان دانشگاه پرینستون و دانشگاه میشیگان از رایانه و نه تیغ جراحی برای جداسازی و شناسایی ژنهای مشتقشده از انواع خاص سلولی بهره میگیرد. درک چگونگی عملکرد ژنها در بافتهای خاص برای مقابله با بیماریهای انسانی از قبیل بیماریهای قلبی، نارسایی کلیه و سرطان حیاتی است. با این حال ایزولهکردن انواع سلولها در این نوع مطالعه برای اکثر بافتها غیرممکن است. این شیوه که "کالبدشکافی نانوسیلیکونی" نام گرفته، مطالعه نظاممند ژنهای دخیل در بیماریها را ممکن میکند.
شیوه جدید دانشمندان دانشگاه پرینستون و دانشگاه میشیگان از رایانه و نه تیغ جراحی برای جداسازی و شناسایی ژنهای مشتقشده از انواع خاص سلولی بهره میگیرد. درک چگونگی عملکرد ژنها در بافتهای خاص برای مقابله با بیماریهای انسانی از قبیل بیماریهای قلبی، نارسایی کلیه و سرطان حیاتی است. با این حال ایزولهکردن انواع سلولها در این نوع مطالعه برای اکثر بافتها غیرممکن است. این شیوه که "کالبدشکافی نانوسیلیکونی" نام گرفته، مطالعه نظاممند ژنهای دخیل در بیماریها را ممکن میکند.  مطالعه جدید نشان میدهد افراد متاهلی که مبتلا به سرطان هستند، در مقایسه با افراد مجرد، مدت طولانیتری زندگی میکنند. تحقیقات محققان «موسسه سرطان دانا-فاربر» و بریگهام و بیمارستان زنان امریکا همچنین نشان میدهد سرطان افراد متاهل در مراحل زودتری تشخیص داده میشود. افزون بر این، این افراد همچنین اغلب فرایند درمانی موفقیتآمیزتری دارند و درمان مناسبتری را نیز دریافت میکنند.
مطالعه جدید نشان میدهد افراد متاهلی که مبتلا به سرطان هستند، در مقایسه با افراد مجرد، مدت طولانیتری زندگی میکنند. تحقیقات محققان «موسسه سرطان دانا-فاربر» و بریگهام و بیمارستان زنان امریکا همچنین نشان میدهد سرطان افراد متاهل در مراحل زودتری تشخیص داده میشود. افزون بر این، این افراد همچنین اغلب فرایند درمانی موفقیتآمیزتری دارند و درمان مناسبتری را نیز دریافت میکنند.  پژوهش جدید محققان ژاپنی و آمریکایی نشان میدهد: چاقی در بیماران مبتلا به بیماری مزمن کلیه، باعث افزایش خطر ابتلا به نارسایی کلیوی میشود. چاقی فرآیند سلولی مهمی را که مانع از آسیب سلولهای کلیوی میشود، سرکوب میکند. دکتر "کوزوکه یاماهارا" از دانشگاه علوم پزشکی شیگا، کاهش عملکرد فرآیندی موسوم به "اتوفاژی" را در این چرخه مهم دانستهاند. اتوفاژی، فرآیند تخریب درونسلولی است که طی آن پروتئینهای آسیب دیده و سایر ترکیبات سلولهای معیوب را از بین میبرد؛ ناکارآمدی این چرخه در افراد چاق، امری شایع است.
پژوهش جدید محققان ژاپنی و آمریکایی نشان میدهد: چاقی در بیماران مبتلا به بیماری مزمن کلیه، باعث افزایش خطر ابتلا به نارسایی کلیوی میشود. چاقی فرآیند سلولی مهمی را که مانع از آسیب سلولهای کلیوی میشود، سرکوب میکند. دکتر "کوزوکه یاماهارا" از دانشگاه علوم پزشکی شیگا، کاهش عملکرد فرآیندی موسوم به "اتوفاژی" را در این چرخه مهم دانستهاند. اتوفاژی، فرآیند تخریب درونسلولی است که طی آن پروتئینهای آسیب دیده و سایر ترکیبات سلولهای معیوب را از بین میبرد؛ ناکارآمدی این چرخه در افراد چاق، امری شایع است.  مطالعات پیش گامانه نزدیک به 2300 بیمار دیابتی بسیار چاق به وسیله محققین صورت گرفت و آن ها ژن های مرتبط با عملکرد کبد ناسالم را شناسایی کردند. به نظر می رسد این اولین مطالعه ای است که در این مقیاس در مورد ارتباط ژنوم با بیماران چاق دیابتی صورت می گیرد. آنالیزهای گسترده ژنومی که جایگاه های مرتبط با سطوح کلی بیلی روبین، استئاتوزیز، و فیبروز خفیف را در بیماری کبد چرب غیر الکلی شناسایی می کند، به بررسی این مطلب می پردازد که چگونه عوامل ژنومی روی تکوین بیماری کبد چرب غیر الکلی اثر می گذارند. این عوامل ژنتیکی می توانند به ما در شناسایی بیمارانی که بیشتر در خطر ابتلا به اشکال مختلف بیماری کبد چرب هستند، کمک کنند و این که کدام بیماران احتمال بیشتری وجود دارد که به اشکال حاد تر کبد چرب غیر الکلی مانند steatohepatitis مبتلا شوند.
مطالعات پیش گامانه نزدیک به 2300 بیمار دیابتی بسیار چاق به وسیله محققین صورت گرفت و آن ها ژن های مرتبط با عملکرد کبد ناسالم را شناسایی کردند. به نظر می رسد این اولین مطالعه ای است که در این مقیاس در مورد ارتباط ژنوم با بیماران چاق دیابتی صورت می گیرد. آنالیزهای گسترده ژنومی که جایگاه های مرتبط با سطوح کلی بیلی روبین، استئاتوزیز، و فیبروز خفیف را در بیماری کبد چرب غیر الکلی شناسایی می کند، به بررسی این مطلب می پردازد که چگونه عوامل ژنومی روی تکوین بیماری کبد چرب غیر الکلی اثر می گذارند. این عوامل ژنتیکی می توانند به ما در شناسایی بیمارانی که بیشتر در خطر ابتلا به اشکال مختلف بیماری کبد چرب هستند، کمک کنند و این که کدام بیماران احتمال بیشتری وجود دارد که به اشکال حاد تر کبد چرب غیر الکلی مانند steatohepatitis مبتلا شوند. تحقيقات جديد محققان اسكاتلندي نشان مي دهد افرادي كه كمربند تنگ مي پوشند بيشتر از ديگران در معرض خطر ابتلا به سرطان گلو و دستگاه گوارش قرار دارند. محققان دانشگاه هاي گلاسكو و استراتكلايد و بيمارستان عمومي جنوب اسكاتلند گفتند : استفاده از كمربند تنگ خطر ابتلا به سرطان گلو و دستگاه گوارش را افزايش مي دهد. اين خطر در افرادي كه اضافه وزن دارند بيشتر از ديگران است.
تحقيقات جديد محققان اسكاتلندي نشان مي دهد افرادي كه كمربند تنگ مي پوشند بيشتر از ديگران در معرض خطر ابتلا به سرطان گلو و دستگاه گوارش قرار دارند. محققان دانشگاه هاي گلاسكو و استراتكلايد و بيمارستان عمومي جنوب اسكاتلند گفتند : استفاده از كمربند تنگ خطر ابتلا به سرطان گلو و دستگاه گوارش را افزايش مي دهد. اين خطر در افرادي كه اضافه وزن دارند بيشتر از ديگران است. مطالعه ای جدیدا صورت گرفته که پتانسیل درمان های جایگزینی با پایه سلول های بنیادی را برای مهار مرحله آخر بیماری کلیوی بررسی می کند. این کار شامل طراحی یک نوع جدید از نانوذره های مغناطیسی برای نشان دار کردن سلول های بنیادی برای پی گیری های in vivo است. ریفلاکس نفروپاتی شرایطی است که در آن کلیه ها آسیب دیده هستند و یا در تمام طول مدت به دلیل جریان رو به عقب ادرار به کلیه زخم شده اند. این وضعیت ممکن است منجر به نارسایی کلیه در کودکان و بزرگسالان شود. هدف بلندمدت این پروژه طراحی یک درمان با مبنای سلول های بنیادی برای جایگزینی نفرون های از دست رفته از طریق ریفلاکس نفروپاتی است که در نهایت از بیماری های مزمن کلیه جلوگیری می کند.
مطالعه ای جدیدا صورت گرفته که پتانسیل درمان های جایگزینی با پایه سلول های بنیادی را برای مهار مرحله آخر بیماری کلیوی بررسی می کند. این کار شامل طراحی یک نوع جدید از نانوذره های مغناطیسی برای نشان دار کردن سلول های بنیادی برای پی گیری های in vivo است. ریفلاکس نفروپاتی شرایطی است که در آن کلیه ها آسیب دیده هستند و یا در تمام طول مدت به دلیل جریان رو به عقب ادرار به کلیه زخم شده اند. این وضعیت ممکن است منجر به نارسایی کلیه در کودکان و بزرگسالان شود. هدف بلندمدت این پروژه طراحی یک درمان با مبنای سلول های بنیادی برای جایگزینی نفرون های از دست رفته از طریق ریفلاکس نفروپاتی است که در نهایت از بیماری های مزمن کلیه جلوگیری می کند. محققان امریکایی قصد دارند با شناسایی اجزای مسیر انسولین، داروهای بهتری را برای دیابت تولید کنند. محققان موسسه
محققان امریکایی قصد دارند با شناسایی اجزای مسیر انسولین، داروهای بهتری را برای دیابت تولید کنند. محققان موسسه  محققان یک مارکرزیستی را کشف کرده اند که می تواند هدف درمانی بالقوه ای برای سرطان لوزالمعده باشد. محققان یک مارکر زیستی به نام
محققان یک مارکرزیستی را کشف کرده اند که می تواند هدف درمانی بالقوه ای برای سرطان لوزالمعده باشد. محققان یک مارکر زیستی به نام  استفاده از داروهای فشار خون مانند لوزارتان می تواند با باز کردن رگ ها خونی تخریب شده در تومورهای جامد در بهبود پیامد شیمی درمانی سرطان کمک مؤثری کند. دانشمندان توضیح دادند که چگونه داروی لوزارتان که مهار کننده آنژیوتانسین می باشد، انتقال داروهای شیمی درمانی و اکسیژن را با افزایش جریان خون به تومور در مدل های موشی سرطان سینه و پانکراس بهبود می بخشد.
استفاده از داروهای فشار خون مانند لوزارتان می تواند با باز کردن رگ ها خونی تخریب شده در تومورهای جامد در بهبود پیامد شیمی درمانی سرطان کمک مؤثری کند. دانشمندان توضیح دادند که چگونه داروی لوزارتان که مهار کننده آنژیوتانسین می باشد، انتقال داروهای شیمی درمانی و اکسیژن را با افزایش جریان خون به تومور در مدل های موشی سرطان سینه و پانکراس بهبود می بخشد.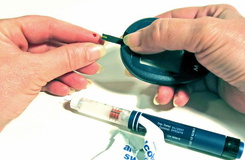 نوعی دارو که برای بیماری پوستی تجویز میشود میتواند در درمان دیابت نوع یک مورد استفاده قرار گیرد. داروی Alefacept که پیش از این برای درمان بیماری پوستی پسوریازیس استفاده می شد نتایج ترغیب کننده ای را در فاز2 آزمایشات به منظور ارزیابی موثر بودن آن در درمان دیابت نوع1 نشان داد. بیماری دیابت نوع1 بیماری اتوایمنی است که سیستم ایمنی بدن سلول های پانکراسی تولیدکننده انسولین را مورد تهاجم قرار میدهد و در نتیجه میزان انسولین برای تنظیم قند خون کافی نیست. حدود 400000 نفر در انگلستان به این بیماری مبتلا هستند که نیاز به تزریقات مکرر انسولین دارند و رفته رفته خطر بیماری و مرگ در این افراد با توجه به شرایط شان بالا می رود.
نوعی دارو که برای بیماری پوستی تجویز میشود میتواند در درمان دیابت نوع یک مورد استفاده قرار گیرد. داروی Alefacept که پیش از این برای درمان بیماری پوستی پسوریازیس استفاده می شد نتایج ترغیب کننده ای را در فاز2 آزمایشات به منظور ارزیابی موثر بودن آن در درمان دیابت نوع1 نشان داد. بیماری دیابت نوع1 بیماری اتوایمنی است که سیستم ایمنی بدن سلول های پانکراسی تولیدکننده انسولین را مورد تهاجم قرار میدهد و در نتیجه میزان انسولین برای تنظیم قند خون کافی نیست. حدود 400000 نفر در انگلستان به این بیماری مبتلا هستند که نیاز به تزریقات مکرر انسولین دارند و رفته رفته خطر بیماری و مرگ در این افراد با توجه به شرایط شان بالا می رود.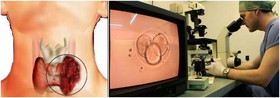 با کشفیات تازه در حوزه ژنتیک و مسیرهای پیام رسانی سلولی تومورهای تیروئید، محققان دانشگاه پنسیلوانیا موفق به توسعه سلاح جدیدی برای مقابله با سرطان تیروئید شدند. هیچ روش درمانی موثری برای بیماران مبتلا به سرطان تیروئید پیشرفته وجود ندارد، اما دستاوردهای اخیر محققان میتواند امیدهای تازهای برای بیماران ایجاد کند.
با کشفیات تازه در حوزه ژنتیک و مسیرهای پیام رسانی سلولی تومورهای تیروئید، محققان دانشگاه پنسیلوانیا موفق به توسعه سلاح جدیدی برای مقابله با سرطان تیروئید شدند. هیچ روش درمانی موثری برای بیماران مبتلا به سرطان تیروئید پیشرفته وجود ندارد، اما دستاوردهای اخیر محققان میتواند امیدهای تازهای برای بیماران ایجاد کند.