..:::: مصرف اورليستــات در بيمــاران مبتلا به کبدچـرب غيــرالکلي ::::..
تحقيقات تازه نشان ميدهد استفاده از داروي اورليستات همراه با برنامههاي کاهش وزن، در مقايسه با برنامه کاهش وزن به تنهايي، به طور قابلتوجهي بيماري کبد چرب غيرالکلي را کاهش ميدهد. هيچ درمان دارويي خاصي براي بيماران با بيماري کبد چرب غير الکي (NAFLD)، توصيه نميشود، و تنها تعداد اندکي از رژيمهاي درماني طي کارآزمائيهاي باليني مورد بررسي قرار گرفتهاند. اورليستات يک مهارکننده آنزيم ليپاز روده است که جريان ورود اسيدچرب آزاد به کبد را کاهش ميدهد و سبب کاهشوزن شده و حساسيت به انسولين را بهبود ميبخشد.
محققان در يک کارآزمايي تصادفي دوسوکور عملکرد اورليستات را در 52 بيمار مبتلا به NAFLD (با متوسط سني 47 سال؛ و متوسط شاخص توده بدني kg/m233) که در برنامه کاهش وزن شرکت داشتند، با دارونما مورد مقايسه قرار دادند. تشخيص NAFLD بر اساس انجام بيوپسي پايه کبدي در 40 بيمار و انجام سونوگرافي در ديگران بود. بيماران به طور تصادفي براي دريافت اورليستات (120 ميليگرم سه بار در روز) يا دريافت دارونما به مدت 6 ماه در دو گروه تقسيم شدند. در گروهي که اورليستات دريافت ميکردند، قندخون و ميزان انسولين به طور قابلتوجهي (03/0>P) بالاتر و ميزان فيبروز کبدي در مرحله پيشرفتهتري بود. بيماران هرماه تحت ارزيابيهاي بيومديکال و سونوگرافي قرار ميگرفتند و در 22 نفر از آنها در پايان مطالعه تحت بيوپسي مجدد کبدي قرار گرفتند. 44 بيمار مطالعه را کامل کردند (23 نفر آنها در گروه دارونما بودند). پيامدهاي مطالعه شامل تغييرات بيوشيميايي، تصويربرداري، بافت شناختي و تغييرات وزني بود.
شاخص توده بدني و ميزان آنزيمهاي کبدي از مقدار اوليه، در هر دو گروه به طور قابلتوجهي کاهش پيدا کرده بود اما کاهش آنزيمهاي کبدي در گروهي که اورليستات دريافت کرده بود در مقايسه با گروهي که دارونما مصرف کرده بودند، تقريبا دوبرابر بود (48% در مقابل 26%). در گروهي که اورليستات مصرف کردهبودند، تنها يک مورد عود قابلتوجه NAFLD براساس تشخيص سونوگرافي ديده شد (05/0>P). در ميان افرادي که تحت بيوپسي مجدد قرار گرفته بودند، وجود درجات متوسطي از استئاتوز که به معني بهبودي قابلتوجه نسبت به ميزان اوليه بود، هيچ تفاوتي در دو گروه وجود نداشت. اگرچه اين مطالعه کوچک بود، اما مشخص کرد که در مقايسه با کاهش وزن به تنهايي، اورليستات به همراه برنامه کاهشوزن، ميتواند به طور قابلتوجهي NAFLD را کاهش دهد. براي اينکه مشخص شود که آيا آيا اورليستات مزاياي بافتشناختي ديگري هم دارد يا نه مطالعات بزرگتري لازم است.
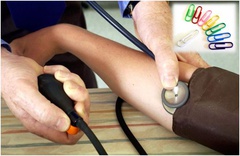 محققان انگلیسی دستگاه کوچکی شبیه گیره کاغذ طراحی کرده اند که داخل ران بیمار کاشته شده و به کاهش فشار خون کمک می کند. باریک شدن سرخرگ ها باعث افزایش فشار خون و در نتیجه بالا رفتن فشار خون می شود؛ در کنار کاهش مصرف نمک و افزایش فعالیت بدنی، داروهای مختلفی برای کنترل فشار خون تجویز می شوند. اما برخی بیماران به فشار خون بالای مقاوم (به درمان های دارویی) مبتلا بوده و دست کم سه نوع داروی مختلف برای آنها بی تأثیر است.
محققان انگلیسی دستگاه کوچکی شبیه گیره کاغذ طراحی کرده اند که داخل ران بیمار کاشته شده و به کاهش فشار خون کمک می کند. باریک شدن سرخرگ ها باعث افزایش فشار خون و در نتیجه بالا رفتن فشار خون می شود؛ در کنار کاهش مصرف نمک و افزایش فعالیت بدنی، داروهای مختلفی برای کنترل فشار خون تجویز می شوند. اما برخی بیماران به فشار خون بالای مقاوم (به درمان های دارویی) مبتلا بوده و دست کم سه نوع داروی مختلف برای آنها بی تأثیر است. محققان انگلیسی آزمایش ژنتیک منحصر به فردی را توسعه دادهاند که جهش ژنتیکی و احتمال توسعه بیماری در بین سایر اعضای خانواده بیمار سرطانی را مشخص می کند. افرادی که در بستگان درجه یک خود سابقه ابتلا به بیماری سرطان دارند، احتمالا داری ژن سرکش این بیماری هستند که خطر ابتلای آنها به این بیماری مهلک را بشدت افزایش می دهد. محققان موسسه تحقیقات سرطان انگلیس با همکاری شرکت تحقیقات ژنتیک Illumina آمریکا آزمایش ژنتیک جدیدی را توسعه داده اند که به تشخیص افراد در معرض خطر ابتلا به سرطان وراثتی ناشی از ناقل بودن ژن جهش یافته کمک می کند.
محققان انگلیسی آزمایش ژنتیک منحصر به فردی را توسعه دادهاند که جهش ژنتیکی و احتمال توسعه بیماری در بین سایر اعضای خانواده بیمار سرطانی را مشخص می کند. افرادی که در بستگان درجه یک خود سابقه ابتلا به بیماری سرطان دارند، احتمالا داری ژن سرکش این بیماری هستند که خطر ابتلای آنها به این بیماری مهلک را بشدت افزایش می دهد. محققان موسسه تحقیقات سرطان انگلیس با همکاری شرکت تحقیقات ژنتیک Illumina آمریکا آزمایش ژنتیک جدیدی را توسعه داده اند که به تشخیص افراد در معرض خطر ابتلا به سرطان وراثتی ناشی از ناقل بودن ژن جهش یافته کمک می کند.  محققان دانشگاه کوئینز بلفاست یک نانوداروی «گلوله جادویی» را طراحی کرده اند که میتواند اولین درمان موثر برای آسیبدیدگی حاد ریه باشد. عوامل اصلی این بیماری تصادفات جادهای و عفونت بوده و بسیاری از مبتلایان به آن در اثر نارسایی ریه میمیرند. بیماران مبتلا به آسیبهای حاد ریه اغلب نیازمند دستگاه کمک تنفس بوده و در حال حاضر درمان موثری برای این بیماری وجود ندارد اما در یک همکاری مشترک بین دانشکده داروسازی و مرکز عفونت و ایمنی دانشگاه کوئینز، دانشمندان توانستهاند داروی جدیدی را تولید کنند که میتواند مدیریت بالینی بیماران را در بخشهای آیسییو متحول کند.
محققان دانشگاه کوئینز بلفاست یک نانوداروی «گلوله جادویی» را طراحی کرده اند که میتواند اولین درمان موثر برای آسیبدیدگی حاد ریه باشد. عوامل اصلی این بیماری تصادفات جادهای و عفونت بوده و بسیاری از مبتلایان به آن در اثر نارسایی ریه میمیرند. بیماران مبتلا به آسیبهای حاد ریه اغلب نیازمند دستگاه کمک تنفس بوده و در حال حاضر درمان موثری برای این بیماری وجود ندارد اما در یک همکاری مشترک بین دانشکده داروسازی و مرکز عفونت و ایمنی دانشگاه کوئینز، دانشمندان توانستهاند داروی جدیدی را تولید کنند که میتواند مدیریت بالینی بیماران را در بخشهای آیسییو متحول کند. در دستاورد جالبی که میتواند بزودی رایانهها را جایگزین انسان در امور پزشکی کند، محققان بیمارستان پزشکی دانشگاه ماستریخت، فرمولهای ریاضی طراحی کردهاند که بهتر از انسان، واکنش بیماران سرطانی به شیمیدرمانی را تشخیص میدهند. هر مدل ریاضیاتی با جزئیات پزشکی شخصی و تاریخچه درمان هر بیمار تغذیه میشود و تا کنون یک مدل رایانهای از سرطان ریه توانسته بهتر از پزشکان انسان علائم آینده بیمار را پس از رادیودرمانی یا شیمیدرمانی پیشبینی کند. سازندگان این فرمولها معتقدند که بهتر است از این مدلها در عملکرد بالینی برای تصمیمگیریهای بهتر استفاده شود. محققان از مدلهای رایانهای برای تعیین میزان زنده ماندن یک گروه 21 نفری از بیماران سرطان ریه، تعداد افرادی که با مشکل تنفس روبرو میشوند و تعداد افراد دارای مشکل بلع در طول دو سال، استفاده کردند. هرچه اطلاعات بیشتری در مورد بیماران مانند ساختار ژنتیکی آنها جمعآوری میشد، مدلهای رایانهای از اهمیت بیشتری در تصمیمگیری در چگونگی واکنش به بیماریهای خاص برخوردار میشدند. دانشمندان اخیرا دریافتهاند که تومورهای سرطانی میان بیماران متفاوت بوده و درمانهای مختلف طبق ژنتیک بیماران مورد نیاز است. مدلهای رایانهای میتواند در محاسبه این بررسی پیچیده ریاضیاتی موثر باشد.
در دستاورد جالبی که میتواند بزودی رایانهها را جایگزین انسان در امور پزشکی کند، محققان بیمارستان پزشکی دانشگاه ماستریخت، فرمولهای ریاضی طراحی کردهاند که بهتر از انسان، واکنش بیماران سرطانی به شیمیدرمانی را تشخیص میدهند. هر مدل ریاضیاتی با جزئیات پزشکی شخصی و تاریخچه درمان هر بیمار تغذیه میشود و تا کنون یک مدل رایانهای از سرطان ریه توانسته بهتر از پزشکان انسان علائم آینده بیمار را پس از رادیودرمانی یا شیمیدرمانی پیشبینی کند. سازندگان این فرمولها معتقدند که بهتر است از این مدلها در عملکرد بالینی برای تصمیمگیریهای بهتر استفاده شود. محققان از مدلهای رایانهای برای تعیین میزان زنده ماندن یک گروه 21 نفری از بیماران سرطان ریه، تعداد افرادی که با مشکل تنفس روبرو میشوند و تعداد افراد دارای مشکل بلع در طول دو سال، استفاده کردند. هرچه اطلاعات بیشتری در مورد بیماران مانند ساختار ژنتیکی آنها جمعآوری میشد، مدلهای رایانهای از اهمیت بیشتری در تصمیمگیری در چگونگی واکنش به بیماریهای خاص برخوردار میشدند. دانشمندان اخیرا دریافتهاند که تومورهای سرطانی میان بیماران متفاوت بوده و درمانهای مختلف طبق ژنتیک بیماران مورد نیاز است. مدلهای رایانهای میتواند در محاسبه این بررسی پیچیده ریاضیاتی موثر باشد. پروژه شبکه تحقیقات اطلس ژنوم سرطانی با طراحی الگوریتم اختصاصی، امکان آنالیز ژنوم انسانی برای جهش های سرطانی را فراهم کرده است. نکات مبهم فراوانی درخصوص نحوه شکل گیری و رشد سلول های سرطانی وجود دارد و ژنوم انسانی این پیچیدگیها را چند برابر میکنند. با استفاده از الگوریتم اختصاصی ++Dendrix که برای آنالیز ژنوم انسانی دخیل در جهشهای سرطانی طراحی شده است، محققان قادر به شناسایی مشخصات ژنتیکی نوعی از سرطان خون موسوم به لوسمی میلوئیدی حاد شدهاند. این الگوریتم اختصاصی با کمک رایانه، اطلاعات ژنتیکی یا ژنهای موجود در سلولهای سرطانی را با ژنومهای سلولهای سالم بیمار مقایسه می کند.
پروژه شبکه تحقیقات اطلس ژنوم سرطانی با طراحی الگوریتم اختصاصی، امکان آنالیز ژنوم انسانی برای جهش های سرطانی را فراهم کرده است. نکات مبهم فراوانی درخصوص نحوه شکل گیری و رشد سلول های سرطانی وجود دارد و ژنوم انسانی این پیچیدگیها را چند برابر میکنند. با استفاده از الگوریتم اختصاصی ++Dendrix که برای آنالیز ژنوم انسانی دخیل در جهشهای سرطانی طراحی شده است، محققان قادر به شناسایی مشخصات ژنتیکی نوعی از سرطان خون موسوم به لوسمی میلوئیدی حاد شدهاند. این الگوریتم اختصاصی با کمک رایانه، اطلاعات ژنتیکی یا ژنهای موجود در سلولهای سرطانی را با ژنومهای سلولهای سالم بیمار مقایسه می کند. اخیرا روشی برای رهاسازی DNA و RNA درون یک سلول سرطانی ارائه شده است. در این روش از مولکولهای چربی در مقیاس نانو استفاده میشود. پزشکی مدرن بدنبال این است که از داروهای کوچک استفاده کند؛ داروهایی که حاوی مسکنهایی نظیر آسپرین و آنتیبیوتیکهایی نظیر پنیسیلین هستند. این داروها طول عمر بشر را افزایش میدهند. اخیرا محققان روشی یافتهاند که با استفاده از آن میتوان رهاسازی دارو را در مقیاس نانو انجام داد که این روش کارایی بیشتری نسبت به روشهای پیشین دارد. با رهاسازی DNA و RNA درون یک سلول خاص، میتوان به صورت خاص یک ژن را روشن یا خاموش کرد. از سوی دیگر یک سیستم نانومقیاس درون بدن قرار میگیرد که میتواند امکان ردیابی دارو را در بافتهای خاصی فراهم کند، همچنین این سیستم میتواند در یک دوره زمانی تعریف شده رهاسازی را انجام دهد.
اخیرا روشی برای رهاسازی DNA و RNA درون یک سلول سرطانی ارائه شده است. در این روش از مولکولهای چربی در مقیاس نانو استفاده میشود. پزشکی مدرن بدنبال این است که از داروهای کوچک استفاده کند؛ داروهایی که حاوی مسکنهایی نظیر آسپرین و آنتیبیوتیکهایی نظیر پنیسیلین هستند. این داروها طول عمر بشر را افزایش میدهند. اخیرا محققان روشی یافتهاند که با استفاده از آن میتوان رهاسازی دارو را در مقیاس نانو انجام داد که این روش کارایی بیشتری نسبت به روشهای پیشین دارد. با رهاسازی DNA و RNA درون یک سلول خاص، میتوان به صورت خاص یک ژن را روشن یا خاموش کرد. از سوی دیگر یک سیستم نانومقیاس درون بدن قرار میگیرد که میتواند امکان ردیابی دارو را در بافتهای خاصی فراهم کند، همچنین این سیستم میتواند در یک دوره زمانی تعریف شده رهاسازی را انجام دهد. تحقیقات صورت گرفته توسط محققان دانشگاه هاروارد نشان می دهد، افرادی که در خواب خروپف کرده و بیش از 9 ساعت می خوابند، دو برابر بیش از سایرین در معرض ابتلا به سرطان روده قرار دارند. این مطالعه رابطه معناداری بین مدت زمان خواب و احتمال ابتلا به سرطان روده بزرگ را بویژه در بین افرادی که دچار اضافه وزن هستند یا در هنگام خواب خروپف می کنند، نشان میدهد. افراد دچار آپنه انسدادی خواب بدلیل مختل شدن خواب ناشی از قطع تنفس، بیشتر خسته شده و تمایل به خواب طولانی تری دارند. نتایج بدست آمده در این تحقیق نشان می دهد، آپنه انسدادی خواب یا خروپف همراه با قطع تنفس نقش موثری در افزایش خطر ابتلا به سرطان ایفا می کند.
تحقیقات صورت گرفته توسط محققان دانشگاه هاروارد نشان می دهد، افرادی که در خواب خروپف کرده و بیش از 9 ساعت می خوابند، دو برابر بیش از سایرین در معرض ابتلا به سرطان روده قرار دارند. این مطالعه رابطه معناداری بین مدت زمان خواب و احتمال ابتلا به سرطان روده بزرگ را بویژه در بین افرادی که دچار اضافه وزن هستند یا در هنگام خواب خروپف می کنند، نشان میدهد. افراد دچار آپنه انسدادی خواب بدلیل مختل شدن خواب ناشی از قطع تنفس، بیشتر خسته شده و تمایل به خواب طولانی تری دارند. نتایج بدست آمده در این تحقیق نشان می دهد، آپنه انسدادی خواب یا خروپف همراه با قطع تنفس نقش موثری در افزایش خطر ابتلا به سرطان ایفا می کند. براساس گزارش انجمن بینالمللی غذا 50 درصد از افراد به دریافت پروتئین بیشتری در رژیم غذایی خود علاقهمند هستند و37 درصد معتقدند که پروتئین به کاهش وزن آنان کمک میکند. در تحقیق جدید منتشر شده، محققان دریافتند مصرف بالای پروتئین در زنان با کاهش وزن آنان مرتبط است. محققان دانشگاه "مینی سوتا " در تحقیق ملی که بر روی 1824 زن میانسال 40تا 60ساله انجام شد منابع پروتئینی و میزان نیاز بدن به آنها و همچنین گزارشهای مربوط به مصرف بالای پروتئین و جلوگیری از اضافه وزن را بررسی کردند و گزارشهای مقدار مصرف پروتئین به طور متناوب باهم مقایسه شدند.
براساس گزارش انجمن بینالمللی غذا 50 درصد از افراد به دریافت پروتئین بیشتری در رژیم غذایی خود علاقهمند هستند و37 درصد معتقدند که پروتئین به کاهش وزن آنان کمک میکند. در تحقیق جدید منتشر شده، محققان دریافتند مصرف بالای پروتئین در زنان با کاهش وزن آنان مرتبط است. محققان دانشگاه "مینی سوتا " در تحقیق ملی که بر روی 1824 زن میانسال 40تا 60ساله انجام شد منابع پروتئینی و میزان نیاز بدن به آنها و همچنین گزارشهای مربوط به مصرف بالای پروتئین و جلوگیری از اضافه وزن را بررسی کردند و گزارشهای مقدار مصرف پروتئین به طور متناوب باهم مقایسه شدند. شاید مغز جای واضحی برای جستوجوی درمانهای ممکن چاقی نباشد؛ اما محققان دانشگاه پنسیلوانیا میگویند کاشت یک دستگاه با قابلیت تحریک منطقه خاصی از مغز میتواند به مهار اجبار در پرخوری کمک کند. پژوهش جدید بر روی موشهای چاق نشان داد تحریک عمیق مغز که شامل کاشت یک دستگاه برای ارسال پالسهای الکتریکی به اهداف دقیق در مغز بوده، میتواند رفتارهای مرتبط با چاقی مانند خوردن مفرط را کاهش دهد.
شاید مغز جای واضحی برای جستوجوی درمانهای ممکن چاقی نباشد؛ اما محققان دانشگاه پنسیلوانیا میگویند کاشت یک دستگاه با قابلیت تحریک منطقه خاصی از مغز میتواند به مهار اجبار در پرخوری کمک کند. پژوهش جدید بر روی موشهای چاق نشان داد تحریک عمیق مغز که شامل کاشت یک دستگاه برای ارسال پالسهای الکتریکی به اهداف دقیق در مغز بوده، میتواند رفتارهای مرتبط با چاقی مانند خوردن مفرط را کاهش دهد. نوعی هورمون با کمک به بدن برای تولید انسولین، درمان جدیدی را برای بیماران مبتلا به دیابت ارائه میدهد و نیاز آنها به تزریق روزانه انسولین را برطرف میکند. محققان دانشگاه هاروارد دریافتند که هورمونی به نام betatrophin رشد سلولهایی که انسولین را به درون خون بدن ترشح میکنند، ارتقا میدهد. در تحقیقات انجامشده، این هورمون موجب شد که موشها سلولهای انسولین را 30 برابر سریعتر از حالت معمول تولید کنند. محققان بر این باورند که این هورمون میتواند درمان بسیار کارآمدتری را برای بیماران دیابت 2 ارائه دهد. در این روش به جای تزریق روزانه برای کنترل میزان قند خون، بیماران هورمون مزبور را هر هفته یا ماهانه و در خوشبینانهترین حالت، سالانه به بدن خود تزریق میکنند.
نوعی هورمون با کمک به بدن برای تولید انسولین، درمان جدیدی را برای بیماران مبتلا به دیابت ارائه میدهد و نیاز آنها به تزریق روزانه انسولین را برطرف میکند. محققان دانشگاه هاروارد دریافتند که هورمونی به نام betatrophin رشد سلولهایی که انسولین را به درون خون بدن ترشح میکنند، ارتقا میدهد. در تحقیقات انجامشده، این هورمون موجب شد که موشها سلولهای انسولین را 30 برابر سریعتر از حالت معمول تولید کنند. محققان بر این باورند که این هورمون میتواند درمان بسیار کارآمدتری را برای بیماران دیابت 2 ارائه دهد. در این روش به جای تزریق روزانه برای کنترل میزان قند خون، بیماران هورمون مزبور را هر هفته یا ماهانه و در خوشبینانهترین حالت، سالانه به بدن خود تزریق میکنند.  محققان دانشگاه واشنگتن یک حسگر زیستپزشکی را با استفاده از نانومیلههای طلا، برای تشخیص افزایش لیپوکالین وابسته به ژلاتیناز نوتروفیل بعنوان یک زیستنشانگر آسیبهای حاد کلیه ساختهاند. یافتههای «اِوان کراش» و همکارانش در دانشکده پزشکی دانشگاه واشنگتن تشخیص آسیبهای جدی کلیه را به سادگی از طریق فرو بردن یک کاغذ آزمایش در ادرار میسر کرده است. زیستنشانگرها عموما مولکولها یا پروتئینهای کوچکی در بدن هستند که با تغییر غلظت در بدن به بیماری و یا درمان پاسخ میدهند. «کراش» معتقد است که این فناوری مبتکرانه بررسی عملکرد کلیه را بصورت بالینی و با هزینه کمتر فراهم میآورد.
محققان دانشگاه واشنگتن یک حسگر زیستپزشکی را با استفاده از نانومیلههای طلا، برای تشخیص افزایش لیپوکالین وابسته به ژلاتیناز نوتروفیل بعنوان یک زیستنشانگر آسیبهای حاد کلیه ساختهاند. یافتههای «اِوان کراش» و همکارانش در دانشکده پزشکی دانشگاه واشنگتن تشخیص آسیبهای جدی کلیه را به سادگی از طریق فرو بردن یک کاغذ آزمایش در ادرار میسر کرده است. زیستنشانگرها عموما مولکولها یا پروتئینهای کوچکی در بدن هستند که با تغییر غلظت در بدن به بیماری و یا درمان پاسخ میدهند. «کراش» معتقد است که این فناوری مبتکرانه بررسی عملکرد کلیه را بصورت بالینی و با هزینه کمتر فراهم میآورد. 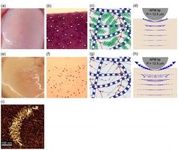 خواص زیست مکانیکی نانو مقیاس غضروفها در مفاصل میتواند آرتروز استخوان را در مراحل اولیه تحت تاثیر قرار دهد. این خواص زیست مکانیکی غضروفها موجب میشود تا در طول فعالیتهای فیزیکی سریع، غضروفها مستعد آسیب باشند. آرتروز استخوان یکی از مشکلات رایج است که بیش از یک سوم افراد کهنسال از آن رنج میبرند. در حال حاضر هیچ درمانی برای این بیماری وجود ندارد. یافتههای این پژوهش میتواند برای شناسایی بیماری در مراحل مقدماتی مفید باشد، همچنین مهندسان بافت میتوانند از این یافتهها برای ترمیم غضروفهای آسیبدیده در بیماران استفاده کنند.
خواص زیست مکانیکی نانو مقیاس غضروفها در مفاصل میتواند آرتروز استخوان را در مراحل اولیه تحت تاثیر قرار دهد. این خواص زیست مکانیکی غضروفها موجب میشود تا در طول فعالیتهای فیزیکی سریع، غضروفها مستعد آسیب باشند. آرتروز استخوان یکی از مشکلات رایج است که بیش از یک سوم افراد کهنسال از آن رنج میبرند. در حال حاضر هیچ درمانی برای این بیماری وجود ندارد. یافتههای این پژوهش میتواند برای شناسایی بیماری در مراحل مقدماتی مفید باشد، همچنین مهندسان بافت میتوانند از این یافتهها برای ترمیم غضروفهای آسیبدیده در بیماران استفاده کنند.  محققان مرکز تحقیقات سرطان انگلستان در دانشگاه کمبریج و همچنین دانشمندان هلندی خبر از کشف نوع جدیدی از سرطان روده داده اند که پیامدهای بدتری را در مقایسه با سایر سرطان های روده بزرگ دارد و در مقابل درمان های خاص، مقاومت نشان می دهد. محققان با بررسی بر اطلاعات 146 ژن مرتبط با سرطان روده که از 11 هزار بیمار به دست آمده بود متوجه شدند که بیش از یک چهارم افراد مبتلا به نوع جدیدی از سرطان روده شده اند که پیش از این در زیر مجموعه هیچ کدام از سرطان ها دیده نشده بود. برای این دسته از بیماران مبتلا به نوع جدید سرطان روده، احتمال بدتر شدن، تهاجمی تر شدن تومورها و همچنین مقاومت به داروهایی درمانی نظیر "ستوکسیمب"، زیاد گزارش شده بود.
محققان مرکز تحقیقات سرطان انگلستان در دانشگاه کمبریج و همچنین دانشمندان هلندی خبر از کشف نوع جدیدی از سرطان روده داده اند که پیامدهای بدتری را در مقایسه با سایر سرطان های روده بزرگ دارد و در مقابل درمان های خاص، مقاومت نشان می دهد. محققان با بررسی بر اطلاعات 146 ژن مرتبط با سرطان روده که از 11 هزار بیمار به دست آمده بود متوجه شدند که بیش از یک چهارم افراد مبتلا به نوع جدیدی از سرطان روده شده اند که پیش از این در زیر مجموعه هیچ کدام از سرطان ها دیده نشده بود. برای این دسته از بیماران مبتلا به نوع جدید سرطان روده، احتمال بدتر شدن، تهاجمی تر شدن تومورها و همچنین مقاومت به داروهایی درمانی نظیر "ستوکسیمب"، زیاد گزارش شده بود. محققان بیمارستان عمومی ماساچوست در بوستون موفق به ساخت یک کلیه کاربردی در آزمایشگاه شدند که پس از پیوند به موش قادر به دفع مایعات شده است. این کلیه مهندسی شده بر روی چارچوب ابتدایی یک کلیه موجود ساخته شده است. در حالیکه کار بیشتری برای استفاده از این فناوری در ساخت کلیه انسان مورد نیاز بوده، محققان امیدوارند که در نهایت چنین شیوهای بتواند به عنوان یک گزینه جدید برای افراد دارای مشکلات کلیوی و نیازمند پیوند عضو مورد استفاده قرار گیرد. از آن جایی که این اندام از سلولهای خود فرد ساخته میشود، خطر دفع آن توسط سیستم ایمنی بدن بسیار کمتر خواهد بود.
محققان بیمارستان عمومی ماساچوست در بوستون موفق به ساخت یک کلیه کاربردی در آزمایشگاه شدند که پس از پیوند به موش قادر به دفع مایعات شده است. این کلیه مهندسی شده بر روی چارچوب ابتدایی یک کلیه موجود ساخته شده است. در حالیکه کار بیشتری برای استفاده از این فناوری در ساخت کلیه انسان مورد نیاز بوده، محققان امیدوارند که در نهایت چنین شیوهای بتواند به عنوان یک گزینه جدید برای افراد دارای مشکلات کلیوی و نیازمند پیوند عضو مورد استفاده قرار گیرد. از آن جایی که این اندام از سلولهای خود فرد ساخته میشود، خطر دفع آن توسط سیستم ایمنی بدن بسیار کمتر خواهد بود. دانشمندان دانشگاه هاروارد در حال طراحی ابزاری به نام «طحال بر روی تراشه» هستند که به طحال در انجام وظیفهاش به هنگام بروز بیماری شدید در بدن کمک میکند. وظیفه طحال، فیلترکردن جریان خون است و زمانی که اشخاص به طور شدیدی بیمار هستند و یا از آسیبهای تروماتیک رنج میبرند، گاهی اوقات این عضو به تنهایی قادر به برطرف کردن کامل پاتوژنها نیست که این امر منجر به بروز مسمومیت عفونی مرگبار میشود. به منظور کمک به اجتناب از چنین امری، دانشمندان موسسه وایس در دانشگاه هاروارد در حال طراحی «طحال بر روی یک تراشه» هستند.
دانشمندان دانشگاه هاروارد در حال طراحی ابزاری به نام «طحال بر روی تراشه» هستند که به طحال در انجام وظیفهاش به هنگام بروز بیماری شدید در بدن کمک میکند. وظیفه طحال، فیلترکردن جریان خون است و زمانی که اشخاص به طور شدیدی بیمار هستند و یا از آسیبهای تروماتیک رنج میبرند، گاهی اوقات این عضو به تنهایی قادر به برطرف کردن کامل پاتوژنها نیست که این امر منجر به بروز مسمومیت عفونی مرگبار میشود. به منظور کمک به اجتناب از چنین امری، دانشمندان موسسه وایس در دانشگاه هاروارد در حال طراحی «طحال بر روی یک تراشه» هستند.  محققان بر اساس نتایج حاصل از یک پژوهش جدید بر روی بیماران مبتلا به بیماری ارثی عروق خون دریافتند: سطوح پایین آهن موجود در خون با افزایش خطر تشکیل لختههای خونی خطرناک در ورید، همراه است. به گفته محققان امپریال کالج لندن یافتههای این پژوهش نشان میدهد: درمان کمبود آهن به جلوگیری از بیماری شناخته شده ترومبوز (تشکیل لختهی خون) وریدهای عمقی (DVT) کمک میکند.
محققان بر اساس نتایج حاصل از یک پژوهش جدید بر روی بیماران مبتلا به بیماری ارثی عروق خون دریافتند: سطوح پایین آهن موجود در خون با افزایش خطر تشکیل لختههای خونی خطرناک در ورید، همراه است. به گفته محققان امپریال کالج لندن یافتههای این پژوهش نشان میدهد: درمان کمبود آهن به جلوگیری از بیماری شناخته شده ترومبوز (تشکیل لختهی خون) وریدهای عمقی (DVT) کمک میکند. دانشمندان دانشگاه میسوری روش جدیدی را برای درمان سرطان معرفی کردهاند که بدون داشتن عوارض جانبی این بیماری مهلک را درمان میکند. مدتی کوتاه پس از کشف نوترون در سال 1932، تعدادی از دانشمندان به پتانسیل «درمان گیراندازی نوترون بور» (BNCT) به عنوان درمانی برای سرطان پی بردند. با این حال علیرغم دههها تحقیق، مشکل یافتن یک عامل تحویل که بتواند تومورها را بدون آسیبرساندن به بافتهای اطراف به طور کارآمدی هدف قرار دهد، به قوه خود باقی ماند.
دانشمندان دانشگاه میسوری روش جدیدی را برای درمان سرطان معرفی کردهاند که بدون داشتن عوارض جانبی این بیماری مهلک را درمان میکند. مدتی کوتاه پس از کشف نوترون در سال 1932، تعدادی از دانشمندان به پتانسیل «درمان گیراندازی نوترون بور» (BNCT) به عنوان درمانی برای سرطان پی بردند. با این حال علیرغم دههها تحقیق، مشکل یافتن یک عامل تحویل که بتواند تومورها را بدون آسیبرساندن به بافتهای اطراف به طور کارآمدی هدف قرار دهد، به قوه خود باقی ماند. نتایج تحقیق انجام شده توسط پژوهشگران آمریکایی نشان داد: چاقی در ناحیه شکم علاوه بر دیابت و بیماریهای قلبی، خطر ابتلا به استئوپروزیس یا پوکی استخوان در زنان را تشدید میکند.
نتایج تحقیق انجام شده توسط پژوهشگران آمریکایی نشان داد: چاقی در ناحیه شکم علاوه بر دیابت و بیماریهای قلبی، خطر ابتلا به استئوپروزیس یا پوکی استخوان در زنان را تشدید میکند.