..:::: کشف ژنی که خطر سرطان پستان را به شدت افزایش میدهد ::::..

جهش های ژنتیکی نادر در این ژن در سه خانواده از مجموع 49 خانواده با سابقه خانوادگی ابتلا به سرطان پستان شناسایی شد. سپس محققان ارتباط بین جهش های RINT1 و خطر ابتلا به سرطان پستان را مورد ارزیابی قرار دادند که این مسأله منجر به شناسایی حاملان 23 ژن در نمونههای گرفته شده از یک هزار و 313 زن با نشانه های اولیه سرطان و شش ژن در یک هزار و 123 نمونه غیر مبتلا به سرطان شد.
بر این اساس، ارتباط معناداری بین جهش ها در ژن RINT1 و افزایش خطر ابتلا به سرطان پستان در زنان با سابقه خانوادگی وجود دارد. پروفسور «ملیسا ساوتی» از محققان دپارتمان پاتولوژی دانشگاه ملبورن تأکید میکند: در حال حاضر تنها 35 درصد از خطر سابقه ژنتیکی ابتلا به سرطان پستان شناسایی شده اند و کشف این ژن جدید کمک بزرگی برای زنان دارای چند مورد سابقه خانوادگی ابتلا به سرطان پستان محسوب میشود. در ادامه تحقیقات، 684 زن مبتلا به سرطان با سابقه خانوادگی برای بررسی جهشهای RINT1 و شش خانواده حامل جهشهای ژن RINT1 مورد ارزیابی قرار می گیرند.
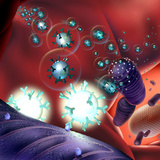 محققان مؤسسه تحقیقات کاربردی پلیمر فرانهوفر آلمان شیوه جدیدی ابداع کردهاند که به نمایش مواد حاوی نانوذرات با قابلیت کشتن انتخابی سلولهای تومور میپردازد. محققان از آبگریزها یا وزیکولهای چربی نامحلول در آب به عنوان حاملهای دارویی کوچک 200 تا 250 نانومتری استفاده کردند. این حاملها از لحاظ زیستی در بدن پس از استقرار قابل تخریب و تجزیه هستند. از پلیمرها برای تثبیت نانوپوشش استفاده میشود که از مولکولهای بسیار خاص و به رسمیت شناخته شده توسط سلولهای تومور برخوردارند. این پوشش نانوذرات که متخصصان آن را ویزکول مینامند، از ساختاری شبیه سلول برخوردارند.
محققان مؤسسه تحقیقات کاربردی پلیمر فرانهوفر آلمان شیوه جدیدی ابداع کردهاند که به نمایش مواد حاوی نانوذرات با قابلیت کشتن انتخابی سلولهای تومور میپردازد. محققان از آبگریزها یا وزیکولهای چربی نامحلول در آب به عنوان حاملهای دارویی کوچک 200 تا 250 نانومتری استفاده کردند. این حاملها از لحاظ زیستی در بدن پس از استقرار قابل تخریب و تجزیه هستند. از پلیمرها برای تثبیت نانوپوشش استفاده میشود که از مولکولهای بسیار خاص و به رسمیت شناخته شده توسط سلولهای تومور برخوردارند. این پوشش نانوذرات که متخصصان آن را ویزکول مینامند، از ساختاری شبیه سلول برخوردارند. 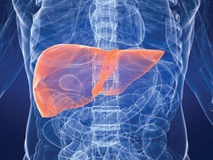 محققان دانشگاه بینالمللی سنگاپور طی پژوهشی دریافتند فعال کردن خانوادهای از پروتئین خاص کوچک موسوم به "Rho" میتواند سرطان کبد را سرکوب کند. این برای نخستین بار است که محققان توانستهاند شواهدی را مبنی بر تاثیر سیگنال دهی مخابراتی بین سوئیچهای پروتئین متفاوت بر توسعه بافت سرطانی نشان دهند.
محققان دانشگاه بینالمللی سنگاپور طی پژوهشی دریافتند فعال کردن خانوادهای از پروتئین خاص کوچک موسوم به "Rho" میتواند سرطان کبد را سرکوب کند. این برای نخستین بار است که محققان توانستهاند شواهدی را مبنی بر تاثیر سیگنال دهی مخابراتی بین سوئیچهای پروتئین متفاوت بر توسعه بافت سرطانی نشان دهند.  «رزوراترول» موجود در پوست انگور قرمز میتواند سلولهای خاصی از تومور را در برابر پرتودرمانی حساستر کند که با استفاده از این امر، میتوان در آینده راههای تولید قرصهای مخرب سرطان را هموارتر کرد. محققان آمریکایی به دنبال پژوهش دانشگاه میسوری مبنی بر تاثیر این ماده بر سرطان پروستات، تحقیق مشابه را بر سلولهای سرطان ملانوم، جدیترین نوع سرطان پوست انجام دادند. به گفته محققان این یافته تصدیقی است بر نتایج تحقیق قبلی و علاوه بر این نشان میدهد که چگونه ترکیب درمان «رزوراترول» و پرتودرمانی، حیات سلولهای ملانومی را از بین میبرد.
«رزوراترول» موجود در پوست انگور قرمز میتواند سلولهای خاصی از تومور را در برابر پرتودرمانی حساستر کند که با استفاده از این امر، میتوان در آینده راههای تولید قرصهای مخرب سرطان را هموارتر کرد. محققان آمریکایی به دنبال پژوهش دانشگاه میسوری مبنی بر تاثیر این ماده بر سرطان پروستات، تحقیق مشابه را بر سلولهای سرطان ملانوم، جدیترین نوع سرطان پوست انجام دادند. به گفته محققان این یافته تصدیقی است بر نتایج تحقیق قبلی و علاوه بر این نشان میدهد که چگونه ترکیب درمان «رزوراترول» و پرتودرمانی، حیات سلولهای ملانومی را از بین میبرد.  تحقیقات حاکی از آن است که نوعی پروتئین در صفرا در تشخیص سرطان پانکراس موثر است. تحقیقات نشان میدهد که این روش میتواند از آزمایش خون هم بهتر عمل کند و در تشخیص زودهنگام این سرطان موثر باشد. بر اساس مطالعات جدید نوعی پروتئین در صفرا در شناسایی سرطان لوزالمعده نیز موثر است. محققان دریافتند که این نشانگر که عروق عامل رشد اندوتلیال (VEGF) نامیده میشود، در 93 درصد موارد به شناسایی سرطان لوزالمعده کمک میکند. بیماران مبتلا به سرطان پانکراس یا مجرای صفراوی معمولا انسداد مجرای صفرا و یرقان دارند. محققان افزودند: انسداد مجرای صفراوی از نشانههای غیرسرطانی مانند سنگ مجرای صفراوی هم ناشی میشود. انسداد مجرای صفراوی انسداد در لولههای حمل کننده صفرا از کبد به کیسه صفرا و روده کوچک است. صفرا به هضم کمک میکند.
تحقیقات حاکی از آن است که نوعی پروتئین در صفرا در تشخیص سرطان پانکراس موثر است. تحقیقات نشان میدهد که این روش میتواند از آزمایش خون هم بهتر عمل کند و در تشخیص زودهنگام این سرطان موثر باشد. بر اساس مطالعات جدید نوعی پروتئین در صفرا در شناسایی سرطان لوزالمعده نیز موثر است. محققان دریافتند که این نشانگر که عروق عامل رشد اندوتلیال (VEGF) نامیده میشود، در 93 درصد موارد به شناسایی سرطان لوزالمعده کمک میکند. بیماران مبتلا به سرطان پانکراس یا مجرای صفراوی معمولا انسداد مجرای صفرا و یرقان دارند. محققان افزودند: انسداد مجرای صفراوی از نشانههای غیرسرطانی مانند سنگ مجرای صفراوی هم ناشی میشود. انسداد مجرای صفراوی انسداد در لولههای حمل کننده صفرا از کبد به کیسه صفرا و روده کوچک است. صفرا به هضم کمک میکند.  محققان دانشگاه مکگیل کانادا موفق به طراحی نانوقفسهای مبتنی بر رشتههای دیانای شدند که از آن میتوان برای رهایش هوشمند دارو استفاده کرد. در حال حاضر این گروه تحقیقاتی در حال مطالعه اثربخشی این نانوقفسههای مبتنی بر دیانای روی سرطان پروستات در حیوانات هستند تا در صورت موفقیت، تجاریسازی این سیستم دارویی را پیگیری کنند. نتایج این پروژه میتواند منجر به تولید داروهای جدید شود. «هانادی اسلیمان» از محققان این پروژه میگوید: این پروژه برای توسعه سیستمهای رهایش دارویی بسیار مهم است، از سوی دیگر این پروژه از نظر فناوری نانو و زیستشناسی نیز حائز اهمیت است.
محققان دانشگاه مکگیل کانادا موفق به طراحی نانوقفسهای مبتنی بر رشتههای دیانای شدند که از آن میتوان برای رهایش هوشمند دارو استفاده کرد. در حال حاضر این گروه تحقیقاتی در حال مطالعه اثربخشی این نانوقفسههای مبتنی بر دیانای روی سرطان پروستات در حیوانات هستند تا در صورت موفقیت، تجاریسازی این سیستم دارویی را پیگیری کنند. نتایج این پروژه میتواند منجر به تولید داروهای جدید شود. «هانادی اسلیمان» از محققان این پروژه میگوید: این پروژه برای توسعه سیستمهای رهایش دارویی بسیار مهم است، از سوی دیگر این پروژه از نظر فناوری نانو و زیستشناسی نیز حائز اهمیت است.  يك مطالعه كه به تازگي انجام شده است نشان مي دهد كه مصرف مكمل هاي معدني و مولتي ويتامين ها در پيشگيري و مقابله با سرطان پستان كمك مي كند. مصرف مكمل هاي معدني و مولتي ويتامين ها نه تنها بدن را تقويت مي كند، بلكه براساس اين مطالعه كه در آمريكا انجام شده است به پيشگيري و مقابله با سرطان پستان در زنان يائسه كمك مي كند.
يك مطالعه كه به تازگي انجام شده است نشان مي دهد كه مصرف مكمل هاي معدني و مولتي ويتامين ها در پيشگيري و مقابله با سرطان پستان كمك مي كند. مصرف مكمل هاي معدني و مولتي ويتامين ها نه تنها بدن را تقويت مي كند، بلكه براساس اين مطالعه كه در آمريكا انجام شده است به پيشگيري و مقابله با سرطان پستان در زنان يائسه كمك مي كند.  یک تیم تحقیقاتی در مرکز سرطان جانسون موفق به ارائه یک سیستم دارویی شامل نانوذرات الماس شدند که میتواند سلولهای سرطان مغز را از بین ببرد بدون این که به سلولهای سالم اطراف اثری داشته باشد. عوامل شیمیدرمانی نظیر دوکسوروبیسین دارای عوارض جانبی زیادی روی بدن هستند که با سیستم دارویی جدید که در آن از نانوذرات الماس به عنوان حمل کننده داروی شیمیدرمانی برای رهایش مستقیم در تومور مغز استفاده شده، عوارض جانبی دارو کاهش یافته و اثربخشی آن بالا رفته است.
یک تیم تحقیقاتی در مرکز سرطان جانسون موفق به ارائه یک سیستم دارویی شامل نانوذرات الماس شدند که میتواند سلولهای سرطان مغز را از بین ببرد بدون این که به سلولهای سالم اطراف اثری داشته باشد. عوامل شیمیدرمانی نظیر دوکسوروبیسین دارای عوارض جانبی زیادی روی بدن هستند که با سیستم دارویی جدید که در آن از نانوذرات الماس به عنوان حمل کننده داروی شیمیدرمانی برای رهایش مستقیم در تومور مغز استفاده شده، عوارض جانبی دارو کاهش یافته و اثربخشی آن بالا رفته است.  محققان دانشگاه ییل دریافتهاند ژنی که خون را از وجود سرطان مصون میدارد، توسط ذرات ریز RNA کنترل میشود؛ این یافته میتواند راهها و حتی درمانهای جدیدی را برای تشخیص سرطان خون پیش رو بگذارد. محققان چند سال پیش متوجه نقش اساسی ژن "TET2" در حفظ سلامت سلولهای خونی شدند. جهشهای این ژن، در حدود 20 درصد سرطانهای خون مشاهده شده بود و باور بر این میرفت که در 80 درصد بیماران، این ژن با سرطان خون مرتبط نیست و در نتیجه به عنوان شاخص ضعیفی در تشخیص این بیماری در نظر گرفته میشد.
محققان دانشگاه ییل دریافتهاند ژنی که خون را از وجود سرطان مصون میدارد، توسط ذرات ریز RNA کنترل میشود؛ این یافته میتواند راهها و حتی درمانهای جدیدی را برای تشخیص سرطان خون پیش رو بگذارد. محققان چند سال پیش متوجه نقش اساسی ژن "TET2" در حفظ سلامت سلولهای خونی شدند. جهشهای این ژن، در حدود 20 درصد سرطانهای خون مشاهده شده بود و باور بر این میرفت که در 80 درصد بیماران، این ژن با سرطان خون مرتبط نیست و در نتیجه به عنوان شاخص ضعیفی در تشخیص این بیماری در نظر گرفته میشد.  بر اساس پژوهشی که توسط انجمن سرطان آمریکا منتشر شده است، بزرگسالان با حداقل 150 دقیقه فعالیت با شدت متوسط یا 75 دقیقه فعالیت با شدت شدید در هر هفته، که ترجیحا در طول هفته به صورت متناوب انجام میشود، میتوانند به کاهش خطر ابتلا به سرطان پستان کمک کنند. یک مطالعه بزرگ که نتایج آن اخیرا در مجله «اپیدمیولوژی سرطان، شاخصهای زیستی و پیشگیری» منتشر شده است، پیاده روی با کاهش خطر ابتلا به سرطان پستان در زنانی که به سن یائسگی رسیدهاند در ارتباط بود.
بر اساس پژوهشی که توسط انجمن سرطان آمریکا منتشر شده است، بزرگسالان با حداقل 150 دقیقه فعالیت با شدت متوسط یا 75 دقیقه فعالیت با شدت شدید در هر هفته، که ترجیحا در طول هفته به صورت متناوب انجام میشود، میتوانند به کاهش خطر ابتلا به سرطان پستان کمک کنند. یک مطالعه بزرگ که نتایج آن اخیرا در مجله «اپیدمیولوژی سرطان، شاخصهای زیستی و پیشگیری» منتشر شده است، پیاده روی با کاهش خطر ابتلا به سرطان پستان در زنانی که به سن یائسگی رسیدهاند در ارتباط بود.  مطالعه جدید نشان میدهد افراد متاهلی که مبتلا به سرطان هستند، در مقایسه با افراد مجرد، مدت طولانیتری زندگی میکنند. تحقیقات محققان «موسسه سرطان دانا-فاربر» و بریگهام و بیمارستان زنان امریکا همچنین نشان میدهد سرطان افراد متاهل در مراحل زودتری تشخیص داده میشود. افزون بر این، این افراد همچنین اغلب فرایند درمانی موفقیتآمیزتری دارند و درمان مناسبتری را نیز دریافت میکنند.
مطالعه جدید نشان میدهد افراد متاهلی که مبتلا به سرطان هستند، در مقایسه با افراد مجرد، مدت طولانیتری زندگی میکنند. تحقیقات محققان «موسسه سرطان دانا-فاربر» و بریگهام و بیمارستان زنان امریکا همچنین نشان میدهد سرطان افراد متاهل در مراحل زودتری تشخیص داده میشود. افزون بر این، این افراد همچنین اغلب فرایند درمانی موفقیتآمیزتری دارند و درمان مناسبتری را نیز دریافت میکنند.  تحقيقات جديد محققان اسكاتلندي نشان مي دهد افرادي كه كمربند تنگ مي پوشند بيشتر از ديگران در معرض خطر ابتلا به سرطان گلو و دستگاه گوارش قرار دارند. محققان دانشگاه هاي گلاسكو و استراتكلايد و بيمارستان عمومي جنوب اسكاتلند گفتند : استفاده از كمربند تنگ خطر ابتلا به سرطان گلو و دستگاه گوارش را افزايش مي دهد. اين خطر در افرادي كه اضافه وزن دارند بيشتر از ديگران است.
تحقيقات جديد محققان اسكاتلندي نشان مي دهد افرادي كه كمربند تنگ مي پوشند بيشتر از ديگران در معرض خطر ابتلا به سرطان گلو و دستگاه گوارش قرار دارند. محققان دانشگاه هاي گلاسكو و استراتكلايد و بيمارستان عمومي جنوب اسكاتلند گفتند : استفاده از كمربند تنگ خطر ابتلا به سرطان گلو و دستگاه گوارش را افزايش مي دهد. اين خطر در افرادي كه اضافه وزن دارند بيشتر از ديگران است. محققان یک مارکرزیستی را کشف کرده اند که می تواند هدف درمانی بالقوه ای برای سرطان لوزالمعده باشد. محققان یک مارکر زیستی به نام
محققان یک مارکرزیستی را کشف کرده اند که می تواند هدف درمانی بالقوه ای برای سرطان لوزالمعده باشد. محققان یک مارکر زیستی به نام  استفاده از داروهای فشار خون مانند لوزارتان می تواند با باز کردن رگ ها خونی تخریب شده در تومورهای جامد در بهبود پیامد شیمی درمانی سرطان کمک مؤثری کند. دانشمندان توضیح دادند که چگونه داروی لوزارتان که مهار کننده آنژیوتانسین می باشد، انتقال داروهای شیمی درمانی و اکسیژن را با افزایش جریان خون به تومور در مدل های موشی سرطان سینه و پانکراس بهبود می بخشد.
استفاده از داروهای فشار خون مانند لوزارتان می تواند با باز کردن رگ ها خونی تخریب شده در تومورهای جامد در بهبود پیامد شیمی درمانی سرطان کمک مؤثری کند. دانشمندان توضیح دادند که چگونه داروی لوزارتان که مهار کننده آنژیوتانسین می باشد، انتقال داروهای شیمی درمانی و اکسیژن را با افزایش جریان خون به تومور در مدل های موشی سرطان سینه و پانکراس بهبود می بخشد. با کشفیات تازه در حوزه ژنتیک و مسیرهای پیام رسانی سلولی تومورهای تیروئید، محققان دانشگاه پنسیلوانیا موفق به توسعه سلاح جدیدی برای مقابله با سرطان تیروئید شدند. هیچ روش درمانی موثری برای بیماران مبتلا به سرطان تیروئید پیشرفته وجود ندارد، اما دستاوردهای اخیر محققان میتواند امیدهای تازهای برای بیماران ایجاد کند.
با کشفیات تازه در حوزه ژنتیک و مسیرهای پیام رسانی سلولی تومورهای تیروئید، محققان دانشگاه پنسیلوانیا موفق به توسعه سلاح جدیدی برای مقابله با سرطان تیروئید شدند. هیچ روش درمانی موثری برای بیماران مبتلا به سرطان تیروئید پیشرفته وجود ندارد، اما دستاوردهای اخیر محققان میتواند امیدهای تازهای برای بیماران ایجاد کند.  به گفته محققان هلندی احتمال ابتلا به سرطان سینه و سرطان روده بزرگ در افراد مبتلا به دیابت نوع دو بیشتر بوده و خطر مرگ آنان نیز به دلیل ابتلا به این بیماریها نسبت به سایر افراد بیشتر است. محققان برای انجام این تحقیق به بررسی 20 مطالعه پیشین که بین سالهای 2007 تا 2013 بر روی حدود دو میلیون نفر انجام شده بود، پرداختند. نتایج این بررسیها حاکی از آن است که خطر ابتلا به سرطان سینه در افراد مبتلا به دیابت نوع دو حدود 23 درصد بیشتر از دیگران بوده و احتمال مرگ آنان نیز نسبت به سایر افراد 38 درصد بیشتر است.
به گفته محققان هلندی احتمال ابتلا به سرطان سینه و سرطان روده بزرگ در افراد مبتلا به دیابت نوع دو بیشتر بوده و خطر مرگ آنان نیز به دلیل ابتلا به این بیماریها نسبت به سایر افراد بیشتر است. محققان برای انجام این تحقیق به بررسی 20 مطالعه پیشین که بین سالهای 2007 تا 2013 بر روی حدود دو میلیون نفر انجام شده بود، پرداختند. نتایج این بررسیها حاکی از آن است که خطر ابتلا به سرطان سینه در افراد مبتلا به دیابت نوع دو حدود 23 درصد بیشتر از دیگران بوده و احتمال مرگ آنان نیز نسبت به سایر افراد 38 درصد بیشتر است.  محققان میگویند: مصرف روزانه آب هویج در مبتلایان به سرطان باعث توقف رشد سلولهای سرطانی میشود. بر اساس تحقیقی که در جولای 2013 در انجمن ملی سرطان آمریکا انجام شده است، با انجام سی تی اسکن مشاهده شده است که با مصرف روزانه آب هویج در بیماران سرطانی به مدت 8 هفته، رشد گرههای لنفاوی سرطانی به حالت طبیعی برگشته است.
محققان میگویند: مصرف روزانه آب هویج در مبتلایان به سرطان باعث توقف رشد سلولهای سرطانی میشود. بر اساس تحقیقی که در جولای 2013 در انجمن ملی سرطان آمریکا انجام شده است، با انجام سی تی اسکن مشاهده شده است که با مصرف روزانه آب هویج در بیماران سرطانی به مدت 8 هفته، رشد گرههای لنفاوی سرطانی به حالت طبیعی برگشته است.  پژوهشها نشان میدهد افرادی که در هنگام تشخیص بیماری سرطان متاهل هستند نسبت به افراد مجرد بیشتر زنده میمانند. در پژوهشی که در مجله سرطانشناسی بالینی منتشر شد، آمده است: احتمال مرگ بیماران سرطانی متاهل 20 درصد کمتر از بیماران سرطانی مجرد، مطلقه یا بیوه است.
پژوهشها نشان میدهد افرادی که در هنگام تشخیص بیماری سرطان متاهل هستند نسبت به افراد مجرد بیشتر زنده میمانند. در پژوهشی که در مجله سرطانشناسی بالینی منتشر شد، آمده است: احتمال مرگ بیماران سرطانی متاهل 20 درصد کمتر از بیماران سرطانی مجرد، مطلقه یا بیوه است.  محققان آمريكايي مي گويند: زردچوبه كه در ادويه كاري استفاده مي شود و به خردل، رنگ زرد مي دهد در درمان سرطان، افسردگي و ديابت موثر است. تحقيقات دانشگاه پزشكي تگزاس و مركز سرطان هوستون واقع در آمريكا نشان مي دهد كوركومين كه يكي از اجزاي تشكيل دهنده زردچوبه است مي تواند به درمان سرطان، افسردگي و ديابت كمك نمايد.
محققان آمريكايي مي گويند: زردچوبه كه در ادويه كاري استفاده مي شود و به خردل، رنگ زرد مي دهد در درمان سرطان، افسردگي و ديابت موثر است. تحقيقات دانشگاه پزشكي تگزاس و مركز سرطان هوستون واقع در آمريكا نشان مي دهد كوركومين كه يكي از اجزاي تشكيل دهنده زردچوبه است مي تواند به درمان سرطان، افسردگي و ديابت كمك نمايد.  محققان آمريكايي اعلام كردند كه باكتري Fn كه در جرم دندان و بخشهاي ديگر دهان وجود دارد، خطر ابتلا به سرطان روده بزرگ را افزايش مي دهد.محققان دانشكده دندانپزشكي كيس وسترن در كليولند آمريكا گفتند : باكتري اف ان ( Fn ) در دهان زندگي مي كند و مي تواند به بخش هاي ديگر بدن منتقل شود. اين باكتري به يك گيرنده سلولي در روده بزرگ متصل مي شود و اين روند مي تواند رشد سلول هاي سرطاني روده بزرگ را تحريك كند.
محققان آمريكايي اعلام كردند كه باكتري Fn كه در جرم دندان و بخشهاي ديگر دهان وجود دارد، خطر ابتلا به سرطان روده بزرگ را افزايش مي دهد.محققان دانشكده دندانپزشكي كيس وسترن در كليولند آمريكا گفتند : باكتري اف ان ( Fn ) در دهان زندگي مي كند و مي تواند به بخش هاي ديگر بدن منتقل شود. اين باكتري به يك گيرنده سلولي در روده بزرگ متصل مي شود و اين روند مي تواند رشد سلول هاي سرطاني روده بزرگ را تحريك كند.  محققان دانشگاه جانهاپکینز با آزمایش بر روی موشها دریافتهاند هفتهها درمان با داروی تاییدشده توسط سازمان دارو و غذای امریکا، رشد سلولهای تومور مغزی مشتقشده از بیماران انسانی بزرگسال را متوقف کرد و هیچ رد قابلشناسایی از این سلولها را به جا نگذاشت. دانشمندان حاضر در این تحقیق جهشی را در ژن IDH1 مورد هدف قرار دادند.
محققان دانشگاه جانهاپکینز با آزمایش بر روی موشها دریافتهاند هفتهها درمان با داروی تاییدشده توسط سازمان دارو و غذای امریکا، رشد سلولهای تومور مغزی مشتقشده از بیماران انسانی بزرگسال را متوقف کرد و هیچ رد قابلشناسایی از این سلولها را به جا نگذاشت. دانشمندان حاضر در این تحقیق جهشی را در ژن IDH1 مورد هدف قرار دادند.  تصور بسیاری از افراد این است که آب موجود در درون بطری تازهتر و بهتر است، اما تحقیقات جدید نشان میدهد ماده شیمیایی اتیلن دی کلراید( EDCs) موجود در آب درون بطری موجب اختلال در غدد درونریز بدن میشود. محققان با تجزیه و بررسی آب درون بطری وجود این ماده شیمیایی را شناسایی کردند که منجر به اختلال سیستم هورمونی و تولیدمثل میشود. محققان این تحقیق با بازبینی تحقیقات قبلی و بررسی 18 محصول دریافتند که این ماده شیمیایی موجب توقف فعالیت استروژن (آنتیاستروژیک) میشود و همچنین از فعالیت تاثیرات بیولوژیکی (ضدآندروژنی) جلوگیری میکند.
تصور بسیاری از افراد این است که آب موجود در درون بطری تازهتر و بهتر است، اما تحقیقات جدید نشان میدهد ماده شیمیایی اتیلن دی کلراید( EDCs) موجود در آب درون بطری موجب اختلال در غدد درونریز بدن میشود. محققان با تجزیه و بررسی آب درون بطری وجود این ماده شیمیایی را شناسایی کردند که منجر به اختلال سیستم هورمونی و تولیدمثل میشود. محققان این تحقیق با بازبینی تحقیقات قبلی و بررسی 18 محصول دریافتند که این ماده شیمیایی موجب توقف فعالیت استروژن (آنتیاستروژیک) میشود و همچنین از فعالیت تاثیرات بیولوژیکی (ضدآندروژنی) جلوگیری میکند.  براساس تحقیقات دانشکده هاروارد با سرپوش گذاشتن بر احساسات در واقع افراد از سالها زندگی خود چشمپوشی میکنند. آخرین تحقیقات نشان داده است افراد با سرکوب کردن احساسات خود حداقل یک سوم زودتر از افرادی که نظر خود را بیان میکنند، میمیرند. این تحقیق که توسط دانشمندان دانشکده بهداشت عمومی هاروارد و دانشگاه روچستر انجام شده است، نشان داد: علت خطر مرگ زودرس در بین افرادی که نظر خود را به راحتی بیان نمیکنند 35 درصد افزایش مییابد. همچنین آنها دریافتند که این موضوع 47درصد ابتلا به بیماریهای قلبی و70 درصد ابتلا به سرطانها را افزایش میدهد.
براساس تحقیقات دانشکده هاروارد با سرپوش گذاشتن بر احساسات در واقع افراد از سالها زندگی خود چشمپوشی میکنند. آخرین تحقیقات نشان داده است افراد با سرکوب کردن احساسات خود حداقل یک سوم زودتر از افرادی که نظر خود را بیان میکنند، میمیرند. این تحقیق که توسط دانشمندان دانشکده بهداشت عمومی هاروارد و دانشگاه روچستر انجام شده است، نشان داد: علت خطر مرگ زودرس در بین افرادی که نظر خود را به راحتی بیان نمیکنند 35 درصد افزایش مییابد. همچنین آنها دریافتند که این موضوع 47درصد ابتلا به بیماریهای قلبی و70 درصد ابتلا به سرطانها را افزایش میدهد.  محققان آلمانی تکنیک بسیار حساسی برای بررسی تغییرات ژنتیکی سرطان روده بزرگ توسعه دادهاند که به تشخیص زودهنگام بیماری در مراحل اولیه کمک میکند. در حدود 60 و 40 درصد از بیماران مبتلا به سرطان روده بزرگ، تغییرات ژنتیکی به ترتیب در ژنهای APC و KRAS دیده میشوند. تشخیص به موقع این تغییرات ژنتیکی در مراحل پیش از بروز کامل بیماری میتواند به اتخاذ تدابیر درمانی موثرتر منجر شود.
محققان آلمانی تکنیک بسیار حساسی برای بررسی تغییرات ژنتیکی سرطان روده بزرگ توسعه دادهاند که به تشخیص زودهنگام بیماری در مراحل اولیه کمک میکند. در حدود 60 و 40 درصد از بیماران مبتلا به سرطان روده بزرگ، تغییرات ژنتیکی به ترتیب در ژنهای APC و KRAS دیده میشوند. تشخیص به موقع این تغییرات ژنتیکی در مراحل پیش از بروز کامل بیماری میتواند به اتخاذ تدابیر درمانی موثرتر منجر شود.  محققان انگلیسی ژنی را در بدن موشها کشف کردهاند که در صورت معیوب یا ناقص بودن، خطر ابتلا به سرطان تخمدان افزایش پیدا میکند. این ژن موسوم به "Helq" میتواند هنگام تقسیم سلولی در اصلاح یا آسیب رسانی به "DNA" نقش مهمی را ایفا کند. این ژن موسوم به "Helq" میتواند آسیبهای به وجود آمده برای "DNA" را که حین نسخه برداری و در زمان تقسیم سلولی رخ میدهد، اصلاح کند؛ بنابراین اگر این ژن معیوب باشد یا در هر صورت وجود نداشته باشد، خطاهای "Helq" افزایش پیدا کرده و در نتیجه خطر سرطان افزایش پیدا میکند.
محققان انگلیسی ژنی را در بدن موشها کشف کردهاند که در صورت معیوب یا ناقص بودن، خطر ابتلا به سرطان تخمدان افزایش پیدا میکند. این ژن موسوم به "Helq" میتواند هنگام تقسیم سلولی در اصلاح یا آسیب رسانی به "DNA" نقش مهمی را ایفا کند. این ژن موسوم به "Helq" میتواند آسیبهای به وجود آمده برای "DNA" را که حین نسخه برداری و در زمان تقسیم سلولی رخ میدهد، اصلاح کند؛ بنابراین اگر این ژن معیوب باشد یا در هر صورت وجود نداشته باشد، خطاهای "Helq" افزایش پیدا کرده و در نتیجه خطر سرطان افزایش پیدا میکند. 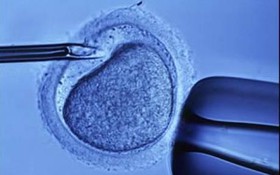 محققان استرالیایی برای اولین بار در دستاوردی چشمگیر که میتواند درمان ناباروری را متحول کند، توانستهاند به یک زن که در اثر مصرف داروی سرطان رحم ناباور شده بود، فرصت مجددی برای مادر شدن ارائه کنند. این زن موسوم به والی، پس از پرورش تخمکهای جدید در بافت پیوندی تخمدان، اکنون تقریبا در بیست و ششمین هفته بارداری خود قرار داشته و منتظر تولد یک جفت دوقلو است.
محققان استرالیایی برای اولین بار در دستاوردی چشمگیر که میتواند درمان ناباروری را متحول کند، توانستهاند به یک زن که در اثر مصرف داروی سرطان رحم ناباور شده بود، فرصت مجددی برای مادر شدن ارائه کنند. این زن موسوم به والی، پس از پرورش تخمکهای جدید در بافت پیوندی تخمدان، اکنون تقریبا در بیست و ششمین هفته بارداری خود قرار داشته و منتظر تولد یک جفت دوقلو است.  محققان با قراردادن آنتیبادیهای ضد سرطان درون یک نانوذره زیستسازگار، نه تنها موفق به از بین بردن تومورها شدند، بلکه احتمال بازگشت سرطان را نیز به حداقل رساندند. هرسپتین و کامپتوتسین دو عامل ضد سرطان بسیار قوی هستند که میتوانند در درمان سرطان بسیار اثربخش باشند. هرسپتین یک آنتیبادی برای هدف قرار دادن فاکتور رشد در سرطان سینه است، بیمارانی که این آنتیبادی را دریافت میکنند، برای مدتی رشد تومور در آنها کند میشود، ولی بعد از مدتی تومور به رشد عادی خود ادامه میدهد که دلیل این امر مقاومت تومور به این آنتیبادی است. برای حل این مشکل یک تیم تحقیقاتی از موسسه فناوری کالیفرنیا به رهبری «مارک دیویس» سیستم جدیدی ارائه کردند که در آن اثربخشی داروی ضد سرطان سینه با استفاده از فناوری نانو بهبود پیدا میکند. این که از نانوذرات برای تولید داروی ضد سرطان استفاده شود چیز جدیدی نیست، آنچه که این گروه برای اولین بار ارائه کردند این است که یک آنتیبادی منفرد به یک نانوذره متصل میشود و هر دوی آنها به عنوان یک داروی ضد سرطان عمل میکنند.
محققان با قراردادن آنتیبادیهای ضد سرطان درون یک نانوذره زیستسازگار، نه تنها موفق به از بین بردن تومورها شدند، بلکه احتمال بازگشت سرطان را نیز به حداقل رساندند. هرسپتین و کامپتوتسین دو عامل ضد سرطان بسیار قوی هستند که میتوانند در درمان سرطان بسیار اثربخش باشند. هرسپتین یک آنتیبادی برای هدف قرار دادن فاکتور رشد در سرطان سینه است، بیمارانی که این آنتیبادی را دریافت میکنند، برای مدتی رشد تومور در آنها کند میشود، ولی بعد از مدتی تومور به رشد عادی خود ادامه میدهد که دلیل این امر مقاومت تومور به این آنتیبادی است. برای حل این مشکل یک تیم تحقیقاتی از موسسه فناوری کالیفرنیا به رهبری «مارک دیویس» سیستم جدیدی ارائه کردند که در آن اثربخشی داروی ضد سرطان سینه با استفاده از فناوری نانو بهبود پیدا میکند. این که از نانوذرات برای تولید داروی ضد سرطان استفاده شود چیز جدیدی نیست، آنچه که این گروه برای اولین بار ارائه کردند این است که یک آنتیبادی منفرد به یک نانوذره متصل میشود و هر دوی آنها به عنوان یک داروی ضد سرطان عمل میکنند.