..:::: مصرف زیاد کلسیم خطر مرگ را افزایش میدهد ::::..
 نتایج یک تحقیق نشان داد که مصرف کم یا زیاد کلسیم میتواند خطر مرگ ناشی از بیماریهای قلبی عروقی در زنان را افزایش دهد. گروهی از محققان با انجام آزمایشها بر روی 61443 زن در سوئد و بررسی رژیم غذایی آنها و نیز منظور کردن اطلاعات آنها درخصوص وضعیت یائسگی، درمان با استروژن پس از یائسگی، وزن و قد، عادات سیگار کشیدن و فعالیت بدنی دریافتند مصرف بالای کلسیم خطر وقوع مرگ و میر ناشی از بیماریهای قلبی عروقی را میان زنان تا 2 برابر افزایش میدهد.
نتایج یک تحقیق نشان داد که مصرف کم یا زیاد کلسیم میتواند خطر مرگ ناشی از بیماریهای قلبی عروقی در زنان را افزایش دهد. گروهی از محققان با انجام آزمایشها بر روی 61443 زن در سوئد و بررسی رژیم غذایی آنها و نیز منظور کردن اطلاعات آنها درخصوص وضعیت یائسگی، درمان با استروژن پس از یائسگی، وزن و قد، عادات سیگار کشیدن و فعالیت بدنی دریافتند مصرف بالای کلسیم خطر وقوع مرگ و میر ناشی از بیماریهای قلبی عروقی را میان زنان تا 2 برابر افزایش میدهد.
محققان با انجام یک پیگیری 19 ساله مشاهده کردند که 32 درصد از 11944 نفر از زنانی که فوت کردهاند بر اثر بیماریهای قلبی عروقی، 16 درصد از بیماریهای قلبی و 8 درصد بر اثر سکته مغزی بوده است. بالاترین میزان وقوع مرگ و میر در اثر بیماریهای قلبی عروقی در میان زنانی بود که به میزان بالاتر از 1400 میلی گرم در روز کلسیم مصرف میکردند. نتایج حاصل از این مطالعه همچنین نشان داد: میزان مرگ و میر زیادی نیز در میان زنانی که کمتر از600 میلیگرم در روز کلسیم را از رژیم غذایی و یا مکملهای کلسیم به دست میآوردند، مشاهده شد و در این میان زنانی که بیشتر از 1400 میلیگرم در روز کلسیم دریافت میکردند تا 2 برابر بیشتر از زنانی که بین 999 – 600 میلیگرم در روز کلسیم مصرف میکردند در معرض احتمال وقوع مرگ و میر قرار گرفتند. به گفته محققان این یافتهها نشان میدهد که رژیمهای غذایی حاوی مقادیر بسیار کم یا مقادیر بسیار زیاد کلسیم در زنان میتواند تعادل نرمال آن را برهم زند و باعث تغییراتی در سطح کلسیم خون شود که پیامدهای نامطلوبی را پی خواهد داشت.
 استفاده از فضولات انسانی به عنوان منبع غنی تامین سلول های مورد نیاز در مطالعات پزشکی، می تواند برخی از مشکلات استفاده از سلول های بنیادی را برطرف کند.
استفاده از فضولات انسانی به عنوان منبع غنی تامین سلول های مورد نیاز در مطالعات پزشکی، می تواند برخی از مشکلات استفاده از سلول های بنیادی را برطرف کند. محققان سوئیسی از نخستین پیوند دست مصنوعی با قابلیت بازگرداندن حس لامسه به افراد معلول در آینده نزدیک خبر میدهند.
محققان سوئیسی از نخستین پیوند دست مصنوعی با قابلیت بازگرداندن حس لامسه به افراد معلول در آینده نزدیک خبر میدهند. 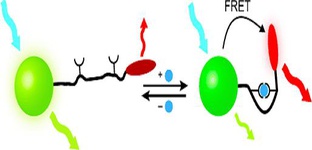 پژوهشگران
پژوهشگران پژوهش جدید دانشمندان دانشگاه وولورهامپتون نشان داد که طب سنتی آفریقایی ممکن است از کلید درمان زخمهایی برخوردار باشد که با طب مدرن در تضاد است.
پژوهش جدید دانشمندان دانشگاه وولورهامپتون نشان داد که طب سنتی آفریقایی ممکن است از کلید درمان زخمهایی برخوردار باشد که با طب مدرن در تضاد است.  دانشمندان درحال بررسی درمان درد مفاصل با تزریق خون به زانوی بیمار هستند.
دانشمندان درحال بررسی درمان درد مفاصل با تزریق خون به زانوی بیمار هستند.  پژوهشگران دانشگاه اوتاوا مکانیزمی را کشف کردهاند که طی آن سلولهای بنیادی عضله به چربی قهوهای تبدیل میشود؛ این نوع چربی نقش جدی را در مبارزه با چاقی ایفا میکند.
پژوهشگران دانشگاه اوتاوا مکانیزمی را کشف کردهاند که طی آن سلولهای بنیادی عضله به چربی قهوهای تبدیل میشود؛ این نوع چربی نقش جدی را در مبارزه با چاقی ایفا میکند. محققان موسسه فرانهوفر آلمان، دسته سنجش فشار ابزار جراحی مجهز به لامپ
محققان موسسه فرانهوفر آلمان، دسته سنجش فشار ابزار جراحی مجهز به لامپ پژوهشگران موسسه فناوری سلطنتی ملبورن، نانوذراتی تولید کردهاند که بسیار ارزان و غیرسمی بوده و از آن میتوان برای رادیودرمانی سرطان استفاده کرد.
پژوهشگران موسسه فناوری سلطنتی ملبورن، نانوذراتی تولید کردهاند که بسیار ارزان و غیرسمی بوده و از آن میتوان برای رادیودرمانی سرطان استفاده کرد.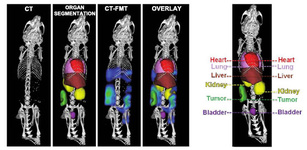 یک تیم تحقیقات بینالمللی روشی جدید برای رصد زیست مولکولها در بدن ارائه کرده است. این روش ترکیبی از سی تی اسکن و تصویربرداری انعکاسی فلورسانس است.
یک تیم تحقیقات بینالمللی روشی جدید برای رصد زیست مولکولها در بدن ارائه کرده است. این روش ترکیبی از سی تی اسکن و تصویربرداری انعکاسی فلورسانس است.  محققان دانشگاه رایس روشی ارائه کردهاند که با استفاده از آن میتوان برخی سلولهای بیمار را از بین برد و برخی دیگر را درمان کرد.
محققان دانشگاه رایس روشی ارائه کردهاند که با استفاده از آن میتوان برخی سلولهای بیمار را از بین برد و برخی دیگر را درمان کرد.  پژوهش محققان دانشگاه لیدز نشان میدهد که مواد شیمیایی طبیعی موجود در چای سبز میتواند مرحله اصلی بیماری آلزایمر را مختل کند.
پژوهش محققان دانشگاه لیدز نشان میدهد که مواد شیمیایی طبیعی موجود در چای سبز میتواند مرحله اصلی بیماری آلزایمر را مختل کند. قارچ «
قارچ « دانشمندان دانشگاه مینوستا "اسفنج کلسیمی" مولکولی را طراحی کردند که با نارساییهای قلبی مقابله میکند.
دانشمندان دانشگاه مینوستا "اسفنج کلسیمی" مولکولی را طراحی کردند که با نارساییهای قلبی مقابله میکند. 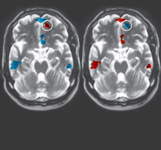 دانشمندان دانشگاه براون نشان دادهاند که اسکنهای مغزی میتواند میزان دوام عشق در میان زوجها را تخمین بزنند.
دانشمندان دانشگاه براون نشان دادهاند که اسکنهای مغزی میتواند میزان دوام عشق در میان زوجها را تخمین بزنند.  محققان دانشگاه پرینستون در حال کار بر روی نوعی خالکوبی هستند که دیگران را از بیمار بودن فرد در مواقع ضروری آگاه میکند
محققان دانشگاه پرینستون در حال کار بر روی نوعی خالکوبی هستند که دیگران را از بیمار بودن فرد در مواقع ضروری آگاه میکند دانشمندان موسسه فناوری کالیفرنیا موفق به شناسایی نورونهایی در موشها شدهاند که در واکنش به نوازش و ماساژ فعال میشوند.
دانشمندان موسسه فناوری کالیفرنیا موفق به شناسایی نورونهایی در موشها شدهاند که در واکنش به نوازش و ماساژ فعال میشوند.  محققان آمریکایی دستگاه اسکنر دستی غیرتهاجمی طراحی کردهاند که عملکردی مشابه دستگاه سی تی اسکن داشته و میتواند خونریزی مغزی را به سرعت تشخیص دهد.
محققان آمریکایی دستگاه اسکنر دستی غیرتهاجمی طراحی کردهاند که عملکردی مشابه دستگاه سی تی اسکن داشته و میتواند خونریزی مغزی را به سرعت تشخیص دهد.  محققان آمریکایی دستگاه قابل کنترل از راه دوری طراحی کرده اند که زیر گونه بیمار کاشته شده و با ایجاد بار الکتریکی ضعیف به توقف سردردهای شدید بویژه در بیماران میگرنی کمک می کند.
محققان آمریکایی دستگاه قابل کنترل از راه دوری طراحی کرده اند که زیر گونه بیمار کاشته شده و با ایجاد بار الکتریکی ضعیف به توقف سردردهای شدید بویژه در بیماران میگرنی کمک می کند.  محققان دانشگاه استنفورد روش جدید ژن درمانی را توسعه دادهاند که سلولهای کلیدی سیستم ایمنی بدن را در مقابل حملات ویروس
محققان دانشگاه استنفورد روش جدید ژن درمانی را توسعه دادهاند که سلولهای کلیدی سیستم ایمنی بدن را در مقابل حملات ویروس یک افزاره همراه که از پیشرفتهترین فناوری نانو برای آشکارسازی سریع عفونت مالاریا و مقاومت دارویی استفاده میکند، میتواند در نحوه تشخیص و درمان بیماری انقلابی ایجاد کند.
یک افزاره همراه که از پیشرفتهترین فناوری نانو برای آشکارسازی سریع عفونت مالاریا و مقاومت دارویی استفاده میکند، میتواند در نحوه تشخیص و درمان بیماری انقلابی ایجاد کند. مصرف بیش از حد قند و وقوع دیابت میتواند باعث افزایش بروز سرطان در افراد شود.
مصرف بیش از حد قند و وقوع دیابت میتواند باعث افزایش بروز سرطان در افراد شود.  گیاهخواری میتواند خطر وقوع بیماریهای قلبی را تا یک سوم کاهش دهد.
گیاهخواری میتواند خطر وقوع بیماریهای قلبی را تا یک سوم کاهش دهد.  کشف ژن جدید سکته مغزی میتواند منجر به طراحی درمانهای جدید شود.
کشف ژن جدید سکته مغزی میتواند منجر به طراحی درمانهای جدید شود.